Роль поджелудочной железы гипофиза и надпочечников
Экстренная медицина
Физиология гипоталамуса. Гипоталамус входит в систему гипоталамус — гипофиз — надпочечники; где он выполняет роль высшего подкоркового эндокринного регулятора. Посредником в выполнении этой функции является нейросекреция — выделение факторов стимуляции функции гипофиза. Эти вещества были открыты Р.Гиллеминым и Э.Шелли и первоначально были названы рилизинг —факторами, т.е. освобождающими, растормаживающими гормональную функцию гипофиза. Теперь известно, что гипоталамус вырабатывает как усиливающие, так и угнетающие функцию гипофиза нейропептиды (либерины и статины). В частности, соматостатин тормозит выработку соматотропного гормона, а соматолиберин стимулирует его образование гипофизом. Происходит это вследствие усиления или угнетания образования циклического АМФ в клетках гипофиза. Статины тормозят образование ц-АМФ и снижают содержание свободных катионов Са2+ в клетках гипофиза. В результате этого снижается биосинтез гормона роста и его выход из клеток гипофиза.
В гипоталамусе вырабатываются факторы, стимулирующие образование тропных гормонов гипофиза.
Физиология гипофиза. Гипофиз связан с серым бугром и передними ядрами гипоталамуса (супраоптическое и паравен-трикулярное) через воронку и ножку, что обусловливает его тесную морфофункциональную связь с высшим подкорковым регулятором эндокринной функции.
Гипофиз состоит из железистой и нервной ткани. В эмбриогенезе из складки на стенке ротовой полости развиваются железистые ткани — передняя и промежуточная доли (аденогипофиз). Вторая часть гипофиза — нейрогипофиз состоит из нервной ткани. Передняя доля гипофиза связана с гипоталамусом сетью кровеносных сосудов, по которым поступают освобождающие (растормаживающие функцию передней доли) или тормозящие факторы гипоталамуса. В задней доле гипофиза оканчиваются аксоны нервных клеток гипоталамуса, продуцирующих гормоны.
В передней доле гипофиза вырабатывается гормон роста — соматотропин и группа тропных гормонов, обеспечивающих пусковое влияние на надпочечник, половые железы, щитовидную железу. Соматотропин стимулирует биосинтез белков в клетках и тканях растущего организма (повышает синтез РНК, усиливает транспорт аминокислот из крови к клеткам и тканям организма).
Опосредованно, через гормоны соматомедины, соматотронин увеличивает проницаемость клеточных мембран для питательных и биологически активных веществ. Следовательно с секрецией соматотропина связан обмен веществ в целом и нарушение его функции приводит к чрезвычайно сложным перестройкам как в растущем, так и в зрелом организме.
Повышенная продукция соматотропина в детском и подростковом возрасте приводит к гигантизму. При искусственном введении гормона роста детям, страдающим недостаточностью функции гипофиза, их рост увеличивался в течение 6 месяцев лечения на 5 —6 см. При гиперфункции гипофиза рост людей, как правило, превышает 2 м (рис. 90). Известно, что римский император Максимилиан имел рост 2,5 м, а русский крестьнин Махнов — 2,85 м. У женщин наибольший рост отмечен у швейцарки Амы — 2,35 м. Самый высокий человек в мире, описанный в литературе, имел рост 3,20 м.
Гигантизм, как правило, сопровождается акромегалией — разрастанием костей лица, рук и стопы (рис. 91). Гипофункция передней доли гипофиза приводит к задержке роста. Больные при этом имеют рост от нескольких десятков сантиметров до 1 м (гипофизарные карлики). Египетская карлица Агибе имела рост 38 см.
Передняя доля гипофиза выделяет группу тройных гормонов. Группа гонадотропных гормонов (фолликулостимулирующий, лютеинизирующий гормоны, пролактин) стимулируют формообразовательную и секторную функции половых желез.
Фолликулостимулирующий гормон гипофиза обусловливает цикличность в созревании женских половых клеток и образование фолликулов. У мужчин этот гормон усиливает сперматогенез. Под его влиянием разрастается сперматогенная ткань и усиливается развитие сперматозоидов.
Лютеинизирующий гормон у женщин регулирует овуляцию и образование желтого тела. У мужчин он выступает регулятором продукции половых гормонов — андрогенов. Пролактин стимулирует лактацию у женщин, а также развитие желтого тела беременности.
Тиротропный гормон тиротропин увеличивает продукцию гормонов щитовидной железы. Он оказывает влияние на рост железистого эпителия, усиливает его секрецию.
Адренокортикотропный гормон (АКТГ вызывает усиленный биосинтез гормонов пучковой и сетчатой зоны коры надпочечников. Продукция АКТГ увеличивается под воздействием стрессовых раздражителей. В практике физического воспитания это соревновательные и высокие тренировочные нагрузки, а также предстартовые волнения, связанные с выступлениями в соревнованиях. В физиологических механизмах стимулирующего воздействия физических нагрузок важное место занимает увеличение производства адреналина под воздействием стрессорных раздражителей. Адреналин действует на ядра гипоталамуса, вырабатывающие АКТГ — освобождающий фактор.
Гормоны передней доли гипофиза оказывают неспецифическое влияние на обмен веществ, выступая регуляторами белкового, жирового и углеводного обмена. Вытяжки из тканей передней доли гипофиза усиливают синтез гликогена из жиров и белков, ускоряют дезаминирование белков печенью.
В заднюю долю гипофиза (нейрогипофиз) по длинным отросткам нервных клеток гипоталамуса поступают два гормона — вазопрессин и окситоцин. Вазопрессин называется иначе антидиуретическим гормоном (АДГ). Он усиливает реабсорбцию воды в дистальных почечных канальцах и в собирательных трубках, увеличивая их проницаемость для воды. При гипофункции задней доли гипофиза развивается болезнь несахарный диабет. Суточный диурез больного достигает нескольких десятков литров. Побочное действие АДГ сказывается на повышении артериального давления.
Окситоцин оказывает неодинаковое действие на матку в разные сроки беременности. В начале беременности матка нечувствительна к окситоцину. К моменту наступления родов чувствительность матки к окситоцину возрастает. Это связано с угасанием гормональной функции желтого тела. Родовая деятельность под влиянием окситоцина усиливается.
Средняя (межуточная) доля гипофиза секретирует мелано-форный (пигментостимулирующий) гормон интермедии. Его действие проявляется в усилении пигментообразующей функции кожи.
Физиология надпочечников. В 1855 г. английский врач Адди-сон впервые описал больного, страдающего бронзовой болезнью. Эта болезнь, названная позднее аддисоновой, — результат атрофических изменений обоих надпочечников. Атрофия надпочечников сопровождается хронической недостаточностью функции их коркового слоя. Адцисонова болезнь характеризуется общи нарушением обменных процессов, отсутствием аппетита, тошнотой, рвотой, болями в области живота. У больного быстро уменьшается масса, наступает истощение, появляются темные пятна на слизистых оболочках губ, десен. Кожа лица и открытых частей тела приобретает цвет старой бронзы.
Надпочечникам принадлежит роль важнейшего регулятора сложных взаимоотношений организма и среды в стрессовых ситуациях. Реакция напряжения, проявляющаяся в резком увеличении энергопроизводства и стимулировании физической работоспособности человека, теснейшим образом связана с усилением гормональной функции надпочечников.
Надпочечники состоят из коркового и мозгового слоев. Корковый слой, в свою очередь, имеет три зоны: внутреннюю — сетчатую, среднюю — пучковую и наружную — клубочковую. Сетчатая зона вырабатывает половые гормоны: андрогены, эстрогены, прогестерон. Пучковая зона продуцирует глюкокортикоиды (кортизон, гидрокортизон). Наружная (клубочковая) зона вырабатывает минералокортикоиды (альдостерон и др.).
Сетчатая доля надпочечников является источником половых гормонов в детском возрасте, когда внутрисекреторная функция половых желез практически отсутствует. На закате жизни, после наступления климактерического периода, сетчатая зона надпочечников остаётся единственным местом, где образуются половые гормоны.
Глюкокортикоиды (кортизон, кортикостерон, дегидрокорти-костерон) регулируют углеводный обмен, в особенности его промежуточные этапы. Кортизон регулирует образование гликогена, задерживает расщепление углеводов и превращение их в жир. Кортикостерон и дегидрокортикостерон повышают уровень сахара в крови. Корковые стероидные гормоны стимулируют физическую работоспособность, снижают утомляемость скелетных мышц. Кортизон обладает высокой противовоспалительной активностью и может с успехом применяться при лечении некоторых видов воспалений.
Минералокортикоиды регулируют водный и минеральный обмен. Так, альдостерон увеличивает реабсорбцию Na+ и выведение К+ с мочой. Альдостерон обладает и антидиуретическим действием. Реабсорбция Na+ приводит к увеличению его концентрации в капиллярах почечной ткани и интерстициальной жидкости мозгового слоя почки. Это приводит к усилению обратного всасывания воды из почечных каналов и собирательных трубок. Количество дефинитивной (конечной) мочи уменьшается.
Общим предшественником кортикоидных и половых гормонов является холестерин. Гормоны мозгового слоя надпочечников (адреналин и норадреналин) оказывают выраженное стимулирующее влияние на мышечную работоспособность. Она поддерживается мобилизацией гликогена печени и мышц, активацией функций сердечно-сосудистой и дыхательной систем. Повышенная секреция адреналина и норадреналина стимулирует синтез стероидных гормонов.
Фомин А. Ф. Физиология человека, 1995 г.
Основная информация
Под влиянием определенных факторов количество гормонов, вырабатываемых надпочечниками, может существенно снижаться, причиняя серьезный вред здоровью человека.
Патология способна затрагивать сразу все гормоны или только одно конкретное вещество. Различают две формы гипофункции надпочечников:
- Острая (аддисонический кризис). Характеризуется резким прекращением продуцирования гормонов, например, под воздействием тяжелых инфекций.
- Хроническая (болезнь Аддисона). Способна длиться годами, обостряясь после перенесенных болезней, длительных стрессов или травм.
Также в зависимости от локализации первопричины патологии его принято разделять на:
- Первичный (встречается в 90% всех случаев). Развивается в результате поражения самих надпочечников.
- Вторичный. Сбой в работе возникает как следствие проблем с гипофизом, под влиянием которых резко падает уровень АКТГ, или адренокортикотропного гормона, отвечающего за стимуляцию деятельности надпочечников.
- Третичный. В основе патологии лежат нарушения в функционировании гипоталамуса, который перестает подавать гипофизу сигналы, необходимые для регуляции работы надпочечников.
В отдельную форму принято также выделять медикаментозную, или ятрогенную, недостаточность, развивающуюся после резкой отмены длительной гормональной терапии, но встречается она довольно редко, всего в 4-11 случаях на 100 тысяч пациентов.
Этиология заболевания
Практически в 98% случаев снижение активности надпочечников является следствием аутоиммунных заболеваний, при которых антитела атакуют ткани органов.
Гораздо реже встречаются другие причины первичного гипокортицизма:
- инфекционные поражения надпочечников, в первую очередь, туберкулез;
- врожденные патологии;
- злокачественные новообразования и метастазы;
- осложнения после оперативного вмешательства;
- необратимые повреждения тканей при ВИЧ-инфекции и т. д.
Развитие вторичной или третичной гипофункции могут спровоцировать:
- нарушения в работе эндокринной системы;
- кровоизлияния в надпочечники в результате полученных травм;
- опухоли головного мозга;
- врожденные аномалии гипофиза и гипоталамуса.
Кроме этого, в основе аддисонических кризисов могут лежать тяжелые инфекционные заболевания, например, герпес или дифтерия, тромбозы, раковые опухоли надпочечников и даже синдром резкой отмены лекарств. А у детей младше 3 лет снизить активность надпочечников может и банальная простуда или сильный стресс.
Методы диагностики
Для постановки правильного диагноза пациентам с подозрением на гипофункцию надпочечников назначается целый ряд анализов и обследований, среди которых наиболее показательным является определение уровня кортизола и альдостерона в крови. Помимо этого проводится общий анализ крови для выявления нарушений метаболизма, диагностика уровня АКТГ в крови и анализ мочи на количество метаболитов кортизола. Кроме этого, важной частью диагностики является УЗИ надпочечников, а также КТ и МРТ головного мозга.
Такой подход позволяет узнать истинную причину гипофункции и подобрать лечение, направленное на ее устранение.
Кроме этого, у пациентов берутся иммунологические пробы для выявления возможных аутоиммунных заболеваний, оценивается вероятность туберкулеза и назначается ЭКГ сердца, чтобы определить, отразились ли проблемы с надпочечниками на его работе.
Расположение в мозге
Теперь обсудим, где именно в мозге находятся эти структуры — гипофиз, гипоталамус, эпифиз. Гипофиз находится у основания мозга, внизу в костном кармане, называемом «турецким седлом». Он расположен близко к спинному мозгу. Через его протоки все вещества, вырабатываемые гипоталамо-гипофизарной системой, поступают в организм.
Гипоталамус — hypothalamus, от греч. отделение или комната. Он входит в промежуточный отдел мозга и является основным регулятором нервных процессов. Находится под зрительными буграми, позади среднего отдела мозга.

Таблица. Гормоны гипофиза
| Полное название гормона | Сокращенное название гормона |
| Тропные гормоны | |
| Фолликулостимулирующий гормон | ФСГ |
| Лютеинизирующий гормон | ЛГ |
| Тиреотропный гормон | ТТГ |
| Адренокортикотропный гормон | АКТГ |
| Эффекторные гормоны | |
| Гормон роста, соматотропный гормон | ГР, СТГ |
| Пролактин (лютеотропный гормон) | ПРЛ (ЛТГ) |
| Меланоцитостимулирующий гормон | МСГ |
При удалении гипофиза в организме развиваются симптомы гормональной недостаточности, так как гормоны аденогипофиза в этом случае не оказывают стимулирующего влияния на ряд эндокринных желез и функций.
Способы лечебной терапии
Стабилизация состояния больного при хроническом вялотекущем гипокортицизме в первую очередь предполагает назначение заместительной терапии, которая за счет приема синтетических препаратов позволяет приблизить количество вырабатываемых надпочечниками гормонов к необходимому уровню.
Схема лечения всегда подбирается индивидуально, в зависимости от степени развития гипофункции в надпочечниках и общего самочувствия пациента.
Так, на начальной стадии болезни может быть достаточно приема одного только кортизона, но при существенном снижении активности надпочечников необходимо использовать уже целый комплекс гормональных препаратов.
Параллельно уделяется внимание и тем патологическим факторам, которые спровоцировали развитие гипофункции, например, проводится лечение инфекционных заболеваний или хирургическое удаление новообразований.
При острой форме болезни пациенту требуется немедленная госпитализация с дальнейшим интенсивным лечением — внутривенным введением гормонов и противошоковой терапией.
Кроме этого, больным с гипофункцией надпочечников рекомендуется на протяжении всей жизни придерживаться диеты, уделяя особое внимание продуктам с повышенным содержанием белков и жирных кислот, избегать стрессов, чрезмерных физических нагрузок, контролировать вес и артериальное давление, поддерживая его на необходимом уровне.
Сфера влияния
Эндокринная система является слаженной структурой, которая поставляет организму такое количество гормонов, которое требуется для поддержания жизнедеятельности. В выработке биологически активных веществ принимают непосредственное участие:
- щитовидная железа;
- надпочечники;
- яичники;
- паращитовидная железа;
- яички и семенники;
- гипоталамус;
- поджелудочная железа.

Гипофиз находится во главе этого перечня. Именно это небольшое образование с весом не больше 0,6 г и с гипофизарной ножкой отвечает за продуцирование гормонов в таком количестве, которое необходимо организму. Многочисленные гормоны передней гипофизарной доли имеют прямое влияние на человеческое поведение и внешность. Они воздействуют на физическую способность ощущать каждый день комфорт.
За что отвечает гипофиз, интересно многим.
Источник
Нарушения углеводного обмена. Система гормонов поджелудочной железы, гипофиза и надпочечников
Гормоны щитовидной железы регулируют основные показатели обмена веществ, при этом их влияние на поставку энергии в клетки минимально. За эту функцию отвечает поджелудочная железа. В отличие от всех остальных эндокринных систем, регуляция эндокринной части поджелудочной железы идет не через гипоталамо-гипофизарную систему. Углеводный и жировой обмен регулируется следующим образом:
• сигналами, поступающими из пищеварительного канала (растяжение желудка, состав пищи);
• сигналами, поступающими из кровеносной системы (уровень циркулирующей глюкозы);
• внутриклеточными сигналами (внутриклеточные запасы энергии).
Общая гомеостатическая функция углеводного и жирового обмена — поставка энергии для использования, депонирования и мобилизации запасов энергии во время голода.
Регулирование обмена углеводов и жирных кислот — ключевая функция инсулина и ассоциированных гормонов. Поддержание адекватного уровня глюкозы в крови особенно важно для мозга и скелетных мышц.
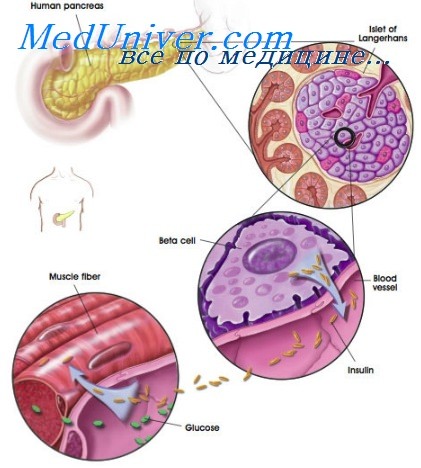
Стимуляция инсулиновых рецепторов активирует транспорт глюкозы на клеточных мембранах инсулин-чувствительных тканей. Внутриклеточные механизмы действия инсулина еще до конца не выяснены. Инсулиновые рецепторы расположены на мембранах клеток-мишеней и связаны с тирозинкиназой. Фосфорилирование внутриклеточных киназ изменяет их энзимную активность, приводя к последовательным фосфорилирующим и дефосфорилирующим этапам во внутриклеточной сигнальной цепи. Стимуляция инсулиновых рецепторов ведет к транслокации транспортеров глюкозы из мест эндосомального хранения к мембране клетки и к увеличению поглощения глюкозы. Упорядочивание транспортеров глюкозы в тканях-мишенях важно для панкреатических (3-клеток, регулирующих выработку инсулина для глюкозо-чувствительных механизмов.

Высвобождение инсулина происходит в ответ на такие стимулы, как глюкоза, аминокислоты, гормоны, вырабатываемые в желудочно-кишечном тракте. Эти стимулы ведут к деполяризации (3-клеток в панкреатических островках Лангерганса и Са2+-опосредованному экзоцитозу инсулина в воротную вену. Потенциал мембраны (3-клеток регулируется АТФ-чувствительными калиевыми каналами (Iк(атф)), являющимися мишенью для сульфонамидных гипогликемических средств. Максимально высокая концентрация инсулина — в печени, перед попаданием в системный кровоток.
Инсулин оказывает различные эффекты на энергетический метаболизм, а общий эффект координирует распределение глюкозы, синтез и накопление гликогена и белков. Различные эффекты на метаболизм обусловлены концентрацией.
Подавление формирования кетоновых тел в печени происходит при более низких концентрациях инсулина, чем стимуляция поглощения глюкозы в скелетных мышцах.
Система гормонов поджелудочной железы, гипофиза и надпочечников защищает от гипогликемии. При голодании по мере уменьшения концентрации глюкозы в крови происходит подавление высвобождения инсулина. Если концентрация глюкозы в плазме падает ниже критического уровня, начинаются множественные нейрогормональные изменения:
• высвобождение поджелудочного глюкагона;
• активация симпатической нервной системы;
• гипоталамо-гипофизарно-надпочечниковое высвобождение гормона роста, кортизола и эпинефрина.
Эти регуляторные процессы увеличивают гликогенолиз и подавляют высвобождение инсулина. Симптомы гипогликемии (нервозность, тахикардия, дрожь, потоотделение) появляются в результате активности симпатической нервной системы. Отсутствие регулирования, как это наблюдается при избытке инсулина и пангипопитуитаризме, приводит к недостаточному уровню глюкозы в головном мозге, что ведет к коме. Соматостатин, синтезируемый в панкреатических 8-клетках, подавляет высвобождение как инсулина, так и иных регулирующих гликемию гормонов.
– Также рекомендуем “Сахарный диабет. Гипергликемия”
Оглавление темы “Терапия нарушений углеводного и липидного обменов”:
1. Нарушения углеводного обмена. Система гормонов поджелудочной железы, гипофиза и надпочечников
2. Сахарный диабет. Гипергликемия
3. Резистентность к инсулину. Инсулин при сахарном диабете
4. Инсулин длительного действия (ультраленте). Инсулины лизпро и аспарт
5. Инсулинотерапия диабета I типа. Пероральные гипогликемические средства
6. Репаглинид и метформин. Тиазолидиндионы
7. Терапия диабета II типа. Осложнения со стороны органов мишений при диабете
8. Гипогликемия. Нарушения липидного обмена
9. Гиперлипидемия и гиполипидемические средства. Ингибиторы ГМГ-КоА-редуктазы – статины
10. Секвестранты желчных кислот – холестирамин, колестипол, колесевелам. Производные фиброевой кислоты – фибраты
Источник
