Омела при раке поджелудочной железы
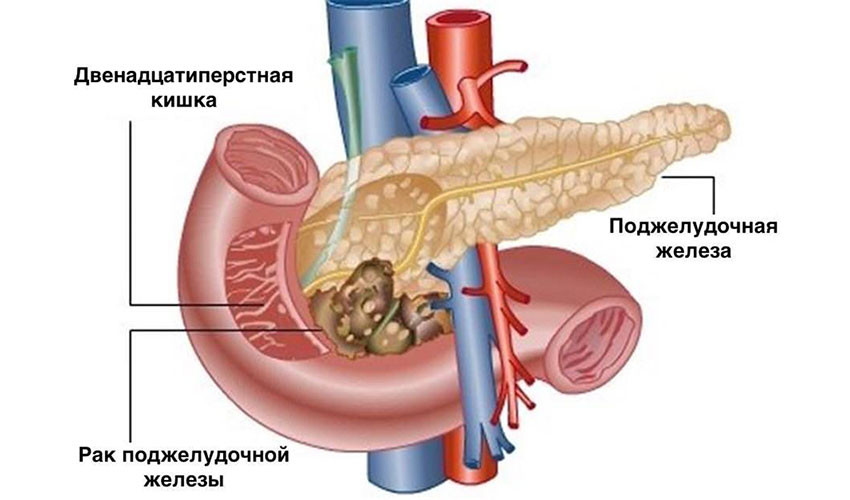
Friedmann Schad, Jan Axtner, Dirk Buchwald, Antje Happe, Stephan Popp, Matthias Kroez и Harald Mattes; IntergrCancer Ther опубликовано онлайн 19 декабря 2013 г.
Реферат
Рак поджелудочной железы остается одной из основных причин случаев смерти, связанных с раковыми заболеваниями. Внутриопухолевое применение противораковых агентов обсуждается как перспективный метод лечения твердых опухолей, таких как рак поджелудочной железы. Эндоскопическое применение ультразвука дает хорошую возможность для обследования и лечения поджелудочной железы. Европейская омела (Viscum album L.) является фитотерапевтическим средством, часто применяемым в Центральной Европе в области комплексной онкологии. Ее применение в качестве дополнительного средства имеет целью индуцировать иммуностимуляцию и противоопухолевые эффекты, а также облегчить побочные эффекты химиотерапии.
Внутриопухолевое применение омелы вызывало локальную реакцию опухоли при различных видах рака. Такое нестандартное применение требует тщательной валидации в плане безопасности и полезности. Здесь мы сообщаем данные о 39 пациентах с прогрессирующим неоперабельным раком поджелудочной железы, которые получили в общей сложности 223 внутриопухолевые дозы препарата омелы, либо с помощью эндоскопической ультрасонографии, либо в условиях трансабдоминального ультразвукового контроля. О каких-либо тяжелых побочных эффектах, связанных с этой процедурой, не сообщается. Неблагоприятные реакции на лекарство представляли собой главным образом повышение температуры или жар в 11 % и 14 % случаев его применения, соответственно. Другие неблагоприятные реакции на лекарство, такие как боль или тошнота, имели место в менее чем 7% случаев применения.
Тяжелых неблагоприятных реакций на лекарство зарегистрировано не было. Пациенты получали стандартную химиотерапию первого и второго уровня, подвергались адекватным паллиативным хирургическим вмешательствам, а также получали дополнительно препараты омелы: подкожно и отчасти внутривенно. Средний период выживания для всех пациентов составил 11 месяцев: 11.8 и 8.3 месяца для стадий II и IV, соответственно. Из-за многомодальности терапевтического подхода и отсутствия контрольной группы эффект от внутриопухолевого применения препарата омелы остается неясным. Ретроспективный анализ дает основания полагать, что внутривенное применение омелы может способствовать продлению периода выживания пациентов, страдающих раком поджелудочной железы. В заключение следует сказать, что это применение является легко осуществимым и безопасным, а его эффективность должна быть оценена путем проведения рандомизированного контролируемого испытания.
Ключевые слова: Рак поджелудочной железы, внутриопухолевый, терапия омелой, Viscum album, эндоскопическая ультрасонография.
Введение
Аденокарцинома протоков поджелудочной железы имеет не благоприятний прогноз. Хотя по частоте случаев рака он занимает 10-е место, по частоте смертельных случаев по причине рака в Германии и США он находится где-то на 4-6 местах 1,2. Из-за отсутствия симптомов он остается не обнаруженным, и более 80 % пациентов при постановке диагноза показывают наличие неоперабельной опухоли или распространение метастаз 1. Единственным способом лечения, который потенциально может привести к выздоровлению, является резекция, однако даже у тех пациентов, у которых она возможна, 5-летний период выживания встречается у менее чем 20 % пациентов – по данным, полученным в многоцентровых исследованиях, и у менее чем 5 % – в когортах пациентов, находящихся под наблюдением 3. Общий процент выживания у пациентов всех стадий составляет менее 2 % по истечении 5 лет 3,4.
Для неоперабельных опухолей в 1997 году стандартом стало применение монотерапии гемцитабином, поскольку он показал себя лучше 5-фторурацила по показателям клинической пользы, а также по общему медианному периоду выживания и проценту 1-годичного выживания 5.Тестированию подвергались многие комбинации гемцитабина с другими терапевтическими агентами, однако никакого существенного увеличения общего периода выживания по сравнению с монотерапией гемцитабином достигнуто не было 6. Недавние исследования, где применялся гемцитабин в сочетании с эрлотинибом – ингибитором рецептора фактора роста эпидермы 7, или ФОЛФИРИНОКСОМ 8, показали значительное увеличение медианного периода выживания, доли пациентов, реагирующих на лечение, а также периода без прогрессирования заболевания, по сравнению с монотерапией гемцитабином. Успех гемцитабина и эрлотиниба все еще тщательно оценивается экспертными комиссиями 9, а роль этого сочетания в случаях применения для пациентов с метастатическим раком поджелудочной железы подвергается сомнению в международных директивах 10. Хотя имеет место повышение токсичности с неблагоприятными реакциями на лекарство степени 3/4, ФОЛФИРИНОКС был принят в качестве лечебного средства первого уровня для пациентов с хорошими показателями моложе 75 лет 11,12.
Аденокарцинома протоков поджелудочной железы показывает раннее локальное распространение за пределы анатомических размеров органа, а также лимфогенные и нейрогенные местастазы 3. Среди клеток редкие опухолевые фибробласты (звездчатые клетки) имеют преимущественно стромальный тип 3, и образуют плотную стромальную ткань из-за сильной десмопластической реакции 14. Эта строма представляет собой участок ткани, который участвует в формировании рака, образовании опухоли, ее прогрессировании, инвазии и метастазе. Возникающая слабая вакуолизация может являться одной из причин того, что системные виды терапии дают ограниченный эффект 15. Вследствие этого давно высказывались предположения, что внутриопухолевое введение химиотерапевтических агентов могло бы стать перспективным методом для лечения прогрессирующего рака поджелудочной железы 16. Теоретической целью было достижение высоких локальных концентраций терапевтических агентов при сведении к минимуму системных побочных эффектов17.
Осуществимость локального применения различных агентов была доказана в моделях на мышах18. Реакция опухоли описывалась после внутриопухолевой химиотерапии18. При внутриопухолевом введении меченых антител наблюдались лучшие результаты в достижении клетки-мишени 20,21, а после применения к генетически трансформированным линиям раковых клеток были продемонстрированы противоопухолевые эффекты или более высокая чувствительность к химиотерапии 22-26. Наблюдались также иммунизация после вакцинации дендритными клетками, содержащими опухолевую РНК 27, 28, а также увеличение периода выживания после вакцинации с химиотерапией 29. Кроме этого, были проведены успешные исследования на животных (морских свинках), в которых химиотерапевтические агенты вводились внутриопухолево с помощью эндоскопической ультрасонографии 30,31.
С 2000 года предпринимались попытки применения эндоскопической ультрасонографии для выполнения тонкоигольных инъекций биологических противоопухолевых агентов человеку 32. В нескольких клинических исследованиях в фазах I и II тестировалось внутриопухолевое применение противораковых агентов для пациентов с прогрессирующей карциномой поджелудочной железы с использованием эндоскопической ультрасонографии для чрескожного трансабдоминального или чресжелудочного доступа, и были показаны осуществимость таких процедур и приемлемый профиль их безопасности 16,17,33-37.
В исследовании, выполненном Matthes et al.,в котором 14 пациентов, страдающих раком поджелудочной железы, получали внутриопухолевую терапию омелой, была продемонстрирована клиническая польза, выражавшаяся в регрессии опухоли (57 %), стабилизации болезни (36 %) и проценте выживания за 1-годичный период (36 %), при общей хорошей переносимости лечения 38. В качестве следующего шага в этом ретроспективном исследовании мы проанализировали данные по всем пациентам с неоперабельной или метастазирующей карциномой поджелудочной железы, проходившим лечение в больнице Havelhoehe в Берлине (Германия), или находящимся под наблюдением в амбулаторном лечебном центре, которые получали лечение препаратом омелы при внутриопухолевом введении. Мы документально регистрировали все виды применявшейся терапии и анализировали выживаемость пациентов. Целью этого исследования была оценка эффекта терапии омелой при внутриопухолевом введении и наблюдение за возможными неблагоприятными реакциями на лекарство.
Методы омелотерапиии
С 2004 по 2011 годы данные по наблюдению за всеми пациентами отделения гастроэнтерологии больницы Havelhoehe (Берлин, Германия), которым был поставлен диагноз карцинома поджелудочной железы, и которые дали согласие на проведение внутриопухолевой терапии омелой, регистрировались в Network Oncology 39. Все связанные с опухолями данные в отношении диагностики и лечения регистрировались с особым акцентированием применения экстрактов омелы. Указывались также традиционные виды терапии, а также любые неблагоприятные явления, документально отраженные в историях болезни пациентов.
Внутриопухолевое введение препаратов омелы выполнялось либо трансабдоминально, либо чресжелудочно/трансдуоденально с применением тонкоигольной техники, направляемой с помощью эндоскопической ультрасонографии. В то время как пациент находился под седативным действием пропофола, опухоль визуализировалась сонографически, и вблизи дальней границы опухоли помещалась игла Chiba (20 G). Препарат омелы вводился фракциями, передвигая иглу к ближней границе опухоли; когда игла вынималась, то вводился 0.9 % NaCl – во избежание обратного истечения препарата омелы из пункционного канала, чтобы уменьшить раздражение брюшины. Каждый раз опухоль подвергалась инъекциям 1-3 раза. По возможности в начале терапии применялась фаза индукции, состоящая из трех инъекций с увеличивающимися дозировками, начиная с 20 мг для препарата Abnoba и 50-100 мг для препарата Helixor.
Каждые 2-3 дня, в зависимости от состояния пациента, находящегося в стационаре, дозировка препарата омелы повышалась. Повышение дозировок составляло 20-40 мг (Abnoba) или 100-200 мг (Helixor) – вплоть до максимальной дозировки примерно 160 мг (Abnoba) или 1400 мг (Helixor). В зависимости от схемы химиотерапии, все дальнейшие инъекции омелы вводились вперемежку с химиотерапией, с интервалами в 4 недели или более, в соответствии с директивами S3 – применение седативных средств в желудочно-кишечной эндоскопии 41. Во время этой процедуры проводилось наблюдение за кровяным давлением, частотой пульса и насыщением кислородом, а также накладывалась рутинная кислородная носовая маска при скорости течения кислорода1.5-3.1 л/мин. После процедуры за пациентом велось наблюдение в течение как минимум 2 часов. Если требовалось, до или после процедуры пациентам давали обезболивающие (пиритрамид3.25 – 7.5 мг) или противорвотные (например метоклопрамид 10-20 мг).
Последующие анализы и графики выполнялись в R (версия 2.14.1, R Development Core team, 2011). Процент неблагоприятных явлений вычислялся как число таких событий, деленное на общее число инъекций препарата. Мы вычисляли оценки Каплана-Мейера для всей популяции пациентов и для подгрупп UICC на стадиях III и IV, используя функцию survfit, введенную в пакет выживаемости (версия 2.37-2); 95 %-ные доверительные интервалы (CI) вычислялись на логарифмической основе (выживаемость).
Таблица I Стадии UICC при первом диагнозе и оценки Каплана-Мейера а
Количество пациентов | Количество событий | Медианное значение (месяцы) | 95 %-ный доверительный интервал | ||
Нижний предел | Верхний предел | ||||
Всего | 39 | 34 | 11.0 | 7.8 | 16.1 |
UICC II | 3 | 3 | 63.1 | 15.6 | – |
UICC III | 10 | 8 | 11.8 | 8.2 | 22.8 |
UICC IV | 24 | 21 | 8.3 | 6.4 | 15.2 |
а Приводится количество пациентов, количество случаев смерти (событий), медианные значения общей выживаемости, а также нижний и верхний пределы доверительного интервала.
Результаты
Регистрировались данные для 39 пациентов (17 женщин и 22 мужчины), которые получали внутриопухолевую терапию омелой в период с 2004 по 2011 годы. Медианный возраст при первом диагнозе составил 61 год (у женщин 64 года, у мужчин 61 год). Минимальный возраст был 39 лет, а максимальный – 85 лет. В Таблице 1 приводятся документально зарегистрированные стадии UICC пациентов при первом диагнозе.
Традиционные виды терапии
Трое из пациентов на стадии UICC II в качестве первичной резекции опухоли были подвергнуты панкреатодуоденэктомии с сохранением пилоруса. Впервые внутриопухолевое введение экстрактов омелы было выполнено у этих пациентов после того, как у них появился неоперабельный рецидив. Прочие хирургические вмешательства, выполнявшиеся в 13 случаях, представляли собой различные виды лапаротомии в диагностических или исследовательских целях. Четырнадцать пациентов были снабжены системой входа, а одному пациенту был имплантирован шунт Денвера. Девять пациентов подвергались паллиативной хирургии следующих видов: чрескожная эндоскопическая гастростомическая трубка, чрескожная эндоскопическая гастростомическая трубка и гастростомия, билиодигестивный анастомоз, задняя гастроэнтеростомия удалением нервного узла, продольная лапаротомия срединной артерии и двухсторонняя аднексэктомия, частичная резекция подвздошной кишки с илеоилеостомией, асцендо-трансверсостомия, и илеоцекальная резекция 1 м подвздошной кишки.
Два пациента получали радиационную терапию из-за костных метастаз. В общей сложности, 33 пациента получали химиотерапию первого уровня; 10 получали второй уровень, а один – третий уровень. Тридцать пациентов получали монотерапию гемцитабином; 11 имели комбинированный лечебный режим, включавший 2 и более химиотерапевтических средств (Таблица 2).
Терапия омелой
Тридцать один пациент получал лечение препаратом омелы Helixor, 30 – препаратом Abnoba VISCUM, 9 – препаратом Iscador и 2 – препаратом Iscucin. Внутриопухолевое введение препарата Helixor выполнялось 26 пациентам, Abnoba VISCUM – 18 пациентам, а Iscucin – одному. В общей сложности было выполнено 223 внутриопухолевые инъекции, среди которых в 139 случаях вводился Helixor, в 89 случаях – Abnoba VISCUM, и в 3 – Iscucin (Таблица 3). Двадцати пациентам вводился внутриопухолево исключительно Helixor Mali, в то время как 13 пациентов получали исключительно Abnoba VISCUM. В дополнение к внутривоопухолевой терапии, 32 пациента получали подкожные, а 21 пациент – внутривенные сопроводительные инъекции омелы.
Безопасность и осложнения, имевшие место во время внутриопухолевого применения омелы
Наиболее часто наблюдавшимся побочным явлением была повышенная температура тела (≤ 38 °С). У 23 пациентов наблюдались неблагоприятные реакции на лекарство, включая жар (> 38 °С), боли, тошнота, общее раздражение кожи, изменения в числе кровяных клеток, проблемы с кровообращением и головные боли (Таблица 4). Во время выполнения 223 инъекций были описаны 6 случаев осложений, связанных с процедурой, и 2 случая ошибки при выполнении процедуры. Связанные с процедурой осложнения представляли собой «плохая видимость», «воздух в брюшной полости» или «кишка на линии пункции». Ошибками при выполнении были: 1 инъекция в перитуморальный венозный конгломерат и 1 – в стенку двенадцатиперстной кишки. В обоих случаях произошло спонтанное заживление, без каких-либо дальнейших клинических последствий. Данные о применении обезболивающих средств при первом диагнозе имелись только для 23 пациентов при поступлении в стационар.
Стадии UICC и выживаемость
Медианный период выживания вычислялся для всех пациентов, а также в зависимости от стадии UICC (Таблица 1). Медианный период выживания для всех пациентов составил 11 месяцев (95 % CI: 7.8; 16.1). На Рисунке 1А показаны периоды выживания для пациентов на всех стадиях, а на Рисунке 1В показаны периоды выживания пациентов для стадий UICC III и IV. Медианные периоды выживания пациентов на стадиях III и IV составили 11.8 месяцев (95 % CI:8.2, 22.8) и 8.3 месяца (95 % CI: 6.4, 15.2), соответственно, однако они не были значимо различными (логарифмический ранговый критерий, χ2 = 0.8, df = 1, P=.379). Одногодичного периода выживания достигали 42 % всех пациентов, или 27 % и 33 % пациентов на стадиях UICC III и IV, соответственно.
Обсуждение
В этом ретроспективном исследовании мы представляем данные о 39 пациентах с прогрессирующей, не подлежащей резекции карциномой поджелудочной железы, которые получали внутриопухолевые препаратов омелы. Кроме этого, пациенты получали системную терапию омелой и стандартную химиотерапию.
Таблица 2. Частота и количество циклов химиотерапии
Химиотерапевтический агент | +Фолиновая кислота | Абсолютная частота | Количество пациентов | Количество циклов | ||||
Медиана | Среднее | SD | Мин | Макс | ||||
Гемцитабин | 323 | 30 | 10.8 | 8.5 | 11.4 | 1 | 51 | |
5-Фторурацил | 19 | 20 | 6 | 1.5 | 3.3 | 3.6 | 1 | 10 |
Эрлотиниб | 1 | 1 | 1 | |||||
Оксалиплатин | 1 | 3 | 2 | 1.5 | 1.5 | 0.7 | 1 | 2 |
Митоксантрон | 1 | 1 | 1 | |||||
Гемцитабин+ эрлотиниб | 23 | 3 | 6 | 7.7 | 4.7 | 4 | 13 | |
Гемцитабин+ оксалиплатин | 1 | 1 | 1 | |||||
Гемцитабин+цисплатин | 4 | 1 | 4 | |||||
5-Фторурацил+ оксалиплатин | 21 | 21 | 6 | 2 | 3.5 | 4.3 | 1 | 12 |
Паклитаксел+ цисплатин | 1 | 1 | 1 | |||||
Гемцитабин+5-фторурацил+ цисплатин | 1 | 1 | 1 | |||||
Источник
1 октября 2019 г.
Просмотров: 7812
Рак поджелудочной железы относится к онкологическим заболеваниям, с которыми сложно бороться, и которые характеризуются относительно низкой выживаемостью. В течение 5 лет с момента установления диагноза в живых остаются лишь 9% больных. Рак поджелудочной железы нередко диагностируют в запущенной стадии, потому что не существует эффективного рекомендованного скрининга, злокачественная опухоль может долго не вызывать симптомов.
Тем не менее, пациенту можно помочь, даже если заболевание диагностировано на поздней стадии. В случаях, когда невозможно добиться ремиссии, врачи могут продлить жизнь пациента и избавить его от мучительных симптомов. Эффективное лечение можно получить в клинике Медицина 24/7.

Хирургическое лечение
Хирургическое удаление опухоли — самый эффективный метод лечения рака поджелудочной железы. Это единственная реальная возможность достичь ремиссии. К сожалению, на момент постановки диагноза только у одного из пяти пациентов опухоль не успела распространиться за пределы поджелудочной железы, и лишь у некоторых из них рак можно полностью удалить. Обычно это узлы в головке органа: через неё проходит желчный проток, при его сдавлении развивается механическая желтуха, и эта симптоматика помогает рано диагностировать опухоль.
Операцию проводят, если хирург уверен, что он сможет удалить рак полностью. Циторедуктивные вмешательства, направленные на частичное удаление как можно большего количества опухолевой ткани, не проводятся, так как нет доказательств того, что они помогают продлевать жизнь пациентов.
При раке головки поджелудочной железы чаще всего выполняют операцию Уиппла. Во время нее удаляют головку органа, иногда вместе с телом, и часть окружающих органов: тонкой кишки, желчного протока, ближайшие лимфатические узлы, желчный пузырь, иногда часть желудка.
Операция Уиппла — сложное вмешательство, оно сопровождается риском тяжелых осложнений. Восстановительный период может продолжаться от нескольких недель до нескольких месяцев. Иногда противопоказанием к такой операции становится плохое общее здоровье пациента. Статистика показывает, что смертность от осложнений операции Уиппла в неспециализированных клиниках составляет около 15%, а в специализированных медицинских центрах — 5%.
При резектабельном раке хвоста поджелудочной железы проводят дистальную панкреатэктомию: удаляют хвост поджелудочной железы, иногда вместе с телом, и селезенку.
В редких случаях встречаются ситуации, когда злокачественная опухоль распространилась по всей поджелудочной железе, но все еще является операбельной. При этом может быть выполнена тотальная панкреатэктомия: поджелудочную железу удаляют полностью, вместе с ней — желчный пузырь, часть желудка и тонкой кишки.

Паллиативные операции
Во время паллиативных операций не удаляют рак, их цель — избавить больного от симптомов, вызванных злокачественной опухолью. При раке головки поджелудочной железы нередко развивается механическая желтуха — состояние, вызванное сдавлением желчного протока и нарушением оттока желчи. У больного окрашиваются в желтый цвет кожа, слизистые оболочки и белки глаз, беспокоит кожный зуд, ухудшается общее состояние, прогноз.
С этим осложнением можно справиться тремя способами:
- Дренирование. Во время эндоскопической ретроградной холангиопанкреатографии (РХПГ) или чрескожной чреспеченочной холангиографии в желчные протоки устанавливают дренажную трубку. По ней желчь может оттекать наружу, в просвет двенадцатиперстной кишки или сразу в обоих направлениях. Это достаточно эффективно, но не очень удобно: дренажная трубка постоянно мешается, может случайно сместиться, выпасть.
- Стентирование — более современное решение. Эндоскопически, с помощью катетера, заведенного в желчные протоки из двенадцатиперстной кишки, в заблокированном участке устанавливают стент — трубку с сетчатой стенкой из полимера или металла. Он расширяет просвет протока и обеспечивает свободный отток желчи. Стентирование — быстрая и относительно безопасная процедура, ее выполняют без разрезов.
- Шунтирование — операция, во время которой хирург создает обходной путь для оттока желчи. По сравнению со стентированием, хирургическое вмешательство несет более высокий риск осложнений, его могут перенести не все больные. Но иногда оно позволяет более эффективно, надолго восстановить отток желчи. Во время операции можно перерезать нервы, из-за которых беспокоят мучительные боли.
Насколько эффективна химиотерапия при раке поджелудочной железы?
Химиопрепараты довольно часто применяют при злокачественных опухолях поджелудочной железы. Они могут быть назначены с разными целями:
- Адъювантная химиотерапия проводится до операции, чтобы уменьшить объем опухоли.
- Неоадъювантная химиотерапия проводится после операции, чтобы снизить риск рецидива.
- Химиотерапия как основной метод лечения применяется при неоперабельных опухолях. Цель лечения в таком случае — не достичь ремиссии, а как можно дольше держать болезнь под контролем.
Чаще всего применяют такие химиопрепараты, как гемцитабин (Гемзар),оксалиплатин (Элоксатин),иринотекан (Камптозар),5-фторурацил, цисплатин, капецитабин (Кселода). Обычно назначают комбинации из двух препаратов с разными механизмами действия, это помогает повысить эффективность лечения. Ослабленным пациентам назначают только один препарат из-за риска серьезных побочных эффектов.
Эффективность лучевой терапии
Лучевую терапию при раке поджелудочной железы зачастую применяют вместе с химиопрепаратами. Такое лечение называется химиолучевой терапией. Ее назначают после операции, при неоперабельном раке.
Если опухоль находится в пограничном состоянии между резектабельной и нерезектабельной, после курса неоадъювантной лучевой терапии ее размеры могут уменьшиться так, что ее получится удалить хирургическим путем.
Также лучевую терапию при раке поджелудочной железы применяют в качестве симптоматического лечения, например, если беспокоят мучительные боли, и пациенту противопоказано хирургическое вмешательство.
Таргетная терапия
Принципиальное отличие таргетных препаратов от традиционных химиопрепаратов в том, что они не атакуют все подряд быстро размножающиеся клетки, а действуют более целенаправленно. Каждый таргетный препарат имеет определенную молекулу-мишень, которая помогает раковым клеткам быстро размножаться, сохранять жизнеспособность, «маскироваться» от иммунной системы. Благодаря этим особенностям, таргетная терапия может быть эффективна, когда химиопрепараты не помогают, и вызывает менее серьезные побочные эффекты.
На поверхности раковых клеток в поджелудочной железе нередко увеличено количество молекул белка-рецептора EGFR. Активируясь, он заставляет клетки быстро размножаться. Его можно заблокировать с помощью таргетного препарата эрлотиниб (Тарцева). Его часто назначают в сочетании с химиопрепаратом гемцитабином. Эффективность этой комбинации различается у разных онкологических больных.
Помогает ли иммунотерапия при раке поджелудочной железы?
Иммунная система человека должна не только атаковать чужеродные агенты, но и знать, когда пора остановиться, чтобы не навредить собственным тканям организма. Для этого в ней есть специальные сигнальные молекулы, подавляющие активность иммунных клеток. При раке эти молекулы начинают мешать. Они не дают иммунитету эффективно распознавать и уничтожать опухолевые клетки. Существуют препараты, которые могут заблокировать эти молекулы, они называются ингибиторами контрольных точек.
При раке поджелудочной железы ингибиторы контрольных точек могут быть полезны для пациентов, у которых выявлены определенные генетические отклонения: высокий уровень микросателлитной нестабильности, мутации в генах восстановления несоответствия (MMR).
В клинике Медицина 24/7 при многих типах рака можно пройти молекулярно-генетическое исследование, которое помогает выявить мишени для лекарственных препаратов, имеющиеся в раковых клетках пациента, и назначить оптимальную, персонализированную терапию.
Иммунотерапия при раке поджелудочной железе может помочь в следующих случаях:
- Рост опухоли на фоне химиотерапии.
- Неоперабельный рак.
- Рецидив после проведенного лечения.
- Рак поджелудочной железы с метастазами.
В мировой онкологической практике применяют иммунопрепарат пембролизумаб (Кейтруда). Он блокирует белок PD-1, который находится на поверхности T-клеток. Лекарство вводят внутривенно через каждые 2–3 недели.
Обычно эффективное лечение при раке поджелудочной железы подбирает консилиум врачей, в зависимости от типа, стадии опухоли, общего состояния здоровья пациента и других факторов. Даже если рак неоперабелен, и ремиссии достичь не удастся, пациенту все еще можно помочь. В клинике Медицина 24/7 доступны наиболее современные виды лечения. Запишитесь на консультацию к нашему специалисту.
Материал подготовлен врачом-онкологом, хирургом клиники «Медицина 24/7» Рябовым Константином Юрьевичем.
Источник
