Гормон поджелудочной железы соматостатин усиливает
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 1 ноября 2018;
проверки требуют 2 правки.
Соматостати́н — гормон дельта-клеток островков Лангерганса поджелудочной железы, а также один из гормонов гипоталамуса. По химическому строению является пептидным гормоном.
Структура[править | править код]
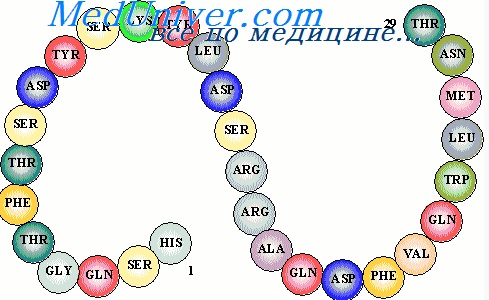
Соматостатин существует в двух биологически активных формах, происходящих от одного предшественника и различающихся длиной N-конца: SST-14 (14 аминокислот: AGCKNFFWKTFTSC, между остатками цистеина дисульфидная связь) и SST-28 (28 аминокислот). Помимо соматостатинов, близкородственные пептиды кортистатин (PCKNFFWKTFSSCK), триттен (13 N-конечных аминокислот SST-28) и уротензин II (ETPDCFWKYCV) также принимают участие в регуляции соматостатинэргической системы[1].
Функция[править | править код]
Соматостатин подавляет секрецию гипоталамусом соматотропин-рилизинг-гормона и секрецию передней долей гипофиза соматотропного гормона и тиреотропного гормона.
Кроме того, он подавляет также секрецию различных гормонально активных пептидов и серотонина, продуцируемых в желудке, кишечнике, печени и поджелудочной железе. В частности, он понижает секрецию инсулина, глюкагона, гастрина, холецистокинина, вазоактивного интестинального пептида, инсулиноподобного фактора роста-1.
Функцию соматостатина опосредуют по меньшей мере 6 различных подтипов рецепторов (sst1, sst2A, sst2B, sst3, sst4, sst5), относящихся к семейству G-белок-сопряжённых рецепторов с 7 трансмембранными доменами. Эти рецепторы, за исключением sst2, кодируются разными генами, в то время как sst2A и sst2B являются сплайсинг-вариантами одного и того же гена. Соматостатиновые рецепторы подразделяются на две группы — SRIF1 (sst2, sst3, sst5) и SRIF2 (sst1, sst4) — на основании связывания с классическими октапептидными и гексапептидными аналогами соматостатина (октреотид, лантреотид, сеглитид, вапреотид): с ними легко связываются SRIF1-, но не SRIF2-рецепторы. Конкретные данные о функции тех или иных подтипов соматостатиновых рецепторов весьма противоречивы[1].
Терапевтический потенциал[править | править код]
Наиболее распространено фармакологическое воздействие на соматостатинэргическую систему в связи с ингибированием выброса гормона роста, что делает данную систему весьма перспективной при лечении опухолевых заболеваний и акромегалии[2]. Вещества, усиливающие выброс соматостатина, могут проявлять свойства когнитивных стимуляторов[3].
Коммерческие препараты[править | править код]
Наиболее распространён и известен Октреотид (и его дженерики) — синтетическое производное гормона соматостатина, обладающее сходными с ним фармакологическими эффектами и значительно бо́льшей продолжительностью действия. Подавляет патологически повышенную секрецию гормона роста, пептидных гормонов и серотонина, продуцируемых в гастроэнтеропанкреатической эндокринной системе. Введение октреотида не сопровождается феноменом гиперсекреции гормонов по механизму «отрицательной обратной связи».[4]
В РФ соматостатин производится в форме раствора для инъекций 0,01 % и 0,005 %, а также в форме лиофилизата для приготовления суспензии для внутримышечного введения пролонгированного действия (Октреотид-депо).
Примечания[править | править код]
- ↑ 1 2 Olias G. et al. Regulation and function of somatostatin receptors. // J. Neurochem. 2004. v. 89. pp. 1057—191.
- ↑ Prasad V., Fetscher S., Baum R.P. Changing role of somatostatin receptor targeted drugs in NET: Nuclear Medicine’s view. // J. Pharm. Pharmaceut. Sci. 2007. 321s-327s.
- ↑ Tokita K. et al. FK962, a novel enhancer of somatostatin release, exerts cognitive-enhancing actions in rats. // Eur. J. Pharm. 2005. v. 527. pp. 111—120.
- ↑ https://www.webapteka.ru/drugbase/name13699.html=Октреотид (недоступная ссылка): Описание препарата.
Источник
В организме человека соматостатин находится в двух формах – с 14 и 28 аминокислотами в составе. Первая обнаруживается преимущественно в головном мозге и образуется гипоталамусом, а вторая в поджелудочной железе и стенке кишечника. В головном мозге соматостатина находится всего 25% от всего количества, а основная масса работает в пищеварительной системе. Рецепторы к этому гормону широко распространены во внутренних органах, мозговой ткани.
Начало синтеза соматостатина приходится на третий месяц внутриутробного развития. В это время его основная роль – это регуляция образования гормона роста. Чем больше образуется ростовых факторов (соматотропин, инсулиноподобный фактор роста), тем больше синтезируется гипоталамусом соматостатина. Он подавляет выделение соматотропного рилизинг-фактора и останавливает в гипофизе выведение, но не образование гормона роста.
При нарушении выработки этого гормона развивается гигантизм и акромегалия. Рецепторы к гормону перестают образовываться при болезни Альцгеймера.
Основные функции соматостатина:
- регуляция выделения гормона роста, подавляет образование дофамина;
- тормозит продукцию норадреналина, гипоталамических гормонов-стимуляторов активности щитовидной железы, надпочечников (тиролиберина и кортиколиберина);
- напрямую изменяет синтез тиреотропных гормонов, альдостерона, адреналина и норадреналина надпочечников;
- препятствует образованию ренина почками;
- снижает поступление в кровь инсулина, глюкагона, участвующих в обмене глюкозы;
- угнетает продукцию пепсина, соляной кислоты, секретина, гастрина, препятствует сокращениям желудка, желчного пузыря, кишечника, замедляет процессы пищеварения и продвижения пищи по желудочно-кишечному тракту;
- замедляет деление клеток иммунной системы, костей, хрящей, сужает кровеносные сосуды в этих тканях;
- уменьшает показатели артериального давления, частоту пульса;
- регулирует ритм дыхания, влияет на его остановку при тяжелой патологии.
В норме с мочой выделяется за час 120-200 пг соматостатина. При опухоли гипофиза (соматостатиноме) этот показатель возрастает примерно в 40 раз. Повышенный уровень гормона сопровождается такими проявлениями:
- образование камней в желчном пузыре из-за снижения его сократимости;
- сахарный диабет;
- поносы с потерей жиров;
- боли в животе;
- потеря веса;
- снижение эритроцитов и гемоглобина;
- пониженная кислотность желудочного сока.
У медикаментов, которые синтезированы по подобию соматостатина, имеются все его основные свойства, а также большая продолжительность нахождения в крови, чем у природного гормона. Существует ряд препаратов, в которых немного изменена последовательность аминокислот:
- октреотид – Октра, Сандостатин, Октрестатин;
- лантреотид – Соматулин;
- пасиреотид – Сигнифор.
С ними подавляется секреция:
- гормона роста;
- инсулина, глюкагона и пищеварительных ферментов, выделяемых под влиянием приема пищи;
- тиреотропного гормона гипофиза.
Показания к применению препаратов:
- после операций на поджелудочной железе для уменьшения риска абсцессов, нагноения, острого панкреатита;
- акромегалия;
- аденома гипофиза, вырабатывающая гормон роста;
- опухоли органов пищеварения, способные вырабатывать гормоны;
- гастринома (опухоль в желудке);
- инсулинома (опухолевое разрастание клеток поджелудочной железы);
- диарея при ВИЧ-инфекции;
- кровотечение из варикозно измененных вен пищевода при циррозе печени.
Противопоказания: индивидуальная непереносимость. При беременности назначение возможно по жизненным показаниям. На период применения кормящими матерями необходимо перевести ребенка на искусственные смеси.
Следует учитывать, что при акромегалии соматостатин может восстановить способность к зачатию у женщин, поэтому на протяжении всего курса нужно использовать контрацептивы.
Читайте подробнее в нашей статье о гормоне соматостатине.
Структура и образование
В организме человека соматостатин находится в двух формах – с 14 и 28 аминокислотами в составе. Первая обнаруживается преимущественно в головном мозге и образуется гипоталамусом, а вторая в поджелудочной железе и стенке кишечника. В головном мозге соматостатина находится всего 25% от всего количества, а основная масса работает в пищеварительной системе. Рецепторы к этому гормону широко распространены во внутренних органах, мозговой ткани.
Начало синтеза соматостатина приходится на третий месяц внутриутробного развития. В это время его основная роль – это регуляция образования гормона роста. Чем больше образуется ростовых факторов (соматотропин, инсулиноподобный фактор роста), тем больше синтезируется гипоталамусом соматостатина. Он подавляет выделение соматотропного рилизинг-фактора и останавливает в гипофизе выведение, но не образование гормона роста.
При нарушении выработки этого гормона развивается гигантизм и акромегалия, которые сопровождаются чрезмерно высоким ростом. Высказано предположение, что соматостатин является причиной остановки дыхания во сне (апноэ сна) у пациентов с акромегалией и развития синдрома внезапной младенческой смерти. Рецепторы к гормону перестают образовываться при болезни Альцгеймера.
Рекомендуем прочитать статью о причинах и симптомах акромегалии. Из нее вы узнаете о причинах развития акромегалии, симптомах у женщин и мужчин, бывает ли у детей, а также о методах диагностики и лечения данного заболевания.
А здесь подробнее о причинах гигантизма.
Основные функции соматостатина
Помимо главной задачи – регуляции выделения гормона роста, соматостатин также обладает следующими свойствами:
- подавляет образование дофамина (отвечает за чувство удовлетворения);
- тормозит продукцию норадреналина, гипоталамических гормонов-стимуляторов активности щитовидной железы, надпочечников (тиролиберина и кортиколиберина);
- напрямую изменяет синтез тиреотропных гормонов, альдостерона, адреналина и норадреналина надпочечников;
- препятствует образованию ренина почками;
- снижает поступление в кровь инсулина, глюкагона, участвующих в обмене глюкозы;
- угнетает продукцию пепсина, соляной кислоты, секретина, гастрина, препятствует сокращениям желудка, желчного пузыря, кишечника, замедляет процессы пищеварения и продвижения пищи по желудочно-кишечному тракту;
- замедляет деление клеток иммунной системы, костей, хрящей, сужает кровеносные сосуды в этих тканях;
- уменьшает показатели артериального давления, частоту пульса;
- регулирует ритм дыхания, влияет на его остановку при тяжелой патологии.
К чему приводит избыток гормона поджелудочной железы
В норме с мочой выделяется за час 120-200 пг соматостатина. При опухоли гипофиза (соматостатиноме) этот показатель возрастает примерно в 40 раз. Повышенный уровень гормона сопровождается такими проявлениями:
- образование камней в желчном пузыре из-за снижения его сократимости;
- сахарный диабет (соматостатин препятствует выделению инсулина);
- поносы с потерей жиров (стеаторея) при снижении количества ферментов, переваривающих липиды в кишечнике, ухудшении процессов всасывания;
- боли в животе;
- потеря веса;
- снижение эритроцитов и гемоглобина;
- пониженная кислотность желудочного сока.
Свойства синтетического аналога
У медикаментов, которые синтезированы по подобию соматостатина имеются все его основные свойства, а также большая продолжительность нахождения в крови, чем у природного гормона. Существует ряд препаратов, в которых немного изменена последовательность аминокислот:
- октреотид – Октра, Сандостатин, Октрестатин;
- лантреотид – Соматулин;
- пасиреотид – Сигнифор.
На фоне лечения этими медикаментами подавляется секреция:
- гормона роста;
- инсулина, глюкагона и пищеварительных ферментов, выделяемых под влиянием приема пищи;
- тиреотропного гормона гипофиза.
В отличие от природного гормона синтетические в большей степени подавляют синтез инсулина и процесс переваривания пищи, не вызывают ответного возрастания образования гормона роста при акромегалии.
Показания к применению
Соматостатин назначается при таких заболеваниях:
- после операций на поджелудочной железе для уменьшения риска абсцессов, нагноения, острого панкреатита;
- акромегалия – снижает уровень соматотропина гипофиза и инсулиноподобного фактора (ИФР-1) наполовину у 90% пациентов, избавляет от утомляемости, потливости, головных и суставных болей. Рекомендуется при отказе от операции, при лучевой терапии, пока не начнется ее действие;
- аденома гипофиза, вырабатывающая гормон роста – сокращает размеры;
- опухоли органов пищеварения, способные вырабатывать гормоны – симптоматическое облегчение состояния. Уменьшается понос, приливы жара, восстанавливается баланс электролитов. У некоторых больных останавливается рост новообразования, метастазирование;
- гастринома (опухоль в желудке) – снижает образование соляной кислоты, прекращает понос;
- инсулинома (опухолевое разрастание клеток поджелудочной железы) – восстанавливает содержание глюкозы в крови;
- диарея при ВИЧ-инфекции – нормализация частоты стула;
- кровотечение из варикозно измененных вен пищевода при циррозе печени останавливает потерю крови, предупреждает рецидивы.
Противопоказания
При наличии заболеваний, которые подлежат лечению синтетическими аналогами соматостатина противопоказание может быть только индивидуальная непереносимость. При беременности назначение возможно по жизненным показаниям. На период применения кормящими матерями необходимо перевести ребенка на искусственные смеси.
Следует учитывать, что при акромегалии соматостатин может восстановить способность к зачатию у женщин, поэтому на протяжении всего курса нужно использовать контрацептивы.
Побочные действия
К самым частым последствиям применения препаратов, содержащих аналоги соматостатина, относятся:
- нарушения пищеварения – запор, понос, боль в животе, вздутие;
- образование камней в желчном пузыре;
- головная боль, головокружение;
- снижение образования гормонов щитовидной железы (гипотиреоз);
- рвота;
- падение содержания сахара в крови, нарушение толерантности к глюкозе;
- боль и жжение в месте введения, кожная сыпь;
- неритмичное дыхание;
- замедление сердечного ритма.
При наличии сахарного диабета важно чаще измерять содержание глюкозы в крови, так как возможно потребуется коррекция доз инсулина или антидиабетических таблеток.
Рекомендуем прочитать статью о гормонах долей гипофиза. Из нее вы узнаете об основных характеристиках гипофиза, физическом значении и функциях долей гипофиза.
А здесь подробнее о недостаточности гипофиза.
Соматостатин образуется гипоталамусе и поджелудочной железой. Обладает свойством подавлять выделение гормона роста гипофизом, при его недостатке развивается акромегалия. В пищеварительной системе снижает образование инсулина, глюкагона и пищеварительных ферментов. Эти свойства используются для лечения избыточного роста тела и при опухолях, которые обладают способностью к образованию инулина, гастрина, секретина.
Показан при кровотечении из вен пищевода, неукротимом поносе у больных СПИДом, аденоме гипофиза, вырабатывающей соматотропин.
Полезное видео
Смотрите на видео о гормоне роста (соматотропине):
Источник
Влияние соматостатина на секрецию поджелудочной железы. Регуляция уровня глюкозыДельта-клетки островков Лангерганса продуцируют гормон соматостатин — полипептид, состоящий из 14 аминокислот и имеющий чрезвычайно короткий период полувыведения, равный 3 мин. Почти все факторы, связанные с поступлением пищи, стимулируют продукцию соматостатина. К ним относят: (1) увеличение глюкозы в крови; (2) увеличение аминокислот; (3) увеличение жирных кислот; (4) увеличение концентрации различных гастроинтестинальных гормонов, высвобождающихся в верхних отделах желудочно-кишечного тракта в ответ на прием пищи. В целом соматостатин обладает многочисленными тормозными влияниями.
Суммируя эту информацию, можно предположить, что главной функцией соматостатина является продление времени поступления питательных веществ в кровоток. В то же время влияние соматостатина, подавляющее секрецию инсулина и глюкагона, снижает использование поступивших питательных веществ тканями, что предупреждает быстрое истощение источников питательных веществ и поэтому делает их доступными в течение более длительного периода. Необходимо повторить, что соматостатин является тем же веществом, что и рост-ингибирующий гормон, который продуцируется гипоталамусом и подавляет секрецию гормона роста передней долей гипофиза. В норме у человека концентрация глюкозы в крови поддерживается в узком диапазоне значений: между 80 и 90 мг/дл крови натощак (обычно утром перед завтраком). Концентрация глюкозы повышается до 120-140 мг/дл крови сразу после еды либо в течение первого часа после приема пищи, но система обратной связи быстро возвращает концентрацию глюкозы к исходному уровню обычно в течение 2 ч после всасывания углеводов. При голодании процессы глюконеогенеза в печени обеспечивают сохранение глюкозы в крови в пределах, характеризующих ее концентрацию в крови натощак. 1. Печень функционирует как важная буферная система, поддерживающая уровень глюкозы в крови. Если концентрация глюкозы в крови поднимается до высоких значений после приема пищи, то секреция инсулина возрастает настолько, что 2/3 всосавшейся глюкозы немедленно депонируется в печени в виде гликогена. Затем в течение последующих часов, когда снижаются и уровень глюкозы в крови, и продукция инсулина, печень начинает высвобождать глюкозу в кровоток. Таким способом печень снижает колебания концентрации глюкозы в крови приблизительно до 1/3 уровня флюктуации, который должен быть обнаружен при отсутствии этого механизма. Действительно, больные с тяжелыми заболеваниями печени не могут поддерживать узкий диапазон колебаний значений концентрации глюкозы в крови. 3. При выраженной гипогликемии непосредственное влияние низкого уровня глюкозы на гипоталамус стимулирует симпатическую нервную систему. В итоге из мозгового вещества надпочечников выделяется адреналин, обеспечивающий высвобождение глюкозы из печени, что препятствует возобновлению гипогликемии. – Также рекомендуем “Важность регуляции глюкозы. Сахарный диабет” Оглавление темы “Недостаток и избыток инсулина. Роль глюкагона”: |
Источник