Дуоденальная дистрофия поджелудочной железы
ГППЖ — главный проток поджелудочной железы
ДД — дуоденальная дистрофия
ДПК — двенадцатиперстная кишка
КТ — компьютерная томография
МРТ — магнитно-резонансная томография
ПДР — панкреатодуоденальная резекция
ПЖ — поджелудочная железа
УЗИ — ультразвуковое исследование
ХП — хронический панкреатит
ЭГДС — эзофагогастродуоденоскопия
ЭУС — эндоскопическая ультрасонография
АГА — антитела к глиадину
АГД — аглютеновая диета
АтТГ — антитела к тканевой трансглутаминазе
ДПК — двенадцатиперстная кишка
КВ — контрастное вещество
МСКТ — мультиспиральная компьютерная томография
МЭЛ — межэпителиальные лимфоциты
СОТК — слизистая оболочка тонкой кишки
ЭГДС — эзофагогастродуоденоскопия
Дуоденальная дистрофия (ДД) — патологическое изменение стенки двенадцатиперстной кишки (ДПК), вызванное хроническим воспалением эктопированной в нее ткани поджелудочной железы (ПЖ). Добавочная (аберрантная) ПЖ является наиболее частой аномалией этого органа. Аберрантная железа не имеет анатомической или сосудистой связи с основной. Наиболее часто наблюдается эктопия ПЖ в стенку желудка (25—60% случаев) и в стенку ДПК (25—35%) [1, 2]. Она может быть следствием метаплазии полипотентных эндодермальных клеток in situ либо перемещения эмбриональных панкреатических клеток в соседние структуры [3]. Описаны и другие локализации добавочной ПЖ: подвздошная кишка, дивертикул Меккеля, желчевыводящие пути, печень, селезенка, сальник, брыжейка, легкие, средостение, пищевод, толстая кишка, маточные трубы. Чаще эктопированная ткань располагается в подслизистой основе (75%), реже — в мышечном слое (15%) или субсерозно (10%) [4].
Впервые ДД описана в 1970 г. французскими авторами F. Potet и N. Duclert [5]. ДД представляет собой фиброзное утолщение стенки ДПК с образованием кист в ее мышечном слое и/или подслизистой основе [6]. Прогрессирование хронического панкреатита (ХП) в ортотопической ПЖ при наличии эктопированного очага в ДПК, как правило, сопровождается развитием Д.Д. Описана также другая последовательность событий, когда прогрессирование эктопического панкреатита в вертикальной части ДПК может приводить к сдавливанию главного протока ПЖ (ГППЖ) и развитию обструктивного панкреатита в ортотопической железе [7, 8]. В этом случае острый или ХП с преимущественным поражением головки или ПЖ на всем протяжении рассматривается как осложнение ДД [9].
Дифференциальная диагностика при данной патологии проводится с опухолями, ХП и врожденными аномалиями ПЖ. В зависимости от преобладания фиброзных или кистозных изменений выделяют кистозный и солидный варианты ДД, которые являются стадиями одного патологического процесса. Вариант определяется диаметром кист, выявляемых методами визуализации: при кистозной форме заболевания диаметр кист составляет более 1 см, при солидной — не превышает 1 см. Помимо этого выделяют смешанный вариант — сочетание мягкотканного компонента с кистами диаметром более 1 см [9]. Внутренняя поверхность кист, образующихся при ДД, лишена эпителиальной выстилки, а в их просвете в большинстве случаев содержится некротическая или геморрагическая жидкость, могут образовываться конкременты. В ДПК отмечается гипертрофия бруннеровых желез [10].
Основными клиническими проявлениями ДД служат боль в эпигастральной области, снижение массы тела и желтуха. Эти признаки неспецифичны и могут указывать на другие заболевания панкреатодуоденального отдела, в том числе ХП, рак ПЖ, желчнокаменную болезнь, что определяет трудности диагностики данного заболевания. Боль может быть постоянной или рецидивирующей, сопровождаться тошнотой и рвотой. Наиболее часто ДД, как и ХП, страдают мужчины в возрасте 40—50 лет, злоупотребляющие алкоголем.
При лабораторных исследованиях может наблюдаться повышение активности амилазы в сыворотке крови, у больных с желтухой — увеличение уровня билирубина, щелочной фосфатазы и γ-глутамилтранспептидазы. Уровень онкомаркеров, как правило, не изменен [10].
При эндоскопическом и рентгенологическом исследованиях могут быть выявлены подслизистое образование ДПК, стеноз ДПК, а при морфологическом исследовании биопсийного материала отмечают лишь признаки дуоденита.
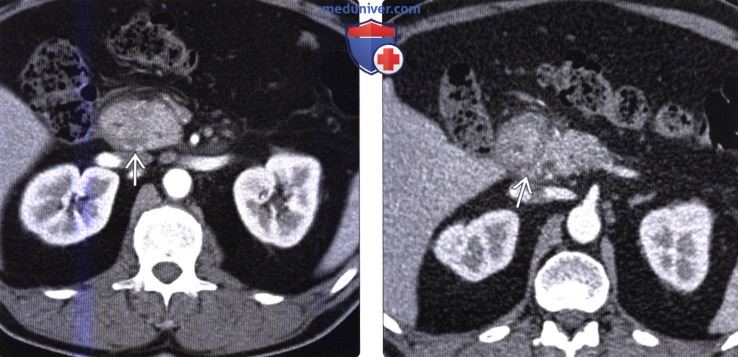
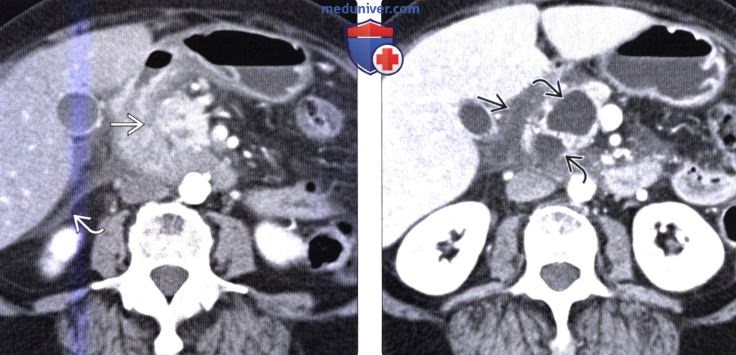
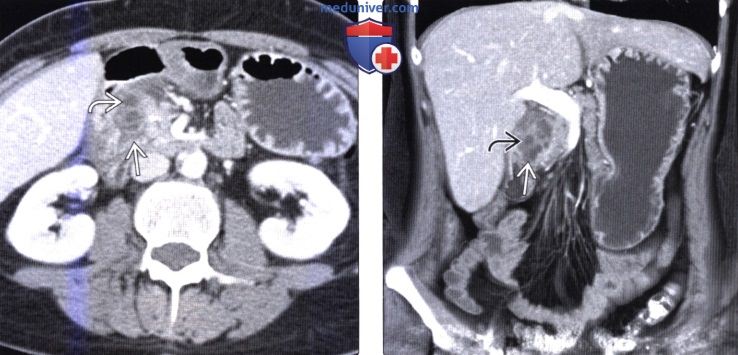
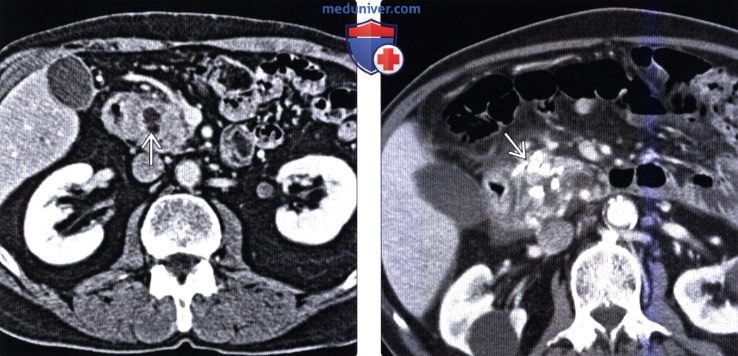
Ведущую роль в диагностике ДД играют современные лучевые методы визуализации. При компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ) и эндоскопической ультрасонографии (ЭУС) кистозная форма ДД определяется как утолщенная за счет фиброза стенка ДПК, содержащая полостные образования [9, 11]. Специфическим признаком ДД при КТ и МРТ является пристеночное кистозное образование с наличием выраженного мягкотканного компонента или без такового, фиброзное уплотнение, проявляющееся слоем компактной ткани между просветом ДПК и ПЖ [11].
В литературе встречаются сообщения о лечении ДД длительным приемом октреотида, применением эндоскопических методик, таких как цистогастростомия, фенестрация, однако результат их остается неудовлетворительным [12, 13]. Ведущим методом лечения пациентов с ДД остается хирургический [14—16]. При выраженных фиброзно-кистозных изменениях в головке ПЖ и ДПК операцией выбора признана панкреато-дуоденальная резекция (ПДР) [15, 16]. Наиболее перспективным является использование лапароскопических технологий, для которых характерны меньшая кровопотеря, отсутствие гнойно-воспалительных осложнений, снижение выраженности болевого синдрома в послеоперационном периоде и более быстрая реабилитация больных [17—20]. Вместе с тем выполнение лапароскопической ПДР ограничено техническими возможностями стационара, необходимостью особых хирургических навыков и знания хирургии данной области. Мы не встретили в доступных источниках литературы публикаций о выполнении лапароскопической ПДР при ДД.
При изолированном поражении эктопированной ПЖ возможна резекция ДПК с сохранением основной ПЖ [14]. Тем не менее мировой опыт выполнения подобных вмешательств минимален, а преимущества неясны, что не позволяет рекомендовать этот способ к широкому применению.
Представляем одно из клинических наблюдений. Больной Н., 44 года, впервые обратился в МКНЦ в июле 2014 г. с жалобами на постоянную боль в верхних отделах живота средней интенсивности (6—7 баллов по 10-балльной вербальной описательной шкале боли), иррадиирующую в поясничную область, не устраняемую приемом спазмолитиков, отрыжку воздухом, преимущественно натощак, вздутие, урчание в животе, снижение массы тела на 10 кг за последний год.
Из анамнеза известно, что с 1998 г. больной злоупотреблял алкоголем. В 2012 г. стала беспокоить боль в верхних отделах живота. При амбулаторном обследовании по месту жительства диагностирован ХП. В марте 2013 г. после погрешности в диете появились интенсивные боли в верхних отделах живота. При экстренной госпитализации по данным ультразвукового исследования (УЗИ) выявлена киста головки П.Ж. Получал консервативное лечение с положительным эффектом. С февраля 2014 г. приступы боли в верхней половине живота беспокоили ежемесячно, что приводило к повторным госпитализациям. В апреле 2014 г. наряду с болью стала беспокоить рвота после каждого приема пищи, осложнившаяся желудочно-кишечным кровотечением. Больной экстренно госпитализирован. При эзофагогастродуоденоскопии (ЭГДС) выявлены синдром Маллори—Вейсса, состоявшееся желудочно-кишечное кровотечение, признаки сдавления извне передней стенки бульбодуоденального перехода и верхней горизонтальной части ДПК. При МРТ в мае 2014 г. выявлены расширение ГППЖ, поликистозная трансформация ПЖ, кисты в отечной парапанкреатической клетчатке. В июне 2014 г. пациент госпитализирован в отделение патологии ПЖ и желчных путей МКНЦ.
При УЗИ выявлены диффузные изменения печени, деформация желчного пузыря, взвесь в желчном пузыре, признаки хронического кальцифицирующего панкреатита, киста головки П.Ж. Луковица и нисходящий отдел ДПК имели циркулярно утолщенные стенки до 7—11 мм, в стенке ДПК отмечены единичные гипоэхогенные участки от 4 до 5 мм (кисты?), просвет ДПК несколько сужен. Следовательно, выявлены ультразвуковые признаки ДД.
ЭГДС: поверхностный гастрит. Луковица ДПК средних размеров. Выход из луковицы сужен за счет циркулярного утолщения стенок бульбодуоденального перехода и верхней горизонтальной части.
Для подтверждения ДД проведена ЭУС, выявившая асцит, сонографические признаки ДД, хронического кальцифицирующего панкреатита, формирующейся кисты головки ПЖ, панкреатической гипертензии. Отмечалось увеличение лимфатических узлов по ходу гепатодуоденальной связки (см. рис. 1).
 Рис. 1. Результаты ЭУС больного Н. 1 — киста в стенке ДПК; 2 — кальцинаты в паренхиме ПЖ; 3 — киста головки ПЖ; 4 — расширенный ГППЖ.
Рис. 1. Результаты ЭУС больного Н. 1 — киста в стенке ДПК; 2 — кальцинаты в паренхиме ПЖ; 3 — киста головки ПЖ; 4 — расширенный ГППЖ.
Данные МСКТ органов брюшной полости с контрастным усилением свидетельствовали о наличии у больного кальцифицирующего панкреатита, вирсунголитиаза, панкреатической гипертензии с блоком на уровне головки П.Ж. Выявлены постнекротические кисты головки ПЖ, ДД, асцит.
В клиническом анализе крови уровень гемоглобина составил 11,6 г/дл. Биохимический анализ крови без особенностей. Наблюдалось повышение уровня диастазы в моче до 804 ед/л (норма 45—450 ед/л). Онкомаркеры С.А. 19—9 и РЭА в пределах референтных значений. Уровень фекальной эластазы-1 составил 150 мкг/г (<200 мкг/г).
Больному лапароскопическим способом выполнена гастропанкреатодуоденальная резекция. Технология выполнения такого вмешательства успешно используется в МКНЦ при лечении больных раком билиопанкреатодуоденальной зоны [21]. При патоморфологическом исследовании удаленного гастропанкреатодуоденального комплекса выявлены хронический калькулезный панкреатит; ДД, кистозная форма (см. рис. 2).
 Рис. 2. Гистологическое исследование: признаки хронического воспаления в аберрантной ПЖ. Окраска гематоксилином и эозином, ув. 100.
Рис. 2. Гистологическое исследование: признаки хронического воспаления в аберрантной ПЖ. Окраска гематоксилином и эозином, ув. 100.
Ранний послеоперационный период протекал без осложнений. Больной выписан на 8-е сутки в удовлетворительном состоянии. Выраженность болевого синдрома снизилась до 2 баллов.
Через 3 нед после хирургического лечения больного стали беспокоить учащение стула до 4—6 раз в сутки, изменение его консистенции на кашицеобразную, появление слабости, снижение массы тела. При лабораторном исследовании отмечено снижение концентрации эластазы кала до 15 мкг/г кала (тяжелая степень панкреатической недостаточности). Выявлено снижение уровня инсулина в крови до 2 мкед/мл (норма 2,7—10,4 мкед/мл) и С-пептида до 156 пмоль/л (норма 258—1718 пмоль/л), при этом уровень глюкозы и гликированного гемоглобина (5,4%) в крови оставались в норме.
Больному рекомендовали прием полиферментных препаратов в мини-микросферах или мини-таблетках в дозе по 40 000 ед. в обед и ужин и по 25 000 ед. на завтрак и полдник. Соблюдение диеты с низким содержанием легкоусвояемых углеводов, измерением уровня глюкозы в крови натощак, 1 раз в 3 мес определение уровня гликированного гемоглобина, наблюдение гастроэнтеролога, эндокринолога по месту жительства.
Спустя 5 мес от начала заместительной ферментной терапии больной жалоб не предъявлял, боль не беспокоила, стул нормализовался (1 раз в сутки), отмечалось увеличение массы тел на 5 кг.
В представленном случае клиническая картина заболевания, данные ЭГДС и УЗИ позволили предположить, а МСКТ и ЭУС подтвердить диагноз ДД.
Эндоскопическое и рентгенологическое исследование позволяют выявить деформацию и сужение просвета ДПК. Для исключения злокачественного процесса показана биопсия слизистой оболочки ДПК, которая у больного с ДД обычно выявляет лишь признаки воспаления. Диагностику Д.Д. значительно облегчает ЭУС, определяющая область и распространенность поражения, характер образования и позволяющая исключить другие причины сужения ДПК, такие как опухоль и кольцевидная ПЖ [22—24].
Таким образом, в диагностике и лечении столь редкой патологии, как ДД, требуется тесное сотрудничество врачей нескольких специальностей: гастроэнтерологов, хирургов, эндоскопистов, специалистов лучевой диагностики. Тщательный анализ клинической картины заболевания и специфические данные визуализирующих исследований позволяют установить правильный диагноз. При выраженном болевом синдроме и нарушении пассажа пищи по ДПК возникает необходимость хирургического лечения. Операцией выбора является ПДР, как правило, эффективно устраняющая болевой синдром. Применение лапароскопического доступа у больных данной категории целесообразно при наличии в клинике соответствующего опыта. Однако в последствии нередко развивается панкреатическая недостаточность, обусловливающая необходимость постоянной заместительной ферментной терапии и коррекции нарушения углеводного обмена. Ведение больных с ДД в условиях высокоспециализированных центров, обеспечивающих мультидисциплинарный подход, способствует благоприятному течению заболевания.
Конфликт интересов отсутствует.
Источник
Дуоденальной дистрофией называют патологическое состояние, при котором ткань поджелудочной железы хронически воспалена и вдобавок эктопирована в стенку двенадцатиперстной кишки. Это очень непростое заболевание, которое впервые было диагностировано только в 1970 году. Физиологическая основа — фиброзное утолщение стенок кишки, а также кистозный процесс мышечных и подслизистых тканей ее.
Типология и проявления
Кистозная и фиброзная дуоденальная дистрофия — это не различные расстройства, а стадии одного и того же заболевания. К кистозной фазе относятся кисты диаметром свыше сантиметра. Осложнением ДД чаще всего выступает панкреатит острой или хронической формы в ортотропической железе, при котором головка железы имеет воспалительную опухоль либо развивается тотальное повреждение ее и дилатация главного протока.
Дифференцировать дуоденальную дистрофию нужно от:
* злокачественных новообразований
* воспалений
* врождённых аномалий
Диагностические меры
Медицинская литература позволяет утверждать, что наиболее эффективно при диагностике этого вида расстройств именно трансабдоминальное УЗИ. В предоперационном периоде рекомендовано комплексное обследование — ЦДК, импульсная и отражательная допплерография. В отдельных случаях, при неудовлетворительности полученных таким образом данных, прибегают к трёхмерной или четырёхмерной разновидности сканирования. Эффективность распознавания кистозной формы дуоденальной дистрофии приближается к 96% (если работают профессионально).
Более чем в половине случаев отмечается наличие постнекротических кист. Рекомендуется, если дифференцировать патологический очаг затруднительно, перед самым сканированием, дать пациенту 200 мл жидкости (она должна быть выпита без проглатывания воздуха). Нисходящая ветвь двенадцатипёрстной кишки визуализируется с неравномерным уплотнением задней стенки, толщина ее колеблется от 1,6 до 8 сантиметров. Длина патологических очагов может составлять от 2,3 до 7,6 сантиметров.
Ещё о картине
Слизистая часть кишечной стенки при дуоденальной дистрофии не меняется, мышечные структуры ее содержат одно или несколько образований округлой (но не совсем правильной) формы. У кист всегда ровные и гладкие контуры, отмечается наличие тонкой сверхэхогенной капсулы, внутри которой — ещё более тонкие сверхэхогенные перегородки. Дуплексное сканирование никогда не показывает кровообращения ни в самой капсуле, ни в перегородках. Зато артерия, соединяющая желудок и двенадцатиперстную кишку, всегда при этом расстройстве смещается вперёд и влево, визуализируется правее патологического очага.
В отдельных случаях отмечают билиарную или портальную гипертензию, экстравазальную компрессию селезёночной, воротной, нижней полой и верхней брыжеечной вен. Обнаруживается калькулёз протоковой системы и паренхимы. Наряду с трансабдоминальным УЗИ рекомендуется проведение эндоскопического ультразвукового исследования, контрастной многофазной КТ и МРТ. Целесообразна повторная проверка прооперированных пациентов теми же методами через 3 месяца после операции. Солидная форма дуоденальной дистрофии должна дифференцироваться от солидных новообразований панкреатической природы.
Несмотря на хорошую отработанность инструментальных методов, окончательный диагноз почти всегда ставится только после гистологического изучения удалённого патологического очага. Эндоскопическая ультрасонография надёжнее других способов в различении дуоденальной дистрофии и муцинозных новообразований.
НАПИШИТЕ ВАШЕ ИМЯ И ТЕЛЕФОН, И МЫ ВАМ ПЕРЕЗВОНИМ И ЗАПИШЕМ НА УЗИ!
Источник
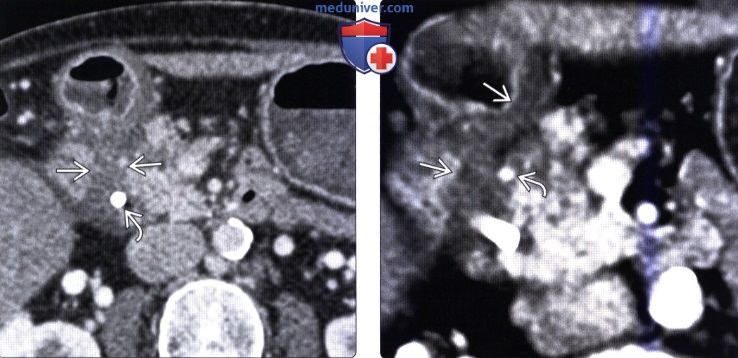
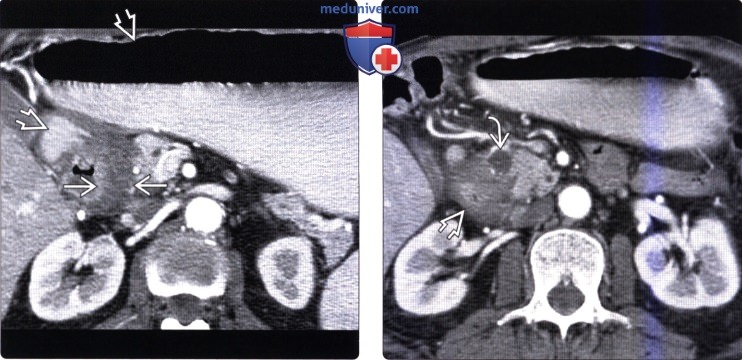
КТ, МРТ, УЗИ признаки парадуоденального (бороздчатого) панкреатитаа) Терминология: 1. Синонимы: 2. Определение: б) Визуализация: 1. Общая характеристика: 2. КТ признаки парадуоденального (бородчатого) панкреатита:
3. МРТ признаки парадуоденального (бородчатого) панкреатита: 4. УЗИ признаки парадуоденального (бородчатого) панкреатита: 5. Рекомендации по визуализации: б) Дифференциальная диагностика парадуоденального (бородчатого) панкреатита: 1. Протоковая аденокарцинома поджелудочной железы: 2. Рак двенадцатиперстной кишки: 3. Острый отечный панкреатит с вовлечением борозды:
в) Патология: 1. Общая характеристика: 2. Макроскопические и хирургические особенности: 3. Микроскопия: г) Клинические особенности: 1. Проявления парадуоденального (бородчатого) панкреатита: 2. Демография: 3. Течение и прогноз: 4. Лечение: д) Список использованной литературы: – Также рекомендуем “Лучевая диагностика аутоиммунного панкреатита (IgG4-обусловленного панкреатита)” Редактор: Искандер Милевски. Дата публикации: 9.3.2020 Оглавление темы “Лучевая диагностика патологии поджелудочной железы.”:
|
Источник