Аутотрансплантация поджелудочной железы это
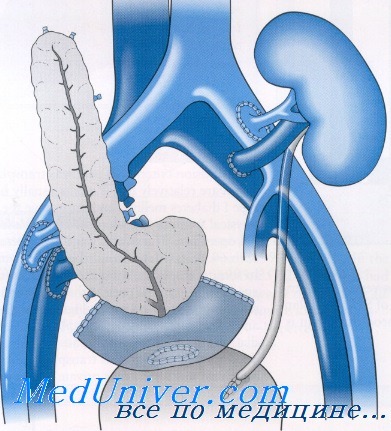
Техника трансплантации поджелудочной железы. Методики
История клинической трансплантации поджелудочной железы развивалась на фоне постоянного совершенствования техники оперативного вмешательства.
Первая попытка лечения СД трансплантационными методами была выполнена задолго до того, как De Mayer в 1909 г. дал название теоретически обоснованной эндокринной субстанции поджелудочной железы — инсулин, a F.G. Banting и С.Н. Best в 1921 г. выделили ее и таким образом открыли новую эпоху в лечении диабета. В декабре 1983 г., через 3 года после того, как J. von Mering и О. Minkowski экспериментально показали, что панкреатэктомия приводит к развитию сахарного диабета у собак, P. Williams в Бристоле пересадил 3 фрагмента овечьей поджелудочной железы в подкожную клетчатку 15-летнему пациенту, спустя 5 месяцев от клинической манифестации заболевания. Больной умер через 3 суток на фоне прогрессирующего кетоацидоза. Тем не менее этот эксперимент послужил мощным толчком к пониманию патогенеза заболевания и роли поджелудочной железы в углеводном обмене.
Впервые инсулинонезависимость при СД 1-го типа была достигнута 17 декабря 1966 г., когда W. Kelly и R. Lillehei одномоментно пересадили фрагмент поджелудочной железы с лигированным панкреатическим протоком и донорскую почку 28-летней пациентке, страдающей сахарным диабетом и уремией в состоянии диабетического кетоацидоза. Сегмент поджелудочной железы (тело и хвост) был трансплантирован экстраперитонеально, в левую подвздошную ямку. Инсулинонезависимость сохранялась в течение 6-ти суток послеоперационного периода. В дальнейшем у больной сформировалась панкреатическая фистула, нарастали явления панкреатита трансплантата, присоединилась раневая инфекция, и 14 февраля 1967 г. трансплантат поджелудочной железы (ТПЖ) был удален. Через 13 суток больная погибла от тромбоэмболии легочной артерии.
Вторую пересадку поджелудочной железы осуществила та же бригада хирургов. 31 декабря 1966 г. они выполнили аллогенную трансплантацию панкреатодуоденального комплекса (АТПДК) и почки 32-летнему пациенту, с наложением анастомоза между дистальной частью донорской duodenum и начальным отделом тощей кишки реципиента. В послеоперационном периоде дважды развивалась реакция отторжения трансплантата. Через 4,5 месяца на фоне септического состояния пациент скончался. К этому моменту инсулинотерапия проводилась в первоначальном объеме.
К началу 1973 г. R. Lillehei выполнил уже 13 АТПДК: у четырех пациентов была наложена наружная дуоденостома ТПЖ; у следующих 8-ми — Roux-en-Y дуоденоеюнальный анастомоз. Последней была выполнена пересадка целой поджелудочной железы, в которой для анастомоза с мочевым пузырем реципиента была использована только площадка Фатерова сосочка. Из 13 трансплантатов только один функционировал более года.
В 1978 г. J. Dubernard предложил оригинальную методику сегментарной трансплантации поджелудочной железы с окклюзией панкреатических протоков синтетическим отвердевающим полимером неопреном. По этой методике 3—10 мл неопрена инъецировались непосредственно в выводящие протоки сегмента поджелудочной железы, с последующим лигированием протоков для предотвращения экстравазации. Артериальное кровоснабжение хвоста и тела поджелудочной железы осуществлялось по селезеночной артерии, а венозный отток — через селезеночную вену, анастомозированным с наружными подвздошными сосудами реципиента.
Преимущество методики в том, что операция, по существу, сводится к наложению сосудистых анастомозов.
Окклюзия протоковой системы поджелудочной железы производится в ходе ее изъятия у донора, либо непосредственно перед наложением сосудистых анастомозов, либо через 10—14 дней после операции. В последнем случае в просвет главного панкреатического протока вводился полиэтиленовый катетер для наружного отведения экзокринного секрета и промывания протоковой системы железы с целью снижения явлений послеоперационного панкреатита.
Главный же недостаток трансплантации поджелудочной железы с окклюзией протоков — невозможность контроля уровня амилазы в экзогенном секрете. Между тем именно этот показатель зачастую служит главным маркером реакции отторжения поджелудочной железы.
Кроме того, введение неопрена вызывает прогрессирующий фиброз трансплантата и увеличивает частоту реакций отторжения.

В результате эндокринная функция большинства трансплантатов утрачивалась в среднем через 1 год после успешной пересадки, поэтому с появлением новых способов интерес к данной методике снизился. Тем не менее в некоторых европейских трансплантационных центрах метод по-прежнему используется.
Еще в 1971 г. M.L. Gliedman предложил оригинальную методику трансплантации сегмента поджелудочной железы с выведением экзокринного секрета в мочеточник (после предварительной нефрэктомии) у пациентов, находящихся в терминальной стадии диабетической нефропатии. К 1973 г. Gliedman сообщил о результатах четырех подобных трансплантаций сегментов поджелудочной железы.
На основе принципа отведения панкреатического сока в мочевы водящие пути (bladder drainage — BD) в дальнейшем было разработано множество способов трансплантации поджелудочной железы. В 1983 г. Н. Sollinger предложил отводить секрет в мочевой пузырь не посредством дуктоуретероанастомоза с нативным мочеточником реципиента, а с помощью панкреатикоцистостомии.
Но полное признание и повсеместное распространение пересадка поджелудочной железы по типу BD получила только с 1987 г., когда D.D. Nghiem и R.J. Сопу предложили использовать для анастомоза с мочевым пузырем нисходящую часть 12-перстной кишки донора с сохраненным дуоденальным сосочком и неповрежденным Вирсунговым протоком.
В настоящее время за редким исключением трансплантация поджелудочной железы по типу BD выполняется следующим образом: после МОЗ на отдельном столе проводится разделение блока печень — поджелудочная железа и/или проводится предоперационная подготовка изолированного трансплантата поджелудочной железы.
Селезенку отделяют, а селезеночные сосуды надежно перевязывают лигатурами, клипируют или прошивают степлером. Длина нисходящего участка 12-перстной кишки с головкой поджелудочной железы и большим дуоденальным сосочком рекомендуется в пределах 6—10 см; после орошения просвета кишки раствором антисептиков и противогрибковых препаратов обе культи кишки прошиваются степлером и погружаются кишечным швом по Lembert.
Селезеночную и верхнюю брыжеечную артерии трансплантата анастомозируют с общими подвздошными артериями V-образного сосудистого трансплантата, полученного от того же донора.
Используют бифуркацию аорты, общих подвздошных или бедренных артерий. При короткой портальной вене ее удлиняют по типу «конец-в-конец» при помощи трансплантата полой или общей подвздошной вен. Избыточный жир тщательно удаляется, избегая значимого контакта с паренхимой железы, а адвентициальные сосуды перевязываются. В течение всей подготовки поджелудочная железа тщательно сохраняется в охлажденном консервирующем растворе UW или Custodiol.
Производят срединную лапаротомию: этот доступ снижает риск раневой инфекции в послеоперационном периоде и позволяет выполнить одновременную пересадку поджелудочной железы и почки из одного разреза. Нередко используется и параректальный доступ.
Трансплантат поджелудочной железы помещают в правую подвздошную область головкой вниз. В левую подвздошную ямку помещают почечный трансплантат. Оба органа располагают интраперитонеально. Накладывают анастомозы между сосудами панкреатодуоденального комплекса и общими или наружными подвздошными сосудами реципиента. Двухрядным швом, вручную или степлером накладывается дуоденоцистостома длиной 3—4 см по типу «бок-в-бок». После наложения анастомозов трансплантат окутывают большим сальником и помещают в правый латеральный канал брюшной полости.
Трансплантация почки производится стандартно.
Лапаротомная рана ушивается послойно наглухо без дренирования брюшной полости. При необходимости дренирования дренажная трубка располагается непосредственно у сосудистых анастомозов и выводится наружу через контрапертуру.
Некоторые хирурги предпочитают экстраперитонеальную трансплантацию поджелудочной железы в одну из подвздошных ямок; оперативный доступ в этом случае будет аналогичен доступу, используемому для пересадки почки.
АТПЖ по типу BD обладает рядом неоспоримых преимуществ. Выведение экзокринного секрета в мочевой пузырь позволяет отслеживать уровень вырабатываемой трансплантатом амилазы и наличие воспалительных клеток с помощью анализа мочи и выявлять реакцию отторжения на ранних сроках. Отсутствие контакта с кишечным содержимым позволяет уменьшить опасность инфицирования протоков трансплантата поджелудочной железы, а мочевой катетер помогает контролировать состояние дуоденоцистоанастомоза.
Выживаемость трансплантата поджелудочной железы после изолированной пересадки по этому способу и по настоящее время существенно выше в сравнении с остальными. Однако наряду с достоинствами эта методика имеет и существенные недостатки: высокая частота инфекции мочевыводящих путей, гематурия, камнеобразование, мочевые затеки, панкреатит трансплантата поджелудочной железы, цистит, а также метаболический ацидоз и дегидратация за счет хронической потери жидкости и бикарбонатов с панкреатическим секретом. Поэтому с 1998 г. в мировой практике чаще используют отведение экзокринного секрета трансплантата поджелудочной железы в просвет кишечника реципиента.
Задача создания естественного, наиболее физиологичного дренирования панкреатического сока во внутрикишечное пространство стояла перед хирургами с самого начала освоения проблемы пересадки поджелудочной железы.
Трансплантации ПДК с наложением дуоденоеюноанастомоза были пионерскими операциями пересадки поджелудочной железы. Даже при сегментарных трансплантациях предпринимались попытки наложения инвагинационно-го панкреатикоеюноанастомоза. Однако частые осложнения в виде некрозов 12-перстной кишки и формирования фистул, связанные с ишемическим повреждением, скомпрометировали этот принцип. С совершенствованием методов консервации органов и прогрессом в области иммуносупрессии, приведшим к снижению риска ишемического или иммунологического повреждения двенадцатиперстной кишки, с начала 1990-х гг. интерес к возможности интестинального дренирования внешнего секрета трансплантированной поджелудочной железы (enteric drainage — ED) возродился.
На сегодняшний день пересадка поджелудочной железы по типу ED служит операцией выбора при SKPT и РАК.
По данным международного регистра, выживаемость пациентов после SKPT и РАК по типу ED значительно выше, чем по BD-методике, при том, что выживаемость трансплантатов различается незначительно. От 10 до 28% больных, ранее оперированных по BD-методике, в последующем подвергаются релапаротомии и реконструктивной операции по ED-типу в связи с развитием урологических осложнений.
Принципиальная техника оперативного вмешательства заключается в следующем. Выполняется срединная лапаротомия. Подготовка трансплантата поджелудочной железы аналогична операции по BD-методике, однако в этом случае к удлиняющей пластике портальной вены приходится прибегать существенно реже. Трансплантат поджелудочной железы располагается так, что хвост железы ориентирован в каудальном направлении, а головка направлена вверх, в сторону петли тощей кишки. Портальная вена анастомозируется с наружной или общей подвздошной веной реципиента вблизи нижней полой вены по типу «конец-в-бок». Общий аортоподвздошный V-образный черенок трансплантата поджелудочной железы анастомозируют с правой общей подвздошной артерией реципиента. Сначала удаляют венозные зажимы, кровотечение останавливается лигированием сосудов шелком 3—0 или 4—0. После остановки венозного кровотечения восстанавливают артериальный кровоток. Кровотечение устраняется аналогично.
После наложения сосудистых анастомозов и реваскуляризации трансплантата формируется кишечный дренаж. Для этого мобилизуют сегмент тощей кишки и отжимают его на расстоянии 40—80 см от дуоденоеюнального перехода. Рана промывается раствором антибиотика и отграничивается. Между оставшейся частью 12-перстной кишки трансплантата поджелудочной железы и мобилизованной петлей тощей кишки вручную двухрядным швом по Lambert или степлером накладывается дуоденоеюноанастомоз длиной 3—4 см по типу «бок-в-бок».
После пересадки поджелудочной железы в левый латеральный канал брюшной полости по стандартной методике трансплантируют донорскую почку.
Операционную рану закрывают послойно наглухо, при необходимости дренируют брюшную полость через отдельный прокол.
ED-вариант трансплантации поджелудочной железы имеет несколько модификаций. Некоторые хирурги использует для кишечного дренирования трансплантата Roux-петлю, сформированную из тощей или даже подвздошной кишки, при этом головка поджелудочной железы может быть направлена краниально, каудально или латерально. При анализе результатов как достоверных преимуществ, так и недостатков использования Roux-en-V петли не выявлено.
Межкишечный анастомоз может быть наложен также по типу «конец-в-конец» и «конец-в-бок».
Для наложения сосудистых анастомозов некоторые хирурги используют наружные подвздошные сосуды, а также аорту и нижнюю полую вену; в редких случаях накладывают разнонаправленные сосудистые анастомозы.
Заслуживает внимания способ дренирования Вирсунгова протока ПВХ-катетером, последовательно выведенным наружу через дуоденоеюноанастомоз и сформированную энтеростому. Метод позволяет контролировать функцию трансплантата по составу и динамике выделения панкреатического сока, на ранних сроках диагностировать реакцию отторжения, проводить профилактику ишемического панкреатита. Однако в связи с высоким риском инфекционных осложнений на фоне иммуносупрессивной терапии модификация не получила широкого распространения.
Некоторые хирурги рекомендуют накладывать анастомоз между веной трансплантата и верхней брыжеечной веной по типу «конец-в-бок», т.е. осуществлять венозный отток в систему воротной вены реципиента, что теоретически более физиологично.
Обоснованием этого считают отмеченные в ряде исследований случаи гиперинсулинемии за счет попадания секретируемого трансплантатом инсулина непосредственно в системный кровоток, минуя печеночный этап регуляции углеводного обмена. Однако практически незначительные преимущества портального дренирования связаны с немалыми техническими трудностями, и большинство хирургов выбирает системное отведение крови от ПДК, тем более что факт послеоперационной гиперинсулинемии в этом случае признают далеко не все исследователи.
Недостатки АТПДК с отведением панкреатического сока в просвет кишечника: во-первых, высокий риск хирургических послеоперационных осложнений (кишечная непроходимость и несостоятельность межкишечного анастомоза); во-вторых, невозможность использовать показатели внешней секреции железы в качестве маркера воспалительных или иммунологических осложнений.
Таким образом, в настоящее время используются три основных метода трансплантации поджелудочной железы. При выполнении АТПДК одновременно или после пересадки почки предпочтительнее использовать различные варианты интестинального дренирования экзокринного секрета трансплантата. АТПЖ с отведением панкреатического сока в мочевыводящие пути преимущественно используется при изолированных пересадках поджелудочной железы в случаях гиперлабильного диабета и предуремической диабетической нефро-патии. Сегментарная АТПЖ с окклюзией панкреатических протоков может быть рекомендована одновременно с пересадкой почки ослабленным больным, а также при длительных сроках консервации или значительном ишемическом повреждении трансплантата поджелудочной железы.
– Вернуться в оглавление раздела “Хирургия”
Оглавление темы “Хирургическая патология поджелудочной железы”:
- Инструментальная диагностика острого панкреатита у пожилых. Методика
- Консервативное лечение острого панкреатита. Принципы
- Хирургическое лечение острого панкреатита. Принципы
- Хирургические вмешательства у больных инфицированным панкреонекрозом в пожилом возрасте. Особенности
- Результаты лечения инфицированного панкреонекроза. Исходы
- Трансплантация поджелудочной железы. Показания
- Требования к трансплантату поджелудочной железы. Подготовка доноров
- Техника изъятия поджелудочно-дуоденального комплекса. Принципы
- Селекция реципиентов поджелудочной железы. Принципы
- Техника трансплантации поджелудочной железы. Методики
Источник
Когда заболевания поджелудочной железы переходят в стадию безуспешности консервативного лечения, тогда не обойтись без хирургического вмешательства. Оно решает многие задачи по исцелению. Самой тяжелой операцией является пересадка поджелудочной железы.
Такие операции начали осуществляться с 1966 года. На сегодняшний день их количество и качество увеличилось, что выражается в увеличении продолжительности жизни после операций. Пересаживают железу отдельными ее частями и полностью. Всегда присутствует риск отторжения трансплантата.
Диагностика и показания к трансплантации
Операция на поджелудочной железе, ее успешность, связана с многочисленными проблемами. Трудности технического плана несравнимы с пересадкой печени и почек. Лишь очень жесткие показания позволяют выполнять такую операцию.
С целью установления необходимости пересадки органа пациенту назначается полноценное обследование по протоколу ведения заболевания:
Инструментальная диагностика:
- КТ;
- ультразвуковое исследование сердечной мышцы, брюшинных органов, сосудов,
- рентген грудной клетки;
- электрокардиограмма;
- лабораторные исследования:
- биохимия состава крови;
- моча, кровь клинические анализы;
- серологический анализ на инфекции;
- подтверждение группы крови.
Возможны и другие исследования, назначенные профессионалами узких специализаций:
- гастроэнтеролога;
- абдоминального хирурга;
- гинеколога;
- терапевта;
- анестезиолога;
- эндокринолога;
- стоматолога.
Чаще всего хирургическое решение проблемы предлагается больным, имеющим недуг сахарного диабета первого или второго типа до того, как у них начнутся его последствия:
- диабет гиперлабильный;
- нейропатия;
- неполноценность функций эндокринной или экзокринной частей;
- угроза слепоты при ретинопатии — поражение сетчатки глазного яблока;
- поражение почек — нефропатии;
- тяжелые недуги сосудов.
Поэтому пересадка поджелудочной железы при сахарном диабете не является жизненно необходимой. Она способствует предотвращению тяжелых последствий сахарного диабета.
Симптоматический сахарный диабет, т. е. вторичный – причина развития следующих осложнений:
- панкреатит, сопровождающийся развитием панкреонекрозов;
- гемохроматоз;
- иммунность к инсулину;
- рак поджелудочной железы;
Трансплантация поджелудочной железы показана при этих заболеваниях
Особо надо выделить пересадку органа при панкреатите. Это связано с тем, что чаще всего сбои в работе органа сопровождаются развитием такого недуга. А вот его последствия и осложнения — прямой путь к хирургическому вмешательству, если консервативная терапия не принесла результата.
При панкреатите острой фазы могут проявиться признаки гнойно-деструктивного характера, это случается в промежутке 7-14 дней. Кроме того, у раненной поджелудочной железы может развиться онкология. Все осложнения при панкреатите, требующие вмешательства хирургов, могут привести к пересадке органа, или его частей.
Редкие случаи показаний к пересадке при структурных повреждениях:
- опухоли разных характеров, приведшие к диффузии железы;
- значительное омертвение составляющих железы;
- неподдающееся консервативной терапии поражение железы, которое произошло вследствие гнойного воспаления в брюшине.
Какая предстоит пересадка и ее отличительные черты
Характерность разрушения тканей органа, анализ готовности пациента к операции, которая базируется на обследовании, краеугольные камни в выборе хирургической операции пересадки:
- железа в полном объеме;
- ее хвостовая часть;
- зоны тела органа;
- железа плюс участок 12-перстной кишки, так называемый панкрео — дуоденальный комплекс;
- клеточная терапия культурами бета-клеток железы.
В отличие от почек поджелудочная железа один орган в организме. Трансплантация поджелудочной железы, ее успешность зависит от подбора донора, и забора поджелудочной железы.
Донор по возрасту может быть от 3 до 55 лет, главное, чтобы он был здоров, и его состояние сопровождалось мозговой смертью. Для определения показаний к забору органа донора исследуется на различные инфекции и заболевания.
Если орган пригоден, то его отчуждают либо с печенью и 12-перстной кишкой, либо каждый по отдельности. В любом случае поджелудочная железа отделяется от них, консервируется в специальном растворе, хранится в контейнере с низкой температурой не более 20–30 часов.
Существуют различные методики отвода ферментного сока при операциях:
- Пересадка участками, сегментами использует блокировку выводного канала каучуковым полимером неопреном или иным синтетическим быстроотвердевающим.
- Отвести ферментный сок можно в другие выводящие органы: кишки, мочевой пузырь. Недостатком таких объединений с выводной протокой являются последующие болезни органа, проявляющиеся гематуриеи, инфекциями, ацидозом, утерей солидного объема бикарбонатов ферментов. Зато есть возможность распознать начало отторжения трансплантата, благодаря контролю содержания амилазы в моче.
Диабетическая нефропатия предполагает пересадку почка вместе с поджелудочной железой. Здесь избирается один из путей пересадки:
- только железа;
- сначала почка, затем поджелудочная железа последовательно;
- одновременная пересадка почки и железы, которая стала предпочтительней другим.
Развитие медицины не стоит на месте. На смену стандартным методам пересадки приходят новые инновации. Среди них трансплантация клеток островков Лангерганса. Пока это сделать трудно. Механизм действия такой операции:
- измельчить поджелудочную железу донора, подвергнув состав клеток влиянию коллагеназы;
- в особой центрифуге их надо разделить на фракции по плотности;
- жизнеспособный материал, который удается извлечь, вводят в органы: селезенку, под капсулу почки, портальную вену.
Эта методика находится в начале своего жизненного пути. Но если эксперимент удается, пациенты с диабетом 1-го и 2-го типа получают возможность выработки собственного инсулина, что повышает качество жизни счастливчиков.
Еще одна экспериментальная методика заключается в попытке пересадки поджелудочной железы от эмбриона 16–20-недель. Железа эмбриона по массе 10-20 мг, но уже может выделять инсулин со своим ростом. По непроверенной статистике таких пересадок произведено до 200 штук, но успех ограничен.
Результаты пересадки
Пациента всегда волнует удачность операции. Во многом ее исход зависит от предоперационного протокола действий:
- результаты тканевой совместимости в зависимости от анализов на антигены трансплантата;
- операция по трансплантации должна быть плановой. Срочное проведение операции не позволяет выполнить весь протокол мероприятий по подготовке больного и трансплантата;
- пересадку надо проводить в специализированных клиниках по трансплантации органов, у которых накоплен опыт таких операций;
- достаточное финансирование операции.
После вмешательства следует длительное наблюдение, сдача анализов, осмотры, которые позволят сделать вывод о результате трансплантации:
- Если углеводный обмен приходит в норму и пациент освобождается от потребности ввода инсулина, то пересадка была успешной. Если вдобавок пересажена и почка, то удается прекратить усиление болезней, приводящих к гемодиализу почек: нейропатии, ретинопатии, нефропатии:
- Отторжение проявляется не сразу. Одна железа, как правило, не отторгается, она сопровождается отторжением и почки, если была такая пересадка. Для почки характерные признаки отторжения в повышении креатинина, олигурии и другие анализы, что служит показателем и к железе. Трансплантат набухает, его края размыты, хвост визуализируется плохо при обследовании на УЗИ, МРТ.
В любом случае пациентам назначается иммуносупрессивная терапия на всю жизнь. Ее цель – подавление ненужных, агрессивных проявлений иммунных реакций против клеток собственного организма. Она имеет протокол применения, состоящего из 2–3 препаратов, которые имеют различные механизмы влияния, а также симптоматическая терапия. Это необходимое условие по поддерживанию приживаемости пересаженного органа.
В дальнейшем пациент находится на диспансеризации, продолжает лечиться дома, получая подробные рекомендации от доктора, в том числе и нового качества жизни.
Источник
