Синтез инсулина в поджелудочной железе вызывает
Инсулин — самый молодой гормон
Строение
Инсулин представляет собой белок, состоящий из двух пептидных цепей А (21 аминокислота) и В (30 аминокислот), связанных между собой дисульфидными мостиками. Всего в зрелом инсулине человека присутствует 51 аминокислота и его молекулярная масса равна 5,7 кДа.
Синтез
Инсулин синтезируется в β-клетках поджелудочной железы в виде препроинсулина, на N-конце которого находится концевая сигнальная последовательность из 23 аминокислот, служащая проводником всей молекулы в полость эндоплазматической сети. Здесь концевая последовательность сразу отщепляется и проинсулин транспортируется в аппарат Гольджи.
На данном этапе в молекуле проинсулина присутствуют А-цепь, В-цепь и С-пептид (англ. connecting – связующий). В аппарате Гольджи проинсулин упаковывается в секреторные гранулы вместе с ферментами, необходимыми для «созревания» гормона . По мере перемещения гранул к плазматической мембране образуются дисульфидные мостики, вырезается связующий С-пептид (31 аминокислота) и формируется готовая молекула инсулина. В готовых гранулах инсулин находится в кристаллическом состоянии в виде гексамера, образуемого с участием двух ионов Zn 2+ .
Схема синтеза инсулина
Регуляция синтеза и секреции
Секреция инсулина происходит постоянно, и около 50% инсулина, высвобождаемого из β-клеток, никак не связано с приемом пищи или иными влияниями. В течение суток поджелудочная железа выделяет примерно 1/5 от запасов имеющегося в ней инсулина.
Главным стимулятором секреции инсулина является повышение концентрации глюкозы в крови выше 5,5 ммоль/л, максимума секреция достигает при 17-28 ммоль/л. Особенностью этой стимуляции является двухфазное усиление секреции инсулина:
- первая фаза длится 5-10 минут и концентрация гормона может 10-кратно возрастать, после чего его количество понижается,
- вторая фаза начинается примерно через 15 минут от начала гипергликемии и продолжается на протяжении всего ее периода, приводя к увеличению уровня гормона в 15-25 раз.
Чем дольше в крови сохраняется высокая концентрация глюкозы, тем большее число β-клеток подключается к секреции инсулина.
Индукция синтеза инсулина происходит от момента проникновения глюкозы в клетку до трансляции инсулиновой мРНК. Она регулируется повышением транскрипции гена инсулина, повышением стабильности инсулиновой мРНК и увеличением трансляции инсулиновой мРНК.
Активация секреции инсулина
1. После проникновения глюкозы в β-клетки (через ГлюТ-1 и ГлюТ-2) она фосфорилируется гексокиназой IV (глюкокиназа, обладает низким сродством к глюкозе),
2. Далее глюкоза аэробно окисляется, при этом скорость окисления глюкозы линейно зависит от ее количества,
3. В результате нарабатывается АТФ, количество которого также прямо зависит от концентрации глюкозы в крови,
4. Накопление АТФ стимулирует закрытие ионных K + -каналов, что приводит к деполяризации мембраны,
5. Деполяризация мембраны приводит к открытию потенциал-зависимых Ca 2+ -каналов и притоку ионов Ca 2+ в клетку,
6. Поступающие ионы Ca 2+ активируют фосфолипазу C и запускают кальций-фосфолипидный механизм проведения сигнала с образованием ДАГ и инозитол-трифосфата (ИФ3),
7. Появление ИФ3 в цитозоле открывает Ca 2+ -каналы в эндоплазматической сети, что ускоряет накопление ионов Ca 2+ в цитозоле,
8. Резкое увеличение концентрации в клетке ионов Ca 2+ приводит к перемещению секреторных гранул к плазматической мембране, их слиянию с ней и экзоцитозу кристаллов зрелого инсулина наружу,
9. Далее происходит распад кристаллов, отделение ионов Zn 2+ и выход молекул активного инсулина в кровоток.
Схема внутриклеточной регуляции секреции инсулина при участии глюкозы
Описанный ведущий механизм может корректироваться в ту или иную сторону под действием ряда других факторов, таких как аминокислоты, жирные кислоты, гормоны ЖКТ и другие гормоны, нервная регуляция .
Из аминокислот на секрецию гормона наиболее значительно влияют лизин и аргинин. Но сами по себе они почти не стимулируют секрецию, их эффект зависит от наличия гипергликемии, т.е. аминокислоты только потенциируют действие глюкозы.
Свободные жирные кислоты также являются факторами, стимулирующими секрецию инсулина, но тоже только в присутствии глюкозы.
Логичной является положительная чувствительность секреции инсулина к действию гормонов желудочно-кишечного тракта – инкретинов (энтероглюкагона и глюкозозависимого инсулинотропного полипептида), холецистокинина, секретина, гастрина, желудочного ингибирующего полипептида.
Клинически важным и в какой-то мере опасным является усиление секреции инсулина при длительном воздействии соматотропного гормона, АКТГ и глюкокортикоидов, эстрогенов, прогестинов. При этом возрастает риск истощения β-клеток, уменьшение синтеза инсулина и возникновение инсулинзависимого сахарного диабета. Такое может наблюдаться при использовании указанных гормонов в терапии или при патологиях, связанных с их гиперфункцией.
Нервная регуляция β-клеток поджелудочной железы включает адренергическую и холинергическую регуляцию. Любые стрессы (эмоциональные и/или физические нагрузки, гипоксия, переохлаждение, травмы, ожоги) повышают активность симпатической нервной системы и подавляют секрецию инсулина за счет активации α2-адренорецепторов. С другой стороны, стимуляция β2-адренорецепторов приводит к усилению секреции.
Также выделение инсулина повышается n.vagus, в свою очередь находящегося под контролем гипоталамуса, чувствительного к концентрации глюкозы крови.
Мишени
Рецепторы инсулина находятся практически на всех клетках организма, кроме нервных, но в разном количестве. Нервные клетки не имеют рецепторов к инсулину, т.к. последний просто не проникает через гематоэнцефалический барьер.
Механизм действия
После связывания инсулина с рецептором активируется ферментативный домен рецептора. Так как он обладает тирозинкиназной активностью, то фосфорилирует внутриклеточные белки — субстраты инсулинового рецептора. Дальнейшее развитие событий обусловлено двумя направлениями: MAP-киназный путь и ФИ-3-киназный механизмы действия (подробно).
При активации фосфатидилинозитол-3-киназного механизма результатом являются быстрые эффекты – активация ГлюТ-4 и поступление глюкозы в клетку, изменение активности «метаболических» ферментов – ТАГ-липазы, гликогенсинтазы, гликогенфосфорилазы, киназы гликогенфосфорилазы, ацетил-SКоА-карбоксилазы и других.
При реализации MAP-киназного механизма (англ. MAP — mitogen-activated protein) регулируются медленные эффекты – пролиферация и дифференцировка клеток, процессы апоптоза и антиапоптоза.
Два механизма действия инсулина
Скорость эффектов действия инсулина
Биологические эффекты инсулина подразделяются по скорости развития:
Очень быстрые эффекты (секунды)
Эти эффекты связаны с изменением трансмембранных транспортов :
1. Активации Na + /K + -АТФазы , что вызывает выход ионов Na + и вход в клетку ионов K + , что ведет к гиперполяризации мембран чувствительных к инсулину клеток (кроме гепатоцитов).
2. Активация Na + /H + -обменника на цитоплазматической мембране многих клеток и выход из клетки ионов H + в обмен на ионы Na + . Такое влияние имеет значение в патогенезе артериальной гипертензии при сахарном диабете 2 типа.
3. Угнетение мембранной Ca 2+ -АТФазы приводит к задержке ионов Ca 2+ в цитозоле клетки.
4. Выход на мембрану миоцитов и адипоцитов переносчиков глюкозы ГлюТ-4 и увеличение в 20-50 раз объема транспорта глюкозы в клетку.
Быстрые эффекты (минуты)
Быстрые эффекты заключаются в изменении скоростей фосфорилирования и дефосфорилирования метаболических ферментов и регуляторных белков.
Печень
- торможение эффектов адреналина и глюкагона (фосфодиэстераза),
- ускорение гликогеногенеза (гликогенсинтаза),
- активация гликолиза (фосфофруктокиназа, пируваткиназа),
- превращение пирувата в ацетил-SКоА (ПВК-дегидрогеназа),
- усиление синтеза жирных кислот (ацетил-SКоА-карбоксилаза),
- формирование ЛПОНП,
- повышение синтеза холестерина (ГМГ-SКоА-редуктаза),
Мышцы
- торможение эффектов адреналина (фосфодиэстераза),
- стимулирует транспорт глюкозы в клетки (активация ГлюТ-4),
- стимуляция гликогеногенеза (гликогенсинтаза),
- активация гликолиза (фосфофруктокиназа, пируваткиназа),
- превращение пирувата в ацетил-SКоА (ПВК-дегидрогеназа),
- усиливает транспорт нейтральных аминокислот в мышцы,
- стимулирует трансляцию (рибосомальный синтез белков).
Жировая ткань
- стимулирует транспорт глюкозы в клетки (активация Глют-4),
- активирует запасание жирных кислот в тканях (липопротеинлипаза),
- активация гликолиза (фосфофруктокиназа, пируваткиназа),
- усиление синтеза жирных кислот (активация ацетил-SКоА-карбоксилазы),
- создание возможности для запасания ТАГ (инактивация гормон-чувствительной-липазы).
Медленные эффекты (минуты-часы)
Медленные эффекты заключаются в изменении скорости транскрипции генов белков, отвечающих за обмен веществ, за рост и деление клеток, например:
1. Индукция синтеза ферментов в печени
- глюкокиназы и пируваткиназы ( гликолиз ),
- АТФ-цитрат-лиазы, ацетил-SКоА-карбоксилазы, синтазы жирных кислот, цитозольной малатдегидрогеназы ( синтез жирных кислот ),
- глюкозо-6-фосфатдегидрогеназы ( пентозофосфатный путь ),
2. Индукция в адипоцитах синтеза глицеральдегидфосфат-дегидрогеназы и синтазы жирных кислот.
3. Репрессия синтеза мРНК, например, для ФЕП-карбоксикиназы ( глюконеогенез ).
4. Обеспечивает процессы трансляции, повышая фосфорилирование по серину рибосомального белка S6.
Очень медленные эффекты (часы-сутки)
Очень медленные эффекты реализуют митогенез и размножение клеток. Например, к этим эффектам относится
1. Повышение в печени синтеза соматомедина, зависимого от гормона роста.
2. Увеличение роста и пролиферации клеток в синергизме с соматомединами.
3. Переход клетки из G1-фазы в S-фазу клеточного цикла.
Инактивация инсулина
Удаление инсулина из циркуляции происходит после его связывания с рецептором и последующей интернализации (эндоцитоза) гормон-рецепторного комплекса, в основном в печени и мышцах. После поглощения комплекс разрушается и белковые молекулы лизируются до свободных аминокислот. В печени захватывается и разрушается до 50% инсулина при первом прохождении крови, оттекающей от поджелудочной железы. В почках инсулин фильтруется в первичную мочу и, после реабсорбции в проксимальных канальцах, разрушается.
Патология
Гипофункция
Инсулинзависимый и инсулиннезависимый сахарный диабет. Для диагностики этих патологий в клинике активно используют нагрузочные пробы и определение концентрации инсулина и С-пептида.
Источник статьи: https://biokhimija.ru/gormony/insulin.html
Источник
Инсулин – это гормон, вырабатываемый поджелудочной железой, который необходим для метаболизма углеводов и, в меньшей степени, жиров. Благодаря инсулину энергия (глюкоза) из пищи переносится из крови в клетки. Таким образом снижается уровень сахара в крови и обеспечивается питание клеток.
Когда уровень инсулина в норме, уровень сахара в крови в норме. Когда инсулин слишком низкий (или не работает должным образом), диагностируется диабет. Когда уровень инсулина высокий, а уровень сахара в норме, мы говорим об инсулинорезистентности.
Диабет 1 типа, диабет 2 типа и инсулинорезистентность – это проблемы со здоровьем, которые связаны с инсулином – гормоном, необходимым для жизни. Он нужен организму в строго определенном количестве. Опасны как дефицит инсулина, так и его чрезмерный избыток.
Какую роль инсулин играет в организме? Когда следует проверять его уровень? Что происходит, когда инсулина слишком мало или слишком много?
Как действует инсулин
Инсулин – это гормон, понижающий уровень сахара в крови. Его образно называют ключом, открывающим клетки энергии из пищи. Источником энергии для организма являются углеводы. Энергия из простых углеводов проникает в кровь практически сразу после еды, сложные углеводы сначала нужно расщепить на простые сахара – глюкозу в процессе пищеварения. Она циркулирует в крови и попадает в клетки только в присутствии инсулина. Без инсулина клетки не могут получать энергию из пищи, даже если в крови много глюкозы.
Механизм действия инсулина
Отсюда взаимосвязь между уровнем сахара и инсулином. Когда этот гормон отсутствует, глюкоза не попадает в клетки, она остается в крови, что приводит к гипергликемии. Состояние диагностируют в лабораторных исследованиях или с помощью глюкометра.
Важно отметить, что инсулин не снижает уровень сахара в крови до нуля, то есть не вся энергия из пищи поступает в клетки. Строго определенное количество сахара остается в крови и является топливом, необходимым для работы мозга. Мозгу постоянно нужна глюкоза, это орган, не зависящий от действия инсулина, он забирает сахар из крови без этого гормона.
Вот почему в крови здорового человека содержится определенное количество сахара, которое в лабораторных условиях дает результат в диапазоне 70-99 мг/дл глюкозы натощак.
Инсулин – это белок. Поэтому его следует принимать в виде подкожной инъекции. Таблеток инсулина не существует, потому что они перевариваются в пищеварительном тракте.
Подкожная инъекция инсулина
Инсулин и глюкагон
Инсулин вырабатывается в ответ на повышение уровня глюкозы в крови. После обильной еды с большим количеством углеводов уровень этого гормона в кровотоке значительно увеличивается. Между приемами пищи и ночью уровень инсулина ниже.
Гормон, противоположный инсулину, – это глюкагон, повышающий уровень сахара в крови. В здоровом организме эти два гормона остаются в равновесии. Глюкагон высвобождается, когда сахар в крови начинает слишком низко падать (например, ночью), а инсулин – когда сахар в крови начинает слишком сильно повышаться.
Благодаря сбалансированной секреции этих двух гормонов, у здорового человека уровень сахара остается нормальным как после обильной еды, так и в результате многочасового голодания.
Инсулин – анаболический или строительный гормон, благодаря которому можно выращивать клетки (неиспользованная глюкоза превращается в жир). Высокий уровень инсулина в организме, типичный для инсулинорезистентности, способствует увеличению избыточного веса.
Когда не хватает инсулина
Отсутствие или тяжелая недостаточность инсулина означает диабет типа 1. Это заболевание диагностируется по заметно повышенному уровню сахара в крови (гипергликемия). Его лечение заключается в восполнении дефицита инсулина. Причина нехватки инсулина у пациентов с диабетом 1 типа – это разрушение иммунной системой бета-клеток поджелудочной железы (аутоиммунное заболевание).
Сегодня на рынке представлено множество препаратов инсулина. Инсулин животного происхождения ушел в прошлое, сегодня применяются так называемый человеческий инсулин и аналог инсулина.
Инсулины различаются не только способом их получения, но и временем действия. В инсулиновой терапии используются инсулины короткого действия, 3-5 часов, которые следует принимать во время еды, и базальные инсулины, действующие в течение 18-24 часов, которые сохраняют нормальный уровень сахара в крови между приемами пищи.
Симптомы нехватки инсулина:
- Очень сильная жажда;
- Отхождение большого количества мочи;
- Похудение – клетки голодают, не могут получать энергию из крови, организм начинает сжигать жир, что приводит к потере веса.
Очень сильная жажда
Похудение
До того как был «изобретен» инсулин, диабет 1 типа считался смертельным заболеванием. Пострадавшие пациенты гибли от крайнего недоедания. Поскольку теперь инсулин производят в лабораториях, и он доступен всем, диабет 1 типа перешел в разряд хронических заболеваний.
Когда слишком много инсулина
Избыток инсулина тоже вреден для организма. Мы имеем дело с высоким уровнем инсулина в крови при:
- сахарном диабете 2 типа;
- резистентности к инсулину.
Инсулинорезистентность – это нарушение обмена веществ, диабет 2 типа – это заболевание, которое возникает в результате инсулинорезистентности, поэтому эти проблемы можно обсуждать вместе. Они отличаются тем, что гликемия нормальна при инсулинорезистентности и повышена при диабете 2 типа.
Инсулинорезистентность
Высокая концентрация инсулина возникает, когда поджелудочная железа вынуждена производить избыточный инсулин. Когда это происходит? Когда клетки организма нечувствительны к инсулину (другими словами – устойчивы к нему). Чтобы преодолеть это сопротивление, поджелудочная железа вырабатывает повышенное количество гормона, что дает побочные эффекты:
- Инсулин стимулирует аппетит;
- Как анаболический гормон, он способствует увеличению веса.
Выработка большого количества инсулина ложится нагрузкой на поджелудочную железу, она перестает быть эффективной в этом процессе. Поэтому на основе инсулинорезистентности развивается диабет 2 типа.
Когда проверяют уровень инсулина?
Уровни инсулина проверяются в трех случаях:
- У пациентов с диабетом 1 типа, как правило, сразу после постановки диагноза, чтобы узнать, секретирует ли поджелудочная железа больше инсулина. Это делается путем выравнивания пептида C.
- У людей с подозрением на инсулинорезистентность с целью подтверждения / исключения низкой чувствительности к инсулину.
- Для подтверждения реактивной гипогликемии (чрезмерное падение уровня глюкозы в крови у людей без диабета).
Поделиться ссылкой:
Источник
В этой статье вы узнаете:
Очень важно знать, как работает организм в норме, чтобы понять те изменения, которые происходят в нем при развитии диабета. Большинство процессов в теле человека контролируются гормонами. Органом, вырабатывающим инсулин, является поджелудочная железа. Гормон синтезируется в особых клетках, которые называются бетта-клетками.

Такие клетки располагаются в железе в виде отдельных обособленных скоплений. Их называют островками Ларгенганса.
Кроме выработки инсулина поджелудочная железа также синтезирует пищеварительные ферменты. Как правило, эта функция железы не изменяется и хорошо выполняется без отклонений только у пациентов с диабетом 1 типа.
При втором типе на состояние поджелудочной влияет не только диабет, но и множество сопутствующих заболеваний (ожирение, желчекаменная болезнь, хронический гастрит и другие), отчего ее функция может измениться самым различным образом.
Почему поджелудочная перестает вырабатывать инсулин?
Иммунная система помогает человеку бороться с вирусами, микробами, уничтожает чужеродные клетки, в том числе и раковые, которые могут образовываться в процессе жизни человека. Происходит постоянное обновление клеток в разных органах: старые гибнут, а новые образуются, замещая их.
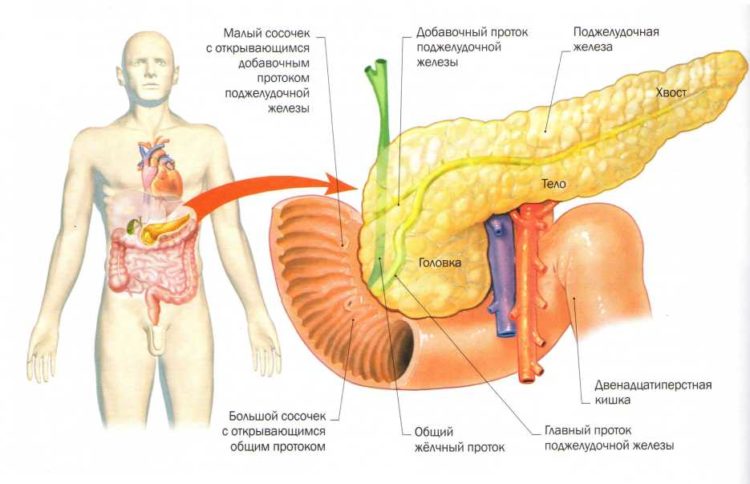 Расположение поджелудочной железы
Расположение поджелудочной железы
Это касается и бетта-клеток поджелудочной железы. Иммунитет в норме хорошо различает «свои» клетки от «чужеродных».
У пациентов с диабетом 1 типа происходит «поломка» в иммунитете, и организм начинает воспринимать собственные клетки как чужие, и убивает их.
Наследственность и действие окружающей среды (чаще всего вирусы) изменяют свойства β-клеток.
Выделяют ряд причин, почему поджелудочная железа не вырабатывает инсулин.
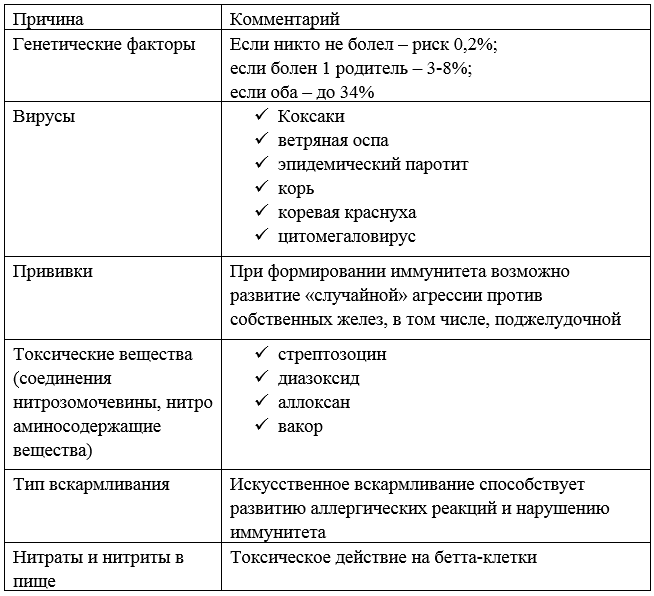 Таблица – Причины, из-за которых может снижаться выработка инсулина
Таблица – Причины, из-за которых может снижаться выработка инсулина
Происходят следующие процессы:
- Выделяются аутоантигены.
- Клетки иммунной системы (макрофаги МФ, дендритные клетки ДК) передают переработанные аутоантигены Т-лимфоцитам, которые, в свою очередь, начинают воспринимать их как чужеродные.
- Часть Т-лимфоцитов, превратившихся в специфические цитотоксические аутоагрессивные лимфоциты (ЦТЛ).
- Развивается воспаление поджелудочной железы и разрушение β-клетки.
Этот процесс длительный и протекает с различной скоростью: от нескольких месяцев у маленьких детей до нескольких лет у взрослых.
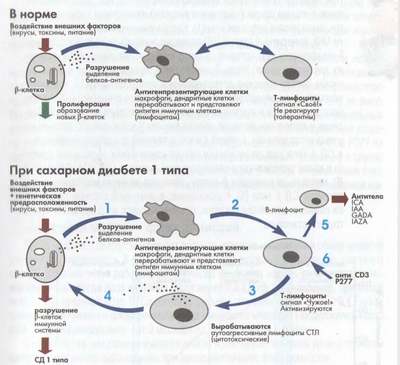 Аутоиммунное разрушение β-клеток
Аутоиммунное разрушение β-клеток
По данным научных исследований, у людей с наследственной предрасположенностью к сахарному диабету 1 типа уже за несколько лет до начала заболевания в крови определяются специфические антитела (IAA, ICA, GADA, IA-2β), которые, не разрушая β-клетку, являются ранними маркерами риска развития СД 1 типа.
К сожалению, в иммунной системе сохраняется память к антигенам β-клеток, поэтому процесс их разрушения очень трудно остановить.
Учёные считают, что при диабете 1 типа бетта-клетки могут восстанавливаться. Даже при гибели 90 % процентов всех бетта-клеток из оставшихся 10 % может произойти восстановление. Однако для этого необходимо остановить «агрессивную» реакцию иммунной системы. Только тогда станет возможным излечение от этой болезни.
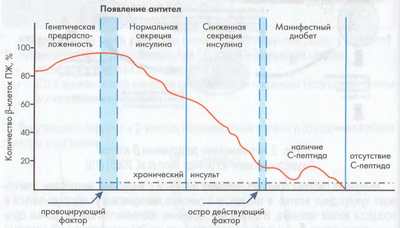 Стадии развития диабета 1 типа
Стадии развития диабета 1 типа
Только введение инсулина может быть настоящим лечением сахарного диабета 1 типа.
Некоторые исследования были направлены на изучение возможности остановить «агрессивное поведение» иммунной системы по отношению к бетта-клеткам путём применения нескольких групп препаратов. Однако достоверных положительных результатов получено не было.
Большую надежду учёные связывают с возможностью применения моноклональных антител, способных изменить агрессивный иммунитет в благоприятную сторону, т. е. снизить аутоиммунную реакцию в поджелудочной железе.
Эти исследования являются очень перспективными, поскольку в случае отсутствия контроля над иммунитетом даже пересадка островков Ларгенганса и применение стволовых клеток будут бессмысленны.
Работа инсулина
Основная функция гормона заключается в том, что он связывается с рецептором на клетке (специальный датчик узнавания). Если узнавание произошло («ключ подошел к замку»), то клетка становится проницаемой для глюкозы.
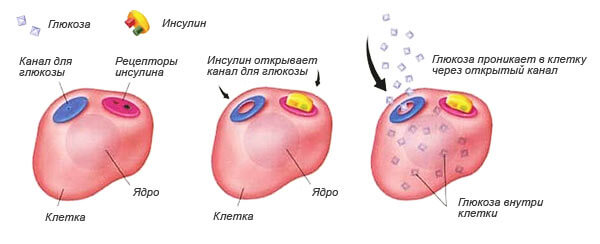 Воздействие инсулина на клетку
Воздействие инсулина на клетку
Выработка инсулина начинается уже тогда, когда мы видим еду и ощущаем ее запах. По мере переваривания пищи, высвобождения из нее глюкозы и попадания ее в кровь, бетта-клетки увеличивают выработку инсулина, поэтому, у здоровых людей уровень сахара крови всегда сохраняется в пределах нормы и не зависит от того, сколько сладкого они съели.
Инсулин отвечает за попадание глюкозы в так называемые «инсулинозависимые ткани»: печень, мышцы, жировая ткань.
Интересный факт: Самые главные органы не нуждаются в инсулине. В «инсулиннезависимые» клетки сахар из крови попадает просто по градиенту концентрации: когда его в клетке меньше, чем в крови, он свободно переходит в клетку. Такими органами являются головной мозг, нервы, сетчатка, почки, надпочечники, кровеносные сосуды и эритроциты.
Такой механизм необходим для того, чтобы в случае недостатка глюкозы крови выработка инсулина останавливалась и сахар поступал бы только в самые важные органы.
Организму необходимо немного инсулина даже в ночное время и в периоды голода, чтобы обеспечить усвоение глюкозы, образующейся в печени. Такой инсулин называют базальным или фоновым.
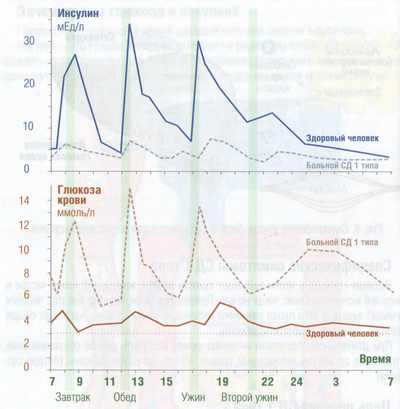 Уровни инсулина и глюкозы в крови
Уровни инсулина и глюкозы в крови
Существует еще болюсный инсулин. Это то количество гормона, которое вырабатывается в ответ на прием пищи.
Помните, необходимо научиться рассчитывать и вводить себе дозу инсулина в зависимости от количества принятой пищи. Поэтому так важно обучение при сахарном диабете 1 типа. Без знаний о своей болезни и правилах поведения адекватное лечение практически невозможно.
Очень важно также оценивать потребность в инсулине. У человека без диабета вырабатывается приблизительно 0,5 ЕД инсулина на кг массы тела каждый день. Для взрослого с массой тела 70 кг получаем 70*0,5=35 ЕД в сутки.
| Период | Доза инсулина |
|---|---|
| Дети до полового созревания | 0,7–1,0 ЕД/кг/день (Обычно ближе к 1 ЕД/кг/день) |
| Период полового созревания | Мальчики – 1,1–1,4 ЕД/кг/день (иногда даже больше) Девочки – 1,0–1,2 ЕД/кг/день |
| Подростки | Девушки – меньше 1 ЕД/кг/день Юноши – примерно 1 ЕД/кг/день |
| Взрослые | 0,7 – 0,8 ЕД/кг/день |
У большинства пациентов через 1–3 года от момента возникновения потребность в инсулине стабилизируется и составляет 0,7–1,0 ЕД/кг.
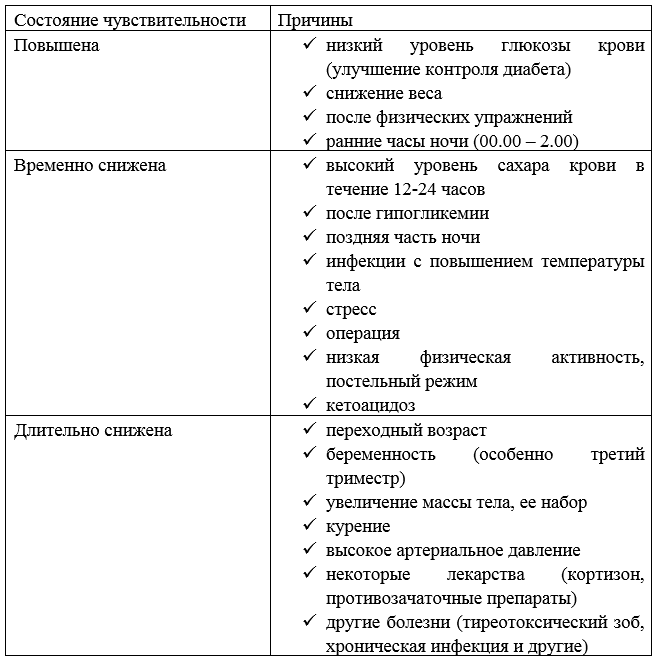
Чувствительность к инсулину
Чувствительность организма к гормону важна для определения того, насколько конкретная доза инсулина снизит уровень сахара крови. К сожалению, одна и та же доза инсулина не всегда оказывает одинаковый эффект на снижение глюкозы крови.
Определенные факторы повышают чувствительность к инсулину, другие причины – уменьшают.
 Таблица – Факторы, влияющие на чувствительность к инсулину
Таблица – Факторы, влияющие на чувствительность к инсулину
Инсулинорезистентность означает, что требуется большее количество инсулина, чтобы поучить такой же эффект снижения сахара крови. Другими словами, происходит уменьшение чувствительности к инсулину.
Давно известно, какая железа вырабатывает инсулин. Но что еще, кроме поджелудочной железы, вырабатывает инсулин в организме человека?
В последние годы пристальный интерес вызываю вещества инкретины – это гормоны, секретируемы клетками желудочно-кишечного тракта и стимулирующие действие инсулина.
Наиболее изучены:
- Глюкагоноподобный пептид-1 (ГПП-1);
- Глюкозозависимый инсулиноподобный пептид (ГИП).
Последнее вещество оказывает эффект, сравнимый с действием инсулина.
Основные эффекты инкретинов:
- увеличивают синтез инсулина после еды;
- улучшают потребление глюкозы клетками, что приводит к снижению сахара крови.
Существуют данные, что у пациентов с диабетом данное вещество продолжает синтезироваться в прежних количествах, в то время, как бетта-клетки гибнут. Проблема состоит в том, что инкретины очень быстро распадаются под действием собственных ферментов организма.
Источник
