Причины нарушений внешней секреции поджелудочной железы

Поджелудочная железа играет важную роль не только в процессах пищеварения, но и в жизнедеятельности организма в целом. Этот орган эндокринной и пищеварительной систем вырабатывает ферментные вещества, необходимые для расщепления пищи, поступающей в желудок, а также некоторые гормоны для регулировки жирового и углеводного обмена.
Описание органа
Рассмотрим строение и функции поджелудочной железы. Она расположена в забрюшинном пространстве между участками двенадцатиперстной кишки и верхними позвонками поясницы, над почками, и внешне напоминает вытянутую «запятую». Вес органа взрослого человека колеблется в диапазоне 80-90 г.
Строение поджелудочной представляет собой сочетание железистых долек, через которые проходят сосуды крови, и выводящих протоков. Дольки продуцируют панкреатический сок, ферменты которого (лактаза, амилаза, трипсин, инвертаза, липаза) влияют на процессы расщепления пищи. По всей железе проходит канал, по которому сок проникает в двенадцатиперстную кишку, где смешивается с желчью и обеспечивает процесс кишечного пищеварения. Комплексы клеток между дольками с развитой капиллярной сетью называются островками Лангерганса. Эти образования из альфа-, бета- и дельта-клеток синтезируют гормоны (инсулин и глюкагон).
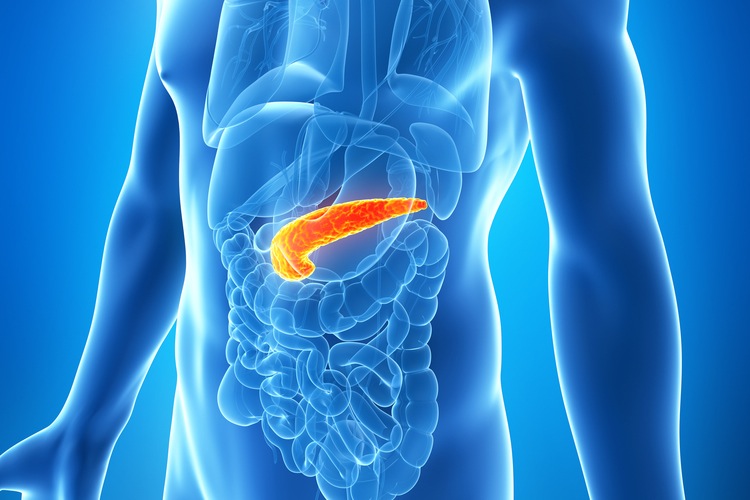
Структура
Орган имеет такую структуру:
- головка (размер 2,5-3,5 см) плотно прилегает к изгибу двенадцатиперстной кишки;
- треугольное тело (2,5 см) располагается слева от позвоночника по направлению к селезенке;
- шейка;
- грушевидный хвост (3 см), через который идет основной проток железы.
Где болит поджелудочная железа у человека, расскажем ниже.
Функции органа
Поджелудочная железа, как уже было сказано, продуцирует панкреатический сок. В двенадцатиперстной кишке пища расщепляется до необходимого для всасывания состояния. Это происходит под действием гидролитических пищеварительных ферментов поджелудочной железы, отвечающих за взаимодействие веществ пищи с водой.
Панкреатический сок состоит из гидролаз, которые выполняют отдельные функции. Их подразделяют на четыре категории:
- Липаза – это фермент, который расщепляет жиры на сложные элементы: глицерин и высшие жирные кислоты. Он также обеспечивает усвояемость витаминов A, E, D, K.
- Протеазы (химотрипсин, карбоксипептидаза, трипсин), активизирующие ферменты, которые разрушают белки до аминокислот.
- Карбогидразы (амилаза, мальтаза, лактаза, инвертаза), необходимые для расщепления углеводов до глюкозы.
- Нуклеазы – ферменты, разрывающие нуклеиновые кислоты и образующие собственные генетические структуры.
Принцип функционирования поджелудочной железы весьма сложен. Ферменты начинают вырабатываться в необходимом количестве через 2-3 минуты после поступления в желудок пищи. При этом все зависит от концентрации жиров, белков и углеводов, присутствующих в ней. При наличии желчи продуцирование панкреатического сока с ферментами может длиться до 12 часов.
Эндокринная функция
Эндокринная функция железы осуществляется благодаря инсулоцитам – специальным клеткам островков Лангерганса. Они синтезируют ряд гормонов: тиролиберин, с-пептид, соматостатин, инсулин, гастрин, глюкагон.

Внешнесекреторная недостаточность поджелудочной железы
Она является одним из наиболее распространенных последствий воспаления органа, особенно если такая патология характеризуется хроническим течением.
Отличительным признаком внешнесекреторной недостаточности поджелудочной железы является снижение всасывания компонентов питания (мальабсорбция) на фоне развития мальдигестии – нарушения расщепления пищи на приемлемые для процесса пищеварения компоненты. Данную патологию также называют ферментной недостаточностью. Несмотря на распространенность подобных патологий среди всех групп людей, недостаточность выработки ферментов считается серьезным состоянием, которое способно привести к истощению и даже летальному исходу пациента при отсутствии лечения.
Разновидности
Внешнесекреторная недостаточность поджелудочной железы бывает врожденного (генетический дефект, который нарушает либо блокирует секрецию ферментов) и приобретенного типа. Кроме того, патология может носить первичный и вторичный характер, быть абсолютной или относительной.
Первичная внешнесекреторная недостаточность обусловлена поражением железы и снижением ее экзокринной функции. При вторичном типе болезни ферменты продуцируются в достаточном количестве, но в тонком кишечнике их активация не происходит.
Причины развития патологии
К основным причинам развития внешнесекреторной недостаточности поджелудочной железы первичного типа относятся все формы хронического панкреатита, муковисцидоз, рак поджелудочной, перерождение панкреас при ожирении, оперативные вмешательства на железе, синдром Швахмана, врожденная недостаточность ферментов, агенезия либо гипоплазия органа, а также синдром Йохансона – Близзарда.
Патогенетические причины формирования внешнесекреторной недостаточности железы включают:
- фиброз и атрофию органа (как результат алкогольного, обструктивного, некалькулезного или калькулезного панкреатита, атеросклероза, неправильного питания, возрастных изменений, гемосидероза, сахарного диабета);
- панкреатический цирроз (считается исходом некоторых форм панкреатита: фиброзно-калькулезного, алкогольного, сифилитического);
- панкреонекроз (гибель клеток железы);
- формирование конкрементов в панкреатических протоках.
Вторичная внешнесекреторная недостаточность развивается при поражениях слизистого покрова тонкого кишечника, после операций на желудке и кишечнике, при гастриноме, снижении секреции энтерокиназы, патологиях гепатобилиарной системы, белково-энергетической недостаточности.
Абсолютная ферментная недостаточность железы обусловлена подавлением секреции бикарбонатов и ферментов на фоне уменьшения объема органа. Относительная недостаточность обусловлена сниженным поступлением панкреатического сока в кишечник вследствие обтурации просветов протоков железы опухолью, камнем, рубцами.
Рубцы на поджелудочной железе возникают в результате гибели клеток паренхимы органа. В этих участках формируется плотная рубцовая ткань. Подобный процесс в медицине называется фиброзом, и он также ведет к развитию внешнесекреторной недостаточности.
Симптомы
Разберемся, где болит поджелудочная железа у человека. Наибольшее значение в клинической картине данной патологии имеет синдром мальдигестии, который характеризуется угнетением процессов пищеварения в кишечнике. Непереваренные жиры в толстой кишке стимулируют продуцирование колоноцитов – развивается диарея и полифекалия, кал приобретает зловонный запах, серый цвет, его поверхность блестящая и маслянистая. В стуле также могут присутствовать непереваренные частицы пищи.
Мальдигестия протеинов способствует появлению белково-энергетической недостаточности, которая проявляется дегидратацией, прогрессирующим похудением, дефицитом микроэлементов и витаминов, анемией. На потерю веса большое воздействие оказывает соблюдение диеты с низким содержанием углеводов и жиров, а также страх приема пищи, который формируется у многих пациентов с панкреатитом хронического характера.
Симптомы внешнесекреторной недостаточности поджелудочной железы довольно неприятны. Нарушение моторики желудка (диспепсические расстройства, чувство переполнения) может быть обусловлено как обострением панкреатита, так и влиянием экзокринной недостаточности железы вследствие изменения гастроинтестинальной регуляции, возникновения дуодено-гастрального рефлюкса.
Панкреатит как причина патологии
Хронический панкреатит – основной фактор, приводящий к ферментной недостаточности. Это поражение поджелудочной железы воспалительно-деструктивного генеза, приводящее к нарушениям ее функций. Каковы последствия панкреатита, мало кто знает. При обострении заболевания возникает боль в животе и левом подреберье, наблюдаются диспепсические явления, желтушность склер и кожного покрова.
Основными причинами развития панкреатита у взрослых (код по МКБ-10 К86) являются желчекаменная болезнь и злоупотребление алкоголем, который довольно токсичен для паренхимы этого органа. При желчекаменной болезни воспалительный процесс становится следствием перехода инфекции из желчевыводящих протоков в железу по лимфатическим сосудам, развитием гипертензии желчных путей либо забросом желчи в железу.
Консервативное лечение данного заболевания включает в себя комплекс мер. В основе терапии лежат следующие принципы:
- обязательна диета;
- недостаточность поджелудочной железы подлежит коррекции;
- болевой синдром нужно устранить;
- осложнения должны быть предупреждены.
При лечении панкреатита необходимо исключить употребление алкоголя, прием лекарственных препаратов, способных оказывать повреждающее воздействие на поджелудочную железу (антибиотики, антидепрессанты, сульфаниламиды, диуретики: гипотиазид и фуросемид, непрямые антикоагулянты, индометацин, бруфен, парацетамол, глюкокортикоиды, эстрогены и многие другие).

Последствия панкреатита могут быть различными: внешнесекреторная недостаточность железы, обтурационная желтуха, портальная гипертензия, инфекции (парапанкреатит, абсцесс, флегмона забрюшинной клетчатки, воспаление желчевыводящих путей), внутренние кровотечения. С развитием данного заболевания могут возникать также сахарный диабет, снижение массы тела, рак поджелудочной железы.
Диагностика
Основную роль при выявлении ферментной недостаточности при панкреатите у взрослых (код по МКБ-10 К86) играют специальные тесты (беззондовые и зондовые), которые часто комбинируют с рентгенологическими, ультразвуковыми и эндоскопическими методами. Зондовая диагностика считается более дорогостоящей и может причинять пациентам дискомфорт, однако ее результаты более точные. Беззондовые процедуры дешевле, они легко переносятся, но дают возможность определить данный патологический процесс в организме только при полном отсутствии или существенном снижении панкреатических ферментов.
Прямой секретин-холецистокининовый зондовый тест считается золотым стандартом диагностики внешнесекреторной панкреатической недостаточности. Данная методика основана на стимуляции секреции железы введением холецистокинина и секретина, с дальнейшим забором проб дуоденального содержимого с промежутком времени в 10 минут. В образцах исследуется скорость и активность панкреатической секреции, уровень цинка, бикарбонатов, лактоферрина.
Непрямое зондовое тестирование Лунда похоже на предыдущий метод, однако стимуляция секреции железы производится посредством введения в зонд пищи.
В основе беззондовых методик лежит введение в организм некоторых веществ, способных взаимодействовать с панкреатическими ферментами в крови и моче. Исследование метаболических продуктов такого взаимодействия предоставляет возможность оценить внешнесекреторные функции железы. К беззондовым тестам относятся: панкреато-лауриловый, бентирамидный, триолеиновый, йодолиполовый и другие.
Определить уровень панкреатической активности можно и некоторыми косвенными способами: по уровню поглощения поджелудочной железой аминокислот плазмы, посредством качественного анализа копрограммы, определения в кале объема жира, трипсина и фекального химотрипсина, эластазы-1.
Инструментальными методами диагностики заболевания являются: рентген брюшины, КТ, МРТ, УЗИ поджелудочной железы, ЭРХПГ.
Лечение патологии
Лечение внешнесекреторной недостаточности поджелудочной железы, как правило, комплексное. Оно включает в себя коррекцию нутритивного статуса, заместительную и этиотропную терапию, а также симптоматическое лечение. На предупреждение прогрессирования гибели клеток железы направлена этиотропная терапия. Коррекция образа жизни заключается в исключении потребления спиртного и табакокурения. Предусмотрено также увеличение количества в рационе белка, сокращение объема жиров, прием витаминов.
Основным методом лечения при хр. панкреатите является заместительный прием ферментов (пожизненно). Показанием к заместительной терапии ферментами выступает стеаторея с утратой более 15 г жира в день, белково-энергетическая недостаточность прогрессирующего характера.

Наибольшей эффективностью обладают микрогранулированные ферментные средства в кислотоустойчивых оболочках и в желатиновых капсулах, которые растворяются в желудке, обеспечивая условия для равномерного смешивания гранул медикамента с пищей. Дозировки таких лекарств подбираются индивидуально и зависят от тяжести заболевания, активности панкреатической секреции.
Источник

Объем секрета поджелудочной железы составляет 1500 мл в сутки. Он выделяется в тонкую кишку и содержит ферменты, гидролизирующие белки, жиры и углеводы. Регуляция секреции осуществляется гормонами – холецистокинином (стимулирует секрецию ферментов) и секретином (стимулирует секрецию бикарбонатов). Регуляция панкреатической секреции осуществляется через блуждающий нерв.
Основными причинами нарушений внешней секреции поджелудочной железы являются:1) недостаточная продукция секретина при ахлоргидрии; 2) неврогенное торможение функции поджелудочной железы (при ваготомии, отравлении атропином); 3) развитие аллергических реакций; 4) воздействие различными химическими веществами (отравление фосфором, свинцом, ртутью, кобальтом); 5) травмы брюшной полости; 6) токсикоинфекции (брюшной тиф, паратифы); 7) хронические инфекции (туберкулез, малярия); 8) алиментарные факторы (избыточный прием пищи, животных жиров и др.); 9) разрушение поджелудочной железы опухолевым процессом; 10) закупорка и сдавление протока опухолью; 11) дуо-
дениты – воспалительные процессы в ДПК любой этиологии (инфекционные, паразитарные и др.), ведущие к уменьшению образования секретина, с последующей гипосекрецией поджелудочной железы; 12) воздействие алкоголем, усиливающим выброс соляной кислоты, что ведет к стимуляции выработки секретина с избыточным выделением панкреатического секрета; 13) острые и хронические панкреатиты.
Этиология и патогенез острого панкреатита.Основными этиологическими факторами(в 70% случаев) острого панкреатита являются желчекаменная болезнь и прием алкоголя.Возникновение острых алкогольных панкреатитов объясняется не только токсическим воздействием алкоголя. Алкоголь стимулирует выброс соляной кислоты, которая, воздействуя на слизистую двенадцатиперстной кишки, усиливает секрецию секретина. Последний является мощным стимулятором панкреатической секреции, избыточное выделение которой ведет к повышению давления в протоках железы и развитию острого панкреатита. Кроме того, крепкие алкогольные напитки способствуют отеку слизистой ДПК, что вызывает спазм фатерова соска с последующим повышением давления в панкреатических протоках. Известно и непосредственное воздействие алкоголя на сосуды поджелудочной железы, вызывающее их спазм. Это ведет к ишемии органа с гибелью ацинозных клеток и к активации ферментов в ткани железы. Прием алкоголя в дозе, превышающей 100 г/сут в течение нескольких лет, может привести к преципитации панкреатических ферментов в мелких протоках и формированию белковых пробок. Более редкими причинами развития острого панкреатита являются травмы живота, гиперлипидемия (особенно I и IV типа), прием некоторых лекарственных препаратов (азотиаприн, сульфазалазин, фуросемид, кортикостероиды, эстрогены), инфекции (эпидемический паротит, болезнь Боткина, сальмонеллез), оперативные вмешательства, диагностическая ретроградная холангиопанкреатография, анатомические аномалии панкреатического протока (стриктуры, опухоли), гиперкальциемия, уремия, сосудистые поражения, наследственная предрасположенность.
Рассматриваются 3 механизма развития острого панкреатита. Наиболее принята теория самопереваривания ткани железы,согласно которой протеолитические ферменты – трипсиноген, химотрипсиноген, проэластаза и фосфолипаза А активируются внутри протока поджелудочной железы. Полагают, что некоторые факто-
ры (эндо- и экзотоксины, в частности алкоголь, вирусные инфекции, ишемия и травма) активируют проферменты, т.е. в условиях патологии трипсиноген может активироваться в железе под влиянием кофермента цитокиназы, выделяющейся из поврежденных клеток паренхимы. Важную роль в развитии панкреатита играет и ингибитор трипсин, который в норме в достаточном количестве содержится в поджелудочной железе и препятствует превращению трипсиногена в трипсин. При большой активности трипсина ингибиторы антиферментной системы истощаются, и возникает их дефицит. Это используется как тест в диагностике острого панкреатита: чем выше содержание трипсиногена в сыворотке крови, тем меньше ингибитора трипсина. При дефиците этого фактора отмечается активный переход трипсиногена в трипсин. Усиленная активность протеолитических ферментов, особенно трипсина, приводит к перевариванию ткани поджелудочной железы и к активации других ферментов – эластазы и фосфолипазы. Происходит переваривание активными ферментами клеточных мембран, развивается протеолиз, отек, интерстициальное воспаление, повреждение сосудов, коагуляционный, жировой некроз (стеатонекроз)и некроз паренхимы железы. Повреждение и разрушение клеток ведут к высвобождению активированных ферментов. Переваривающее действие ферментов сказывается и на периферии. С этим связан феномен «уклонения ферментов в кровь», вызывающий развитие некротических процессов в других органах. При попадании липазы в кровь возможны некрозы отдаленных органов с тяжелой последующей интоксикацией. Процесс может осложниться перитонитом и абсцессами брюшной полости. Трипсин активирует панкреатический калликреин, вызывающий образование каллидина и брадикинина, которые усиливают повреждение ткани железы. Идет дальнейшая активация кининовой системы. Активация и высвобождение брадикинина и гистамина вызывают различные гемодинамические расстройства. Расширяются сосуды, повышается проницаемость их стенок и развивается отек железы. Выход жидкости и белка в ткани ведет к снижению онкотического давления и развитию панкреатического коллапса,иногда со смертельным исходом. Этот коллапс можно воспроизвести в эксперименте при внутривенном введении животному панкреатического сока. Если сок предварительно прокипятить, то коллапс не разовьется.
Вторая теория – это теория «общего канала».Благодаря анатомической особенности у большинства людей (у 80%) имеется об-
щий желчный и панкреатический проток, что облегчает рефлюкс желчи в проток поджелудочной железы. Однако в норме давление в панкреатическом протоке в 2 раза выше, чем в общем желчном протоке (200 мм вод. ст.). Это предохраняет от заброса желчи и кишечного содержимого в протоки поджелудочной железы. Заброс желчи может отмечаться при гипертонусе сфинктера Одди или гипермоторной дискинезии желчных путей. Частое развитие панкреатита при желчекаменной болезни объясняется происходящим повышением давления в желчевыводящей системе. Это обеспечивает заброс инфицированной желчи под большим давлением в панкреатический проток, что вызывает химическое повреждение ткани железы, повышает ее ферментативную активность. Фосфолипаза желчи активирует трипсиноген. При желчекаменной болезни приступы острого панкреатита могут быть связаны с преходящей обтурацией фатерова соска желчными камнями. Заброс кишечного содержимого возможен при зиянии фатерова соска или при гипертонической дискинезии ДПК, возникающей при воспалении, воздействии алиментарных и других факторов. При этом попадающая в железу энтеропептидаза активирует трипсиноген. Образовавшийся трипсин оказывает аутокаталитическое действие – активирует трипсиноген и другие протеолитические ферменты. Так, если в эксперименте ввести в проток поджелудочной железы небольшое количество трипсина, то происходит выраженный некроз ее ткани, поскольку образуются активные протеолитические ферменты.
Третья теория объясняет развитие панкреатита обструкцией панкреатического протокаи гиперсекрецией.Обструкция (спазм сфинктера Одди, отек ДПК и др.) вызывает задержку выделения панкреатического секрета с последующей активацией ферментов внутри железы.
При панкреатите развиваются 3 стадии: острый приступ (отек, возможно панкреонекроз), стадия неполного излечения с персистирующим хроническим воспалением или деструкцией панкреатического протока и затем стадия хронического воспаления с экзокринной недостаточностью поджелудочной железы. С развитием фиброзных изменений в ткани железы, связанных с перенесенным острым панкреатитом, наступает внешнесекреторная (экзокринная) недостаточность поджелудочной железы, характерная для хронического панкреатита. В железе уменьшается, а затем полностью прекращается (при склерозировании, сморщивании органа) об-
разование пищеварительных ферментов (панкреатическая ахилия).Нарушаются полостное пищеварение (в полости тонкой кишки) и всасывание. В первую очередь резко страдает переваривание и всасывание жиров. Жиры до 60-80% не усваиваются и в повышенном количестве выводятся с калом (стеаторея – выделение с калом более 5 г в сутки или более 5-6% от введенного изотопа – триолеат-глицерина J131). Отмечается полифекалия, при копрологическом исследовании в кале много нейтрального жира (так как нарушается расщепление жиров до жирных кислот). Стеаторея вызывает потерю организмом кальция, который экскретируется вместе с жирами в виде нерастворимых мыл (в кале, кроме нейтрального жира, будут мыла). Наряду с ионами кальция теряются и ионы магния, цинка, которые также образуют мыла с невсосавшимися жирами. Развиваются синдромы гипокальциемии, гипомагниемии. В меньшей степени и позднее нарушается переваривание белка (не усваивается до 30-40%). Об этом свидетельствует появление большого количества мышечных волокон в кале (креаторея),особенно после приема мясной пищи. Переваривание углеводов также нарушается. Отмечается снижение объема секреции поджелудочной железы, гидрокарбонатов в панкреатическом соке (после стимуляции секретином 1 мг/кг массы) и ферментов – амилазы, трипсина, липазы (после стимуляции панкреозимином 1,5 мг/кг массы). Расстройство пищеварения усугубляется диспепсическим симптомокомплексом. Возникает синдром диареи, развивается синдром малдигестии, идет прогрессирующая потеря массы тела (в случае отсутствия заместительной терапии).

Не нашли то, что искали? Воспользуйтесь поиском гугл на сайте:
©2015- 2020 zdamsam.ru Размещенные материалы защищены законодательством РФ.
Источник
