Опухоль надпочечников и поджелудочной железы
Болезнь Гиппеля—Линдау (Von Hippel—Lindau syndrome — VHL) — это наследственное заболевание, связанное с делециями и мутациями в гене Va184Leu (VHL tumour suppressor gene) [1]. Частота данного заболевания составляет 1 случай на 36 000—39 000 человек [2]. VHL имеет вариабельный фенотип, который наиболее часто проявляется в виде гемангиобластомы сетчатки, почечно-клеточной карциномы, эндокринных заболеваний надпочечников и поджелудочной железы [3].
По классификации ВОЗ выделяют VHL 1-го и 2-го типов [2]:
1. VHL 1-го типа: ретинальная ангиома, гемангиобластома, почечно-клеточная карцинома. Данный тип встречается в 83% всех случаев болезни Гиппеля—Линдау [4].
2. VHL 2-го типа:
2А — ангиома сетчатки, гемангиобластома и феохромоцитома;
2В — ангиома сетчатки, почечно-клеточная карцинома и феохромоцитома;
2С — только феохромоцитома.
VHL в сочетании с феохромоцитомой встречается только в 17% случаев [4].
Опухоли поджелудочной железы при болезни Гиппеля—Линдау довольно редки и представлены нейроэндокринными поражениями, а также кистозными образованиями (простая киста, серозная цистаденома) [3].
Сочетание болезни Гиппеля—Линдау с эндокринными заболеваниями поджелудочной железы наблюдается в 5—10% случаев [2, 5, 6]. Как правило, это нейроэндокринные опухоли (NET), дисплазия островков Лангерганса и дуктулоинсулярные комплексы [7].
Эндокринные опухоли поджелудочной железы чаще всего светлоклеточные (60% наблюдений), с формированием солидных и железистых структур. При этом в строме опухоли определяются тонкостенные кровеносные сосуды с периваскулярными кровоизлияниями и пучками коллагеновых волокон [8, 9]. Данная гистологическая картина очень напоминает метастаз почечно-клеточной карциномы. Однако в отличие от почечно-клеточного рака также можно увидеть трабекулярные и гирляндоподобные структуры, характерные для эндокринных опухолей.
Иногда в нейроэндокринных образованиях поджелудочной железы, ассоциированных с VHL, определяются многовакуольные клетки с большим количеством липидов. В таких случаях данные образования имитируют перстневидно-клеточный рак особенно при пункционной биопсии поджелудочной железы [1, 10].
Иммуногистохимическое исследование в клетках NET выявляет положительную экспрессию хромогранина, А и синаптофизина [8]. 22% NET при болезни Гиппеля—Линдау негативны к хромогранину А, 17% — очагово-позитивны [6].
Известно, что 35% NET имеют очаговую реакцию к панкреатическим полипептидам, соматостатину, инсулину или глюкагону [9]. В отличие от синдрома множественных неоплазий 1-го типа важной особенностью является положительная реакция к ингибину [1]. Сильная коэкспрессия HIF-1-α, cyclinD1, CA9 и VEGF с отрицательной реакцией к инсулину и глюкагону позволяет отличить нормальные и опухолевые островки Лангерганса в случаях VHL [11].
При молекулярно-генетическом исследовании (флюоресцентная in situ гибридизация) определяется аллельная делеция 2-й копии VHL-гена [9].
Большинство нейроэндокринных опухолей поджелудочной железы при болезни Гиппеля—Линдау доброкачественны и имеют первую степень дифференцировки (2 митоза и менее на 10 HPF, индекс Ki-67 ≤2%). Вместе с тем для данной патологии существует 3 дополнительных критерия оценки потенциала злокачественности по Blansfield [3]:
1) размер опухоли 3 см и более в диаметре;
2) мутация в экзоне 3;
3) увеличение опухоли в размере в 2 раза и более за 500 дней.
Если данные критерии отсутствуют, больной с NET поджелудочной железы при VHL наблюдается каждые 2—3 года, при этом оперативное лечение не проводится. Если есть хотя бы один из указанных критериев, больной наблюдается каждые 6 мес — 1 год. При наличии 2 или 3 критериев необходима операция, так как есть риск малигнизации опухоли [3]. Некоторые авторы предлагают при размере образования 2 см в диаметре выполнять энуклеацию опухоли, при размере 3 см — резекцию поджелудочной железы, более 3 см в диаметре — панкреатодуоденальную резекцию [6].
В литературе встретился только один случай ассоциации болезни Гиппеля—Линдау с миелолипомой [12]. Известно, что эта доброкачественная опухоль неизвестной этиологии составляет 2,5% всех первичных опухолей надпочечника и, возможно, развивается в результате эндокринного дисбаланса [2, 13, 14]. В литературе описано 6 случаев сочетания миелолипомы с аденомой коры надпочечников [13, 14]. При этом опухоль состоит из двух клеточных элементов: светлых и эозинофильных клеток аденомы надпочечника, формирующих альвеолярные структуры. Среди этих клеток определяются участки хорошо отграниченной жировой ткани, смешанной с рассеянными островками элементов костного мозга эритробластами, клетками миелоидного и лимфоидного ряда [14]. Случаи сочетания миелолипомы и феохромоцитомы надпочечника в отечественной и зарубежной литературе нами не встретились.
Приводим собственное наблюдение нейроэндокринной опухоли поджелудочной железы и миелолипомы надпочечника, ассоциированной с VHL 2-го типа.
Больная 44 лет поступила в ФГБНУ «Российский научный центр хирургии им. акад. Б.В. Петровского» 14.05.15 с жалобами на сердцебиение, слабость, потливость, головокружение, затруднение дыхания.
В анамнезе дважды оперирована по поводу феохромоцитомы: в 1987 г. выполнена субтотальная адреналэктомия справа, в 1995 г. — субтотальная адреналэктомия слева. Гистологически оба раза была диагностирована доброкачественная феохромоцитома. Племянник больной оперирован по поводу двусторонней феохромоцитомы в возрасте 11 и 17 лет. Сын оперирован в марте 2015 г. также по поводу феохромоцитомы.
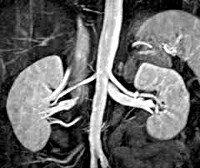
При компьютерном томографическом исследовании в январе 2014 г. у пациентки выявлены образования в проекции левого надпочечника и тела поджелудочной железы.
В июле 2014 г. в ФГБНУ «Российский научный центр хирургии им. акад. Б.В. Петровского» больной выполнена энуклеация опухоли головки поджелудочной железы с удалением образования забрюшинного пространства слева. Согласно протоколу операции, опухоль забрюшинного пространства 3 см в диаметре располагалась медиальнее левой почки, между нижним краем тела поджелудочной железы, левой почечной артерией и левой почечной веной. При интраоперационном УЗИ опухоль головки поджелудочной железы имела размер 1,5×1×1 см.
В марте 2015 г. выявлено новое образование в задних отделах головки поджелудочной железы. При УЗИ по заднемедиальному краю культи головки поджелудочной железы определялось гипоэхогенное слабо васкуляризированное образование размером 3,7×2 см с неровными контурами. ПЭТ-КТ в области резекции головки поджелудочной железы показала метаболически активное образование размером 2,6×2,2 см.
25.05.15 больной выполнена панкреатодуоденальная резекция. Во время операции при интраоперационном УЗИ в задненижних отделах головки поджелудочной железы обнаружено гипоэхогенное образование до 2 см в максимальном измерении.
При макроскопическом исследовании материала после первой операции образование поджелудочной железы было неправильной формы, бурого цвета, плотное, размером 2,5×1,5×1,3 см. Опухоль забрюшинного пространства (5×3×2 см) на разрезе имела вид ткани надпочечника с визуализацией коркового слоя в виде узкой полоски. В центральных отделах образование надпочечника было представлено тканью серо-розового цвета с очаговым кровоизлиянием. В материале после второй операции в головке поджелудочной железы выявлено четко отграниченное образование серовато-бурого цвета размером 1,8×1×1 см плотной консистенции.
При гистологическом исследовании опухоли поджелудочной железы в обоих случаях обнаружено инкапсулированное образование, состоящее из мономорфных клеток с хорошо развитой светлой цитоплазмой, образующих тубулярные, гирляндоподобные и трабекулярные структуры без митотической активности и признаков лимфоваскулярной инвазии (рис. 1, а). В некоторых участках клетки опухоли напоминали перстневидные или имели многовакуольную цитоплазму. В строме образования определялись пучки коллагеновых волокон с большим количеством кровеносных сосудов с тонкими стенками неправильной формы. В клетках опухоли отмечалась PAS-негативная реакция, при окраске по Гримелиусу очагово выявлялись аргирофильные гранулы.
 Рис. 1. Болезнь Гиппеля—Линдау. а — высокодифференцированная нейроэндокринная опухоль поджелудочной железы состоит из светлых клеток, формирующих тубулярные и трабекулярные структуры; б — доброкачественная феохромоцитома левого надпочечника, светлые клетки мозгового слоя с умеренным ядерным полиморфизмом формируют железистые и альвеолярные структуры; в, г — на фоне феохромоцитомы участки миелолипомы надпочечника, жировая ткань с островками клеток эритроидного, миелоидного и лимфоидного ряда; д — гемангиобластоподобные структуры среди клеток опухоли; е — клетки опухоли поджелудочной железы экспрессируют хромогранин А; а—д — окраска гематоксилином и эозином; е — иммуногистохимическое исследование; а, б, д, е — ×200; в — ×100; г — ×400.
Рис. 1. Болезнь Гиппеля—Линдау. а — высокодифференцированная нейроэндокринная опухоль поджелудочной железы состоит из светлых клеток, формирующих тубулярные и трабекулярные структуры; б — доброкачественная феохромоцитома левого надпочечника, светлые клетки мозгового слоя с умеренным ядерным полиморфизмом формируют железистые и альвеолярные структуры; в, г — на фоне феохромоцитомы участки миелолипомы надпочечника, жировая ткань с островками клеток эритроидного, миелоидного и лимфоидного ряда; д — гемангиобластоподобные структуры среди клеток опухоли; е — клетки опухоли поджелудочной железы экспрессируют хромогранин А; а—д — окраска гематоксилином и эозином; е — иммуногистохимическое исследование; а, б, д, е — ×200; в — ×100; г — ×400.
При гистологическом исследовании образования забрюшинного пространства выявлена ткань надпочечника с гиперплазией и узловой перестройкой коркового слоя. В мозговом слое обнаружено образование, состоящее из двух компонентов. Первый компонент представлен светлыми клетками, формирующими трабекулярные и альвеолярные структуры (см. рис. 1, б). Определялись участки с умеренным ядерным полиморфизмом. Второй компонент в виде вкраплений представлен жировой тканью, смешанной с рассеянными островками мегакариоцитов, клеток эритроидного, миелоидного и лимфоидного ряда (см. рис. 1, в, г). Фигуры митоза, некротические изменения и признаки капсулярной и васкулярной инвазии в образовании надпочечника не определялись.
На границе коркового и мозгового слоя надпочечника обнаружены гемангиобластоподобные структуры с большим количеством мелких кровеносных сосудов капиллярного типа и стромальными вакуолизированными клетками со светлой цитоплазмой (см. рис. 1, д).
Выполнено иммуногистохимическое исследование на срезах с парафиновых блоков в автоматическом режиме в иммуногистостейнере (Bond-Max, «Leica») cо следующими антителами: СК18 («Dako», клон DC10, RTU), CK19 («Dako», клон RCK108, разведение 1:100), хромогранин, А («Dako», клон DAK-A3, разведение 1:150), синаптофизин («Dako», клон SY38, разведение 1:100), CD56 («Leica», клон 564, RTU), RCC («Dako», клон SPM314, разведение 1:100), CD10 («Dako», клон SS2/36, разведение 1:100), Ki-67 («Dako», клон MIB-1, разведение 1:100). При иммуногистохимическом окрашивании клетки опухоли поджелудочной железы экспрессировали хромогранин А, синаптофизин, СD56, цитокератины 18-го и 19-го типов. Экспрессия СК19 указывала на высокую вероятность развития рецидива заболевания [5]. Наблюдалась отрицательная реакция с RCC и CD10. Индекс пролиферации Ki-67 составил менее 1%.
В светлоклеточном компоненте опухоли надпочечника отмечалась положительная реакция со следующими маркерами: хромогранином, А (см. рис. 1, е), синаптофизином, СD56, Ki-67 (менее 1%) и отрицательная реакция с RCC, CD10, СК18 и CK19.
Для хромосомного микроматричного анализа ткани опухоли поджелудочной железы из парафиновых блоков использована микроматрица Oncoscan («Affymetrix», США). Все этапы лабораторного исследования проведены в соответствии с протоколом производителя («Affymetrix», США). Анализ данных проводился с помощью программы ChAS, версия 3.0.
В результате исследования получен сигнал, соответствующий двум копиям гена VHL. Вне гена в исследуемом образце обнаружены множественные делеции и амплификации (рис. 2). Подобные профили были ранее описаны у пациентов с нейроэндокринными опухолями [15]. При этом делеций и амплификаций гена VHL обнаружено не было (рис. 3).
 Рис. 2. Делеции и амплификации в образце опухоли поджелудочной железы.
Рис. 2. Делеции и амплификации в образце опухоли поджелудочной железы.
 Рис. 3. Ген VHL. Анализ покрытия гена маркерами указывает на отсутствие делеций и амплификаций (стрелкой указана локализация гена на 3-й хромосоме).
Рис. 3. Ген VHL. Анализ покрытия гена маркерами указывает на отсутствие делеций и амплификаций (стрелкой указана локализация гена на 3-й хромосоме).
Белки, кодируемые геном VHL играют роль в кислородчувствительном пути, в стабильности и ориентации микротрубочек, супрессии опухоли, образовании ресничек, регуляции старения, цитокиновом сигнальном пути и сборке нормального внеклеточного фибронектинового матрикса [15].
С учетом клинических данных, результатов молекулярно-генетического исследования и иммунофенотипа было сделано заключение о болезни Гиппеля—Линдау 2-го типа с наличием высокодифференцированной опухоли поджелудочной железы, доброкачественной феохромоцитомы и миелолипомы надпочечника.
Сочетание болезни Гиппеля—Линдау с нейроэндокринной опухолью поджелудочной железы и миелолипомой надпочечника наблюдается крайне редко. Для постановки диагноза необходимо комплексное клинико-морфологическое и молекулярно-генетическое обследование. В плане дифференциальной диагностики обязательны оценка потенциала злокачественности образований, а также исключение метастаза почечно-клеточной карциномы или перстневидно-клеточного рака.
Конфликт интересов отсутствует.
Источник

Опухоли надпочечников – доброкачественные или злокачественные очаговые разрастания клеток надпочечников. Могут исходить из коркового или мозгового слоев, иметь разную гистологическую, морфологическую структуру и клинические проявления. Чаще проявляют себя приступообразно в виде адреналовых кризов: дрожание мышц, повышение АД, тахикардия, возбуждение, чувство страха смерти, боли в животе и груди, обильное отделение мочи. В дальнейшем возможно развитие сахарного диабета, нарушений работы почек, нарушение половых функций. Лечение всегда оперативное.
Общие сведения
Опухоли надпочечников – доброкачественные или злокачественные очаговые разрастания клеток надпочечников. Могут исходить из коркового или мозгового слоев, иметь разную гистологическую, морфологическую структуру и клинические проявления. Чаще проявляют себя приступообразно в виде адреналовых кризов: дрожание мышц, повышение АД, тахикардия, возбуждение, чувство страха смерти, боли в животе и груди, обильное отделение мочи. В дальнейшем возможно развитие сахарного диабета, нарушений работы почек, нарушение половых функций. Лечение всегда оперативное.

Опухоли надпочечников
Патанатомия
Надпочечники – сложные по гистологическому строению и гормональной функции эндокринные железы, образуемые двумя различными в морфологическом и эмбриологическом отношении слоями – наружным, корковым и внутренним, мозговым.
Корой надпочечников синтезируются различные стероидные гормоны:
- минералокортикоиды, участвующие в водно-солевом обмене (альдостерон, 18- оксикортикостерон, дезоксикортикостерон);
- глюкокортикоиды, участвующие в белково-углеводном обмене (кортикостерон, кортизол, 11- дегидрокортикостерон, 11- дезоксикортизол);
- андростероиды, обусловливающие развитие вторичных половых признаков по женскому (феминизация) или мужскому (вирилизация) типам (эстрогены, андрогены и прогестерон в небольших количествах).
Внутренним, мозговым слоем надпочечников вырабатываются катехоламины: дофамин, норадреналин и адреналин, служащие нейромедиаторами, передающими нервные импульсы, и влияющие на обменные процессы. При развитии опухолей надпочечников эндокринная патология определяется поражением того или иного слоя желез и особенностями действия избыточно секретируемого гормона.
Классификация
По локализации новообразования надпочечников делятся на две большие группы, принципиально отличающиеся друг от друга: опухоли коры надпочечников и опухоли мозгового вещества надпочечников. Опухоли наружного кортикального слоя надпочечников – альдостерома, кортикостерома, кортикоэстрома, андростерома и смешанные формы – наблюдаются достаточно редко. Из внутреннего мозгового слоя надпочечников исходят опухоли хромаффинной или нервной ткани: феохромоцитома (развивается чаще) и ганглионеврома. Опухоли надпочечников, исходящие из мозгового и коркового слоя, могут быть доброкачественными или злокачественными.
Доброкачественные новообразования надпочечников, как правило, небольших размеров, без выраженных клинических проявлений и являются случайными находками при обследовании. При злокачественных опухолях надпочечников наблюдается быстрое увеличение размеров новообразований и выраженные симптомы интоксикации. Встречаются первичные злокачественные опухоли надпочечников, исходящие из собственных элементов органа, и вторичные, метастазирующие из других локализаций.
Кроме того, первичные опухоли надпочечников могут быть гормонально-неактивными (инциденталомы или «клинически немые» опухоли) или продуцирующими в избытке какой-либо гормон надпочечника, т. е. гормонально-активными.
- Гормонально-неактивные новообразования надпочечников чаще доброкачественны (липома, фиброма, миома), с одинаковой частотой развиваются у женщин и мужчин любых возрастных групп, обычно сопутствуют течению ожирения, гипертензии, сахарного диабета. Реже встречаются злокачественные гормонально-неактивные опухоли надпочечников (меланома, тератома, пирогенный рак).
- Гормонально-активными опухолями коркового слоя надпочечников являются альдостерома, андростерома, кортикоэстрома и кортикостерома; мозгового слоя – феохромоцитома. По патофизиологическому критерию опухоли надпочечников подразделяются на:
- вызывающие нарушения водно-солевого обмена – альдостеромы;
- вызывающие метаболические нарушения – кортикостеромы;
- новообразования, оказывающие маскулинизирующее действие – андростеромы;
- новообразования, оказывающие феминизирующее действие – кортикоэстромы;
- новообразования со смешанной обменно-вирильной симптоматикой – кортикоандростеромы.
Наибольшее клиническое значение имеют гормоносекретирующие опухоли надпочечников.
Симптомы опухолей надпочечников
Опухоли надпочечников, протекающие без явлений гиперальдостеронизма, гиперкортицизма, феминизации или вирилизации, вегетативных кризов развиваются бессимптомно. Как правило, они выявляются случайно при выполнении МРТ, КТ почек или УЗИ брюшной полости и ретроперитонеального пространства, выполняемых по поводу других заболеваний.
Альдостерома
Продуцирующая альдостерон опухоль надпочечников, исходящая из клубочковой зоны коры и вызывающая развитие первичного альдостеронизма (синдрома Конна). Альдостерон осуществляет в организме регуляцию минерально-солевого обмена. Избыток альдостерона вызывает гипертензию, мышечную слабость, алкалоз (ощелачивание крови и тканей) и гипокалиемию. Альдостеромы могут быть одиночными (в 70-90% случаев) и множественными (10-15%), одно- или двусторонними. Злокачественные альдостеромы встречаются у 2-4% пациентов.
Альдостеромы проявляются тремя группами симптомов: сердечно-сосудистыми, почечными и нервно-мышечными. Отмечаются стойкая артериальная гипертензия, не поддающаяся гипотензивной терапии, головные боли, одышка, перебои в сердце, гипертрофия, а затем дистрофия миокарда. Стойкая гипертензия приводит к изменениям глазного дна (от ангиоспазма до ретинопатии, кровоизлияниям, дегенеративным изменениям и отеку диска зрительного нерва).
При резком выбросе альдостерона может развиваться криз, проявляющийся рвотой, сильнейшей головной болью, резкой миопатией, поверхностными дыхательными движениями, нарушением зрения, возможно – развитием вялого паралича или приступа тетании. Осложнениями криза могут служить острая коронарная недостаточность, инсульт. Почечные симптомы альдостеромы развиваются при резко выраженной гипокалиемии: появляются жажда, полиурия, никтурия, щелочная реакция мочи.
Нервно-мышечные проявления альдостеромы: мышечная слабость различной степени выраженности, парестезии и судороги – обусловлены гипокалиемией, развитием внутриклеточного ацидоза и дистрофией мышечной и нервной ткани. Бессимптомное течение альдостеромы встречается у 6-10 % пациентов с данным видом опухолей надпочечников.
Глюкостерома
Глюкостерома, или кортикостерома – продуцирующая глюкокортикоиды опухоль надпочечников, исходящая из пучковой зоны коры и вызывающая развитие синдрома Иценко-Кушинга (ожирения, артериальной гипертензии, раннего полового созревания у детей и раннего угасания половой функции у взрослых). Кортикостеромы могут иметь доброкачественное течение (аденомы) и злокачественное (аденокарциномы, кортикобластомы). Кортикостеромы – самые распространенные опухоли коры надпочечников.
Клиника кортикостеромы соответствует проявлениям гиперкортицизма (синдрома Иценко-Кушинга). Развивается ожирение по кушингоидному типу, гипертензия, головная боль, повышенная мышечная слабость и утомляемость, стероидный диабет, половая дисфункция. На животе, молочных железах, внутренних поверхностях бедер отмечается появление стрий и петехиальных кровоизлияний. У мужчин развиваются признаки феминизации – гинекомастия, гипоплазия яичек, снижение потенции; у женщин, напротив, признаки вирилизации – мужской тип оволосения, понижение тембра голоса, гипертрофия клитора.
Развивающийся остеопороз служит причиной компрессионного перелома тел позвонков. У четверти пациентов с данной опухолью надпочечников выявляется пиелонефрит и мочекаменная болезнь. Нередко отмечается нарушение психических функций: депрессия или возбуждение.
Кортикоэстерома
Продуцирующая эстрогены опухоль надпочечников, исходящая из пучковой и сетчатой зон коры и вызывающая развитие эстроген-генитального синдрома (феминизации и половой слабости у мужчин). Развивается редко, обычно у молодых мужчин, чаще носит злокачественный характер и выраженный экспансивный рост.
Проявления кортикоэстеромы у девочек связаны с ускорением физического и полового развития (увеличением наружных половых органов и молочных желез, оволосением лобка, ускорением роста и преждевременным созреванием скелета, влагалищными кровотечениями), у мальчиков – с задержкой полового развития. У взрослых мужчин развиваются признаки феминизации – двусторонняя гинекомастия, атрофия полового члена и яичек, отсутствие роста волос на лице, высокий тембр голоса, распределение жировых отложений на теле по женскому типу, олигоспермия, снижение или утрата потенции. У пациенток-женщин эта опухоль надпочечников симптоматически никак себя не проявляет и сопровождается только увеличением концентрации в крови эстрогенов. Чисто феминизирующие опухоли надпочечников довольно редки, чаще они носят смешанный характер.
Андростерома
Продуцирующая андрогены опухоль надпочечников, исходящая их сетчатой зоны коры или эктопической надпочечниковой ткани (забрюшинной жировой клетчатки, яичников, широкой связки матки, семенных канатиков и др.) и вызывающая развитие андроген-генитального синдрома (раннего полового созревания у мальчиков, псевдогермафродитизма у девочек, симптомов вирилизации у женщин). В половине случаев андростеромы злокачественны, метастазируют в легкие, печень, забрюшинные лимфоузлы. У женщин развивается в 2 раза чаще, обычно в возрастном диапазоне от 20 до 40 лет. Андростеромы являются редкой патологией и составляют от 1 до 3% всех опухолей.
Андростеромы, характеризующиеся избыточной продукцией андрогенов опухолевыми клетками (тестостерона, андростендиона, дегидроэпиандростерона и др.), вызывают развитие анаболического и вирильного синдрома. При андростероме у детей отмечается ускоренное физическое и половое развитие – быстрый рост и мышечное развитие, огрубение тембра голоса, появление угревой сыпи на туловище и лице. При развитии андростеромы у женщин появляются признаки вирилизации – прекращение менструаций, гирсутизм, снижение тембра голоса, гипотрофия матки и молочных желез, гипертрофия клитора, уменьшение подкожно-жирового слоя, повышение либидо. У мужчин проявления вирилизма выражены меньше, поэтому эти опухоли надпочечников часто являются случайными находками. Возможна секреция андростеромой и глюкокортикоидов, что проявляется клиникой гиперкортицизма.
Феохромоцитома
Продуцирующая катехоламины опухоль надпочечников, исходящая из хромаффинных клеток мозговой ткани надпочечников (в 90%) или нейроэндокринной системы (симпатических сплетений и ганглиев, солнечного сплетения и т. д.) и сопровождающаяся вегетативными кризами. Морфологически чаще феохромоцитома носит доброкачественное течение, ее озлокачествление наблюдается у 10% пациентов, обычно с вненадпочечниковой локализацией опухоли. Феохромоцитома встречается у женщин несколько чаще, преимущественно в возрасте от 30 до 50 лет. 10 % данного вида опухолей надпочечников носят семейный характер.
Развитие феохромоцитомы сопровождается опасными гемодинамическими нарушениями и может протекать в трех формах: пароксизмальной, постоянной и смешанной. Течение наиболее частой пароксизмальной формы (от 35 до 85%) проявляется внезапной, чрезмерно высокой артериальной гипертензией (до 300 и выше мм рт. ст.) с головокружением, головной болью, мраморностью или бледностью кожных покровов, сердцебиением, потливостью, загрудинными болями, рвотой, дрожью, чувством паники, полиурией, подъемом температуры тела. Приступ пароксизма провоцируется физическим напряжением, пальпацией опухоли, обильной едой, алкоголем, мочеиспусканием, стрессовыми ситуациями (травмами, операцией, родами и др.).
Пароксизмальный криз может длиться до нескольких часов, повторяемость кризов – от 1 в течение нескольких месяцев до нескольких в день. Криз прекращается быстро и внезапно, артериальное давление приходит к исходной величине, бледность сменяется покраснением кожных покровов, наблюдаются обильное потоотделение и секреция слюны. При постоянной форме феохромоцитомы отмечается стойко повышенное артериальное давление. При смешанной форме данной опухоли надпочечников феохромоцитомные кризы развиваются на фоне постоянной артериальной гипертензии.
Осложнения
Среди осложнений доброкачественных опухолей надпочечников встречается их малигнизация. Злокачественные опухоли надпочечников метастазируют в легкие, печень, кости. При тяжелом течении феохромоцитомный криз осложняется катехоламиновым шоком – неуправляемой гемодинамикой, беспорядочной сменой высоких и низких показателей АД, не поддающихся консервативной терапии. Катехоламиновый шок развивается в 10% случаев, чаще у пациентов детского возраста.
Диагностика
Современная эндокринология располагает такими методами диагностики, которые не только позволяют диагностировать опухоли надпочечника, но и устанавливать их вид и локализацию. Функциональная активность опухолей надпочечников определяется по содержанию в суточной моче альдостерона, свободного кортизола, катехоламинов, гомованилиновой и ванилилминдальной кислоты.
При подозрении на феохромоцитому и кризовых подъемах АД мочу и кровь на катехоламины забирают сразу после приступа или во время него. Специальные пробы при опухолях надпочечников предусматривают забор крови на гормоны до и после приема лекарств (проба с каптоприлом и др.) или измерение АД до и после приема препаратов (пробы с клонидином, тирамином и тропафеном).
Гормональную активность опухоли надпочечников можно оценить, используя селективную надпочечниковую флебографию – рентгенконтрастную катетеризацию надпочечниковых вен с последующим забором крови и определением в ней уровня гормонов. Исследование противопоказано при феохромоцитоме, т. к. может спровоцировать развитие криза. Размеры и локализацию опухоли надпочечников, наличие отдаленных метастазов оценивают по результатам УЗИ надпочечников, КТ или МРТ. Эти диагностические методы позволяют выявить опухоли- инциденталомы диаметром от 0,5 до 6 см.

КТ ОБП/ЗП. Аденомы обоих надпочечников.
Лечение опухолей надпочечников
Гормонально-активные опухоли надпочечников, а также новобразования диаметром более 3 см, не проявляющие функциональной активности, и опухоли с признаками малигнизации лечатся хирургически. В остальных случаях возможен динамический контроль за развитием опухоли надпочечника. Операции по поводу опухолей надпочечников проводятся из открытого или лапароскопического доступа. Удалению подлежит весь пораженный надпочечник (адреналэктомия – удаление надпочечника), а при злокачественной опухоли – надпочечник вместе с близрасположенными лимфоузлами.
Наибольшую сложность представляют операции при феохромоцитоме из-за большой вероятности развития тяжелых нарушений гемодинамики. В этих случаях уделяется большое внимание предоперационной подготовке пациента и выбору анестезиологического пособия, направленных на купирование феохромоцитомных кризов. При феохромоцитомах применяется также лечение с помощью внутривенного введения радиоактивного изотопа, вызывающего уменьшение в размерах опухоли надпочечника и имеющихся метастазов.
Лечение некоторых видов опухолей надпочечников хорошо поддается химиотерапии (митотаном). Купирование феохромоцитомного криза проводится внутривенной инфузией фентоламина, нитроглицерина, натрия нитропруссида. При невозможности купирования криза и развитии катехоламинового шока показана экстренная операция по жизненным показаниям. После оперативного удаления опухоли вместе с надпочечником врач-эндокринолог назначает постоянную заместительную терапию гомонами надпочечников.
Прогноз
Своевременное удаление доброкачественных опухолей надпочечников сопровождается благоприятным для жизни прогнозом. Однако после удаления андростеромы у пациентов нередко отмечается низкорослость. У половины пациентов, перенесших операцию по поводу феохромоцитомы, сохраняются умеренная тахикардия, гипертензия (постоянная или транзиторная), поддающиеся лекарственной коррекции. При удалении альдостеромы артериальное давление приходит в норму у 70% пациентов, в 30% случаев сохраняется умеренная гипертония, хорошо откликающаяся на гипотензивную терапию.
После удаления доброкачественной кортикостеромы регресс симптоматики отмечается уже через 1,5-2 мес.: изменяется внешность пациента, приходят в норму АД и обменные процессы, бледнеют стрии, нормализуется половая функция, исчезают проявления стероидного сахарного диабета, снижается масса тела, уменьшается и исчезает гирсутизм. Злокачественные опухоли надпочечников и их метастазирование прогностически крайне неблагоприятны.
Профилактика
Поскольку причины развития опухолей надпочечников до конца не установлены, профилактика сводится к предупреждению рецидивов удаленных опухолей и возможных осложнений. После адреналэктомии необходимы контрольные обследования пациентов эндокринологом 1 раз в 6 мес. с последующей коррекцией терапии в зависимости от самочувствия и результатов исследований.
Пациентам после адреналэктомии по поводу опухолей надпочечников противопоказаны физические и психические нагрузки, употребление снотворных средств и алкоголя.
Источник
