Октреотид в лечении рака поджелудочной железы
ЗАБОЛЕВАЕМОСТЬ
- Заболеваемость нейроэндокринными опухолями желудочно-кишечного тракта и поджелудочной железы составляет приблизительно 3-5 случаев на 100 000 человек в год.
- НЭО ЖКТ и ПЖ могут развиться в любом возрасте, но чаще после 50 лет.
- При выявлении глюкогоном, гастрином, ВИПом, соматостатином метастазы в регионарные лимфоузлы определяются у 60-80% больных.
- Пятилетняя выживаемость при карциноиде составляет, в среднем, 50-67%. Лучшая медиана выживаемости бывает при локализации опухоли в прямой кишке (88%), бронхе (74%) и аппендиксе (71%).
Клинико-патогенетическая характеристика основных НЭО
| Тип опухоли | Секретируемые гормоны или амины | Клиническая симптоматика |
| Карциноид | Серотонин | Карциноидный синдром: приливы, диарея, бронхоспазм, гипертензия, поражение сердца. |
| Гастринома | Гастрин | Синдром Золлингера-Эллисона, тяжелые пептические язвы |
| ВИПома | Вазоинтестинальный полипептид | Тяжелая диарея («панкреатическая холера», синдром Вернера-Моррисона) |
| Инсулинома | Инсулин | Гипогликемия |
| Глюкагонома | Глюкагон | Диабет, мигрирующая некротическая эритема, раздражение и покраснение языка |
| Соматостатинома | Соматостатин | Дисфункция желчного пузыря, ЖКБ, нарушенная толерантность к глюкозе |
КАРЦИНОИД
Одна из наиболее часто встречающихся опухолей диффузной нейроэндокринной системы!
Опухоль секретирует:
- серотонин
- брадикинин
- 5-гидрокситриптофан
- простагландины
- ВИП
- гистамин
Это приводит к развитию карциноидного синдрома.
КАРЦИНОИДНЫЙ СИНДРОМ
Проявления:
- приливы (63-94%). Внезапное появление глубокой красной или фиолетовой эритемы верхней части туловища, в основном лица и шеи. Сопровождается неприятным ощущением тепла, слезотечением, зудом, отеком лица и конъюнктивитом, саливацией и потоотделением, ощущением пульсации.
- диарея (68-84%)
- бронхоспазм (3-19%)
- одышка (3-19%)
- телеангиэктазии (25%)
- изменения сердца (11-53%)
- пеллагроподобный синдром с гиперкератозом и пигментацией (2-6%)
- поражение сердца – карциноидный кардиальный синдром (синдром Хедингера)выявляется более чем у 50% больных.
Синдром обусловлен развитием фиброзных изменений в эндо- и миокарде правых отделов сердца с поражением клапанов.
Характерны стеноз и недостаточность трехстворчатого клапана и клапана легочной артерии.
КАРЦИНОИДНЫЙ КРИЗ
- Может возникать спонтанно или провоцироваться стрессами, алкоголем, некоторой пищей (например, сыром), инъекциями катехоламинов.
- Первоначальные приступы длятся 2-5 минут, а в дальнейшем их продолжительность может увеличиваться до нескольких часов.
- Кризы чаще возникают при суточной экскреции 5-ГИУК более 200 мг и провоцируются стрессами, наркозом, биопсией или операцией, химиотерапией, давая высокую летальность.
КЛАССИФИКАЦИЯ НЭО (ВОЗ, 2002 г.)
- Высокодифференцированная нейроэндокринная опухоль (доброкачественная).
- Высокодифференцированная нейроэндокринная карцинома (низкой степени злокачественности).
- Низкодифференцированная нейроэндокринная карцинома (мелкоклеточная).
- Смешанная экзокринная и эндокринная карцинома.
- Опухолевоподобное поражение.
Характеристика высокодифференцированных НЭО
- низкий пролиферативный потенциал
- способность секретировать различные биологические вещества
- низкая чувствительность к химиотерапии.
К ним относятся различные карциноиды передней, средней и задней кишки, феохромоцитома, медуллярный рак щитовидной железы.
Характеристика низкодифференцированных НЭО
- высокозлокачественные опухоли с высоким пролиферативным потенциалом
- чувствительны к химиотерапии и лучевой терапии.
К ним относится мелкоклеточный рак легкого и других органов.
Характеристика смешанных экзокринных и эндокринных карцином
- к ним относятся различные опухоли поджелудочной железы (кроме карциноидов)
- чувствительность к химиотерапии данных опухолей умеренная.
КЛАССИФИКАЦИЯ КАРЦИНОИДНЫХ ОПУХОЛЕЙ (ВИЛЬЯМС И САНДЛЕР, 1963)
- Верхние (2-9%) (передняя кишка): опухоли дыхательных путей, тимуса, пищевода, желудка, двенадцатиперстной кишки, поджелудочной железы. Характерна низкая секреция серотонина, повышенная – гистамина и различных гормонов, атипичное течение карциноидного синдрома, частое метастазирование в кости.
- Средние (75-87%) (средняя кишка): опухоли тонкой кишки, аппендикса, слепой кишки, восходящего отдела ободочной кишки. Гиперсекреция серотонина и других вазоактивных субстанций, карциноидный синдром.
- Нижние (1-8%) (задняя кишка): опухоли поперечно-ободочной и нисходящей ободочной кишки, сигмовидной и прямой кишки. Карциноидный синдром не характерен, частое метастазирование в печень.
Классификация в зависимости от наличия или отсутствия карциноидного синдрома
- Гормонально-активные опухоли – характерна гиперсекреция гормонов. Клинические симптомы позволяют осуществить раннюю диагностику.
- Гормонально-неактивные опухоли(нет симптомов гиперсекреции гормонов) – до 50% нейроэндокринных опухолей. Клинически проявляются при большой опухолевой массе – на этом этапе опухоль метастазирует, а также может проявляться симптомами сдавления кишки.
ЛАБОРАТОРНАЯ ДИАГНОСТИКА
- Определение уровня серотонина и его метаболитов в моче. Наиболее распространенный тест – измерение экскреции 5-ГИУК (5-гидроксииндолуксусной кислоты) в суточной моче. Однако данный анализ может давать ложноположительные результаты в зависимости от характера употребляемой больными пищи (цитрусовые, бананы, ананасы, киви, орехи).
- Определение уровня хромогранина А в крови (повышение уровня хромогранина А наблюдают у 87-99% больных), норма – менее 4,5 ммоль/л. Этот плазменный маркер является самым достоверным при НЭО.
- Определение уровня экскреции нейронспецифической енолазы в крови.
ИНСТРУМЕНТАЛЬНАЯ ДИАГНОСТИКА
Рентгенологические методы
- рентгенография органов грудной клетки
- рентгенография пищевода и желудка
- ирригоскопия
Эндоскопические методы
- ЭГДС
- ректороманоскопия
- колоноскопия
- бронхоскопия
Ультразвуковые методы
- УЗИ
- Ультразвуковая допплерография сосудов
- Эндосонография
- Интраоперационное УЗИ
- Лапароскопическое УЗИ
Спиральная КТ с контрастным усилением и МРТ
РАДИОИЗОТОПНАЯ ДИАГНОСТИКА
- Сцинтиграфия костей скелета
- Сцинтиграфия с Октреотидом, меченным 111In
НЭО на поверхности клеток имеют рецепторы, обладающие высоким сродством к гормону соматостатину. В 87% случаев они присутствуют как в первичной опухоли, так и в метастазах. В связи с этим в последние годы для определения локализации опухоли и метастазов используется радиоизотопный метод с меченным 111In Октреотидом. Введенный внутривенно Октреотид, 111In через 24-48 ч. определяется на соматостатиновых рецепторах и позволяет визуализировать соматостатинпозитивную опухоль, а также определить возможность применения аналогов соматостатина для лечения.
Метод с применением Октреотида, 111In обладает чувствительностью 87%, специфичностью 75% и частотой совпадения диагнозов 87%.
Лечение
Хирургическое лечение
Основной метод лечения НЭО – хирургический. Возможные варианты оперативного вмешательства определяют по локализации опухоли, наличию или отсутствию метастазов и осложнений опухолевого процесса. Однако контроль симптомов при хирургическом лечении достигается не всегда!
Немедикаментозное лечение
Контроль за проявлениями карциноидного синдрома: исключение стрессов, алкоголя, соблюдение диеты.
Медикаментозное лечение
Биотерапия:
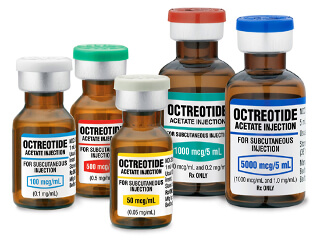
- синтетические аналоги соматостатина: раствор для инъекций Октреотид и лиофилизат для приготовления суспензии для внутримышечного введения пролонгированного действия Октреотид-депо.
- интерферон-?, пролонгированная форма ИНФ-? (PEG-интерферон).
Химиотерапия:
- монохимиотерапия: стрептозоцин, доксирубицин, фторурацил, дактиномицин, этопозид, цисплатин, дакарбазин.
- ПХТ: сочетания стрептозоцина, фторурацила и доксирубицина, цисплатина с этопозидом.
Комбинированная химиотерапия:
биотерапия + химиотерапия.
Симптоматическая терапия:
- гипотензивные препараты
- антигистаминные препараты
- диуретики
- бронходилататоры
- антидиарейные препараты.
Механизм действия ОКТРЕОТИДА-ДЕПО
- Препарат оказывает симптоматический эффект, понижая секрецию гормонов и пептидов, экскретируемых при випомах в 89%, при глюкоганомах в 75%, при инсулиномах в 65%.
- После применения Октреотида-депо при разных НЭО диарея прекращается у 40-60% больных.
- При ВИПомах Октреотид-депо полностью прекращает диарею в 38%случаев, еще у 38% больных значительно её уменьшает.
- Улучшает общее состояние в 75-85% случаев.
- Октреотид-депо контролирует гипогликемию при инсулиномах, некролитические кожные повреждения при глюкоганомах, что значительно улучшает качество жизни пациентов.
При карциноидных опухолях применение Октреотида-депо может приводить к уменьшению выраженности симптомов заболевания, в первую очередь, таких как приливы и диарея. Во многих случаях клиническое улучшение сопровождается снижением концентрации серотонина в плазме и экскреции 5-гидроксииндолуксусной кислоты с мочой.
При опухолях, характеризующихся гиперпродукцией вазоактивного интестинального пептида (ВИПомы), применение Октреотида-депо приводит у большинства больных к уменьшению тяжелой секреторной диареи, которая характерна для данного состояния, что, в свою очередь, приводит к улучшению качества жизни больного. Одновременно происходит уменьшение сопутствующих нарушений электролитного баланса, например, гипокалиемии, что позволяет отменить энтеральное и парентеральное введение жидкости и электролитов. По данным компьютерной томографии у некоторых больных происходит замедление или остановка прогрессирования опухоли, и даже уменьшение ее размеров, особенно метастазов в печень. Клиническое улучшение обычно сопровождается уменьшением (вплоть до нормальных значений) концентрации вазоактивного интестинального пептида (ВИП) в плазме.
При глюкагономах применение Октреотида-депо в большинстве случаев приводит к заметному уменьшению некротизирующей мигрирующей сыпи, которая характерна для данного состояния. У больных, страдающих диареей, Октреотид-депо вызывает ее уменьшение, что сопровождается повышением массы тела. При применении Октреотида-депо часто отмечается быстрое снижение концентрации глюкагона в плазме, однако при длительном лечении этот эффект не сохраняется. В то же время симптоматическое улучшение остается стабильным длительное время.
При гастриномах/синдроме Золлингера-Эллисона Октреотид-депо, применяемый в качестве монотерапии или в комбинации с блокаторами H2-рецепторов и ингибиторами протонного насоса, может снизить образование соляной кислоты в желудке и привести к клиническому улучшению, в т.ч. и в отношении диареи. Возможно также уменьшение выраженности и других симптомов, вероятно связанных с синтезом пептидов опухолью, в т.ч. приливов. В некоторых случаях отмечается снижение концентрации гастрина в плазме.
У больных с инсулиномами Октреотид-депо уменьшает уровень иммунореактивного инсулина в крови. У больных с операбельными опухолями Октреотид-депо может обеспечить восстановление и поддержание нормогликемии в предоперационном периоде. У больных с неоперабельными доброкачественными и злокачественными опухолями контроль гликемии может улучшаться и без одновременного продолжительного снижения уровня инсулина в крови.
У больных с редко встречающимися опухолями, гиперпродуцирующими рилизинг-фактор гормона роста (соматолибериномами), Октреотид-депо уменьшает выраженность симптомов акромегалии. Это, по-видимому, связано с подавлением секреции рилизинг-фактора гормона роста и самого гормона роста. В дальнейшем возможно уменьшение размеров гипофиза, которые до начала лечения были увеличены.
Обнаружено, что применение Октреотида-депо в дозах 30 мг и выше оказывает антипролиферативный эффект, связанный с прямым цитотоксическим действием препарата на опухоль при взаимодействии с соматостатиновыми рецепторами, а также с угнетением образования сосудов, питающих опухоль.
Режим дозирования
При эндокринных опухолях ЖКТ и поджелудочной железы для больных, у которых подкожное введение Октреотида обеспечивает адекватный контроль проявлений заболевания, рекомендуемая начальная доза Октреотида-депо составляет 20 мг каждые 4 недели.
Подкожное введение Октреотида следует продолжать еще в течение 2 недель после первого введения Октреотида-депо.
Для больных, не получавших ранее Октреотид подкожно, рекомендуется начинать лечение именно с подкожного введения Октреотида в дозе 0.1 мг 3 раза/сут. в течение относительно короткого периода времени (примерно 2 недели) с целью оценки его эффективности и общей переносимости. Только после этого назначают Октреотид-депо по вышеприведенной схеме.
В случае, когда терапия Октреотидом-депо в течение 3 мес. обеспечивает адекватный контроль клинических проявлений и биологических маркеров заболевания, возможно снизить дозу Октреотида-депо до 10 мг, назначаемых каждые 4 недели.
В тех случаях, когда после 3 мес. лечения Октреотидом-депо удалось достичь лишь частичного улучшения, дозу препарата можно увеличить до 30 мг каждые 4 недели.
На фоне лечения Октреотидом-депо в отдельные дни возможно усиление клинических проявлений, характерных для эндокринных опухолей ЖКТ и поджелудочной железы. В этих случаях рекомендуется дополнительное подкожное введение Октреотида в дозе, применявшейся до начала лечения Октреотидом-депо. Это может происходить, главным образом, в первые 2 мес. лечения.
Октреотид-депо – препарат первой линии для монотерапии или комбинированной терапии высокодифференцированных нейроэндокринных опухолей ЖКТ и поджелудочной железы, эффективно купирующий гормональные синдромы за счет подавления гиперсекреции гормонов этими опухолями, повышая качество жизни и выживаемость больных.
Источник

На сегодняшний день действенных и эффективных способов лечения воспаления поджелудочной железы не так и много. Обычно доктора прописывают «холод, голод и покой», подкрепляя эти рекомендации симптоматической терапией. Однако в начале 1970-х открыли соматостатин — нейропептид, распространенный в тканях центральной нервной системы и на периферии, правда, его изучение несколько затормозилось из-за быстрого периода полураспада.
Однако было выяснено, что данное вещество секретируется D-клетками островков Лангерганса поджелудочной железы и гипоталамусом, влияя на функции ряд других биологически активных веществ желудочно-кишечного тракта, выделение желчи. Октреотид — синтетический аналог соматостатина пролонгированного действия, разработанный специалистами фармакологической корпорации Sandoz. Он влияет на патогенетические механизмы развития острого панкреатита.
Влияние соматостатина на организм человека осуществляется при помощи пяти разновидностей специфических рецепторов. Их локализация и определяет перечень показаний к применению лекарственного препарата.
Соматостатические рецепторы находятся в нейроэндокринных опухолях, новообразованиях пищеварительного тракта и поджелудочной железы. Октреотид избирательно воздействует на соматостатические рецепторы второго и пятого типа и назначается пациентам с патологиями секреции гормона роста, опухолями и заболеваниями пищеварительного тракта другого генеза.
Основное действующее вещество Октреотида — синтетический аналог гормона соматостатина, действие которого продолжается дольше природного вещества. В организме данное соединение выполняет ряд важнейших функций.
Основными среди них служит регуляция секреции:
- релизинг — гормонов гипоталамуса и гипоталамуса: соматолиберина, влияющего на уровень пролактина и соматотропного гормона гипофиза, тиреотропного гормона, регулирующего активность щитовидной железы;
- серотонина, необходимого для нормальной работы центральной нервной системы и головного мозга;
- инсулина;
- глюкагона, влияющего на депонирование гликогена, функции миокарда, скелетной мускулатуры и других органов и тканей;
- гастрина, регулирующего секрецию желудочного сока и уровень рН;
- холецистокинина, который принимает участие в процессах пищеварения, специалисты также связывают его влияние с чувством страха, беспокойства и другими неврологическими нарушениями;
- вазоактивного интестинального пептида, влияющего на секрецию пищеварительных ферментов, кровоток и сокращение гладкомышечных стенок желудочно-кишечного тракта;
- инсулиноподобного фактора роста, который воздействует практически на все процессы, протекающие в организме человека.
Возможно только пероральное введение синтетических аналогов соматостатина.
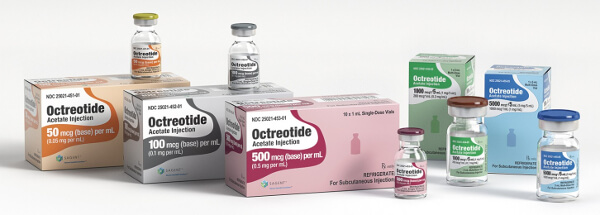
Поэтому препарат выпускается в виде:
- ампул с раствором, предназначенным для внутривенных инфузий и подкожных уколов с дозировкой действующего вещества 50, 100, 300, 600 мкг в 1 мл;
- лиофилизата и микросфер (порошка) для последующего разведения и приготовления суспензии, которая вводится внутримышечно.
В связи с ограниченным перечнем показаний к использованию и высоким риском осложнений, препарат отпускается из аптек только по рецепту врача.
При парентеральном применении Октреотид оказывает действие, сходное с естественным соматостатином. Однако в отличие от физиологического гормона, лекарственный препарат в большей степени влияет на выработку гормона роста и инсулиноподобного фактора роста. Но препарат мало воздействует на процессы синтеза инсулина.
В инструкции указано достаточно много показаний к применению Октреотида, однако при использовании в гастроэнтерологии препарат помогает справиться:
- с острым болевым синдромом;
- тошнотой;
- рвотой;
- расстройствами пищеварения;
- нарушениями стула;
- головокружением и слабостью;
- с тяжелыми осложнениями после операций на поджелудочной железе.
При назначении Октреотида пациентам с акромегалией это синтетическое производное соматостатина:
- устраняет мышечную, костную и неврологическую боль;
- снижает интенсивность головной боли;
- уменьшает частоту приступов головокружения;
- регулирует активность апокринных желез.
При злокачественных новообразованиях препарат:
- уменьшает размер опухоли;
- регулирует стул;
- нормализует перистальтику;
- восстанавливает показатели электролитного обмена;
- регулирует уровень рН в желудочно-кишечном тракте и выработку различных пищеварительных ферментов.
Кроме того, введение Октреотида останавливает и предупреждает повторные кровотечения у пациентов с варикозным расширением вен брюшной полости.
Особенности распределение препарата в организме человека подробно расписаны в инструкции по применению. Максимальная концентрация лекарственного средства в крови достигается быстро — спустя 20 — 30 минут как при подкожном, так и при внутривенном введении. Период полувыведения разнится — при уколе под кожу это время составляет до полутора часов, а при инфузии в вену — увеличивается. Метаболизм Октреотида осуществляется в почках, поэтому при тяжелых поражениях органа биодоступность препарата изменяется и возрастает риск передозировки.
Октреотид: дозировка, показания и ограничения к применению
Октреотид не относят к препаратам, которые есть в каждой домашней аптечке. Перечень показаний к его назначению достаточно ограничен, а введение лекарства должно происходить под медицинским наблюдением.
Если прописывается Октреотид, дозировка подбирается врачом в индивидуальном порядке.
Список показаний к использованию синтетического аналога соматостатина включает:
- Акромегалию. Заболевание характеризуется непропорциональным увеличением отдельных частей тела. Возникает вследствие изменения выработки соматотропного гормона из-за опухоли гипофиза. Помимо внешних признаков, патология проявляется и другими симптомами (частыми головными болями, неврологическими и эндокринными расстройствами). Без должного лечения повышает риск вторичных новообразований.
- Нейроэндокринные опухоли. Обычно локализованы на эпителиальной оболочке желудочно-кишечного и респираторного тракта. Встречаются редко — менее, чем у 1% пациентов. Октреотид эффективен для купирования карциноидного синдрома, который проявляется приливами жара, поносом, бронхоспазмом, тахикардией. Также препарат почти на 70% снижает риск разрастания опухоли и увеличивает продолжительность безрецидивного периода вдвое.
- Низидиобластоз. Врожденное разрастание выделяющих инсулин клеток Лангерганса поджелудочной железы, что вызывает постоянно повторяющиеся тяжелые гипогликемические кризы. Применение Октреотида позволяет избежать тотального удаления органа.
- Профилактику осложнений после операций на поджелудочной железе. В соответствии с данными 17 клинических исследований, введение препарата достоверно снижает выраженность нежелательных реакций после хирургического вмешательства и уменьшает период пребывания пациента на стационарном лечении. Препарат в обязательном порядке применяют при онкологических поражениях, в остальных случаях — по показаниям.
- Диарейный синдром. Возникает при синдроме иммунодефицита, патологиях желудочно-кишечного тракта и не поддается терапии антибактериальными и другими препаратами. Применение Октреотида позволяет избежать обезвоживания и прочих тяжелых последствий подобного состояния.
- Кишечную непроходимость. Иногда применяют для регуляции желудочной секреции при непроходимости, вызванной опухолями в полости кишечника.
- Кровотечение из варикозно-расширенных вен пищевода. По мнению специалистов, для купирования подобного состояния Октреотид более эффективен, чем другие, применявшиеся ранее, препараты.
- Поликистоз почек и печени. Средство уменьшает размер кистозных полостей. В результате функция этих органов в значительной степени восстанавливается.
- Ожирение. Октреотид эффективно помогает избавиться от избыточной массы тела, вызванной чрезмерной концентрацией инсулина. Если подобная проблемы спровоцирована другими проблемами, применение данного средства считают нецелесообразным.
Но в настоящее время Октреотид все чаще назначают пациентам с выраженным болевым синдромом при остром и хроническом панкреатите. Доказано, что помимо влияния на секрецию гормонов, ферментов и других биологически активных веществ, синтетический аналог соматостатина обладает противовоспалительной активностью, нормализует деятельность факторов местного клеточного иммунитета.
При назначении препарата Октреотид его дозировка подбирается индивидуально для каждого пациента. Впоследствии вводимое больному количество лекарства может корректироваться в зависимости от переносимости и оказываемого эффекта.
Начальная доза Октреотида составляет 50 мкг в сутки, раствор вводят подкожно или внутривенно. Кратность применения — 1 — 2 раза в сутки (при нейроэндокринных опухолях — трижды в день).
В среднем дозировка Октреотида составляет:
- при акромегалии — до 200 мкг в сутки, разделенные на два введения, если результат отсутствует через 12 недель, терапию прекращают;
- при злокачественных опухолях, начинают с 50 мкг дважды в сутки, затем дозировку постепенно повышают до 600 мг (по 200 мкг трижды в сутки), во время терапии контролируют состояние гормонального фона, при отсутствии эффекта лечение отменяют через 1 — 2 недели, при улучшении состояния дозу снижают до поддерживающей, которую подбирают индивидуально;
- при неконтролируемой диарее терапию начинают с высоких доз (100 — 250 мкг трижды в сутки), если улучшение не наступает, через 7 ней препарат отменяют;
- для профилактики осложнений в послеоперационном периоде при хирургическом вмешательстве на поджелудочной железе пациенту вводят 100 мкг Октреотида за час до операции, затем в таком же количестве трижды в день на протяжении недели;
- для остановки кровотечения из вен, окружающих пищевод, препарат вводят внутривенно со скоростью 25 мкг в час, терапию проводят как минимум на протяжении 5 дней, вопрос о продолжении лечения принимают в зависимости от состояния пациента.

При остром панкреатите назначают Октреотид с дозировкой действующего вещества 50 — 100 мг в сутки. Длительность терапии определяет врач в индивидуальном порядке.
Как правило, инъекции делают в условиях стационара. Однако при самостоятельном введении препарата необходимо обращать внимание на такие аспекты:
- перед применением раствора его осматривают на предмет наличия осадка, посторонних включений, помутнения;
- лиофилизат разводят непосредственно перед применением в соответствующем растворителе, при этом препарат можно вводить в течение ближайших суток, затем неизрасходованный раствор следует выбросить и развести новый;
- при подкожных инъекциях нельзя колоть в одно и то же место;
- флакон с готовым раствором Октреотида можно использовать в течение 2 недель после вскрытия при условии хранения в холодильнике (температурный диапазон 2 — 8ºС), но перед каждым использованием его проверяют на наличие посторонних включений.
Пациентам с выраженными расстройствами функции печени и почек, больным пожилого возраста может потребоваться коррекция дозировки лекарственного средства.
Нежелательные реакции на фоне применения Октреотида возникают достаточно часто. Многие пациенты предъявляют жалобы на:
- головные боли;
- головокружение;
- боли в эпигастральной области;
- тошноту и рвоту;
- расстройства стула, проявляющиеся в виде запоров, изменения оттенка и консистенции, отделяемого из прямой кишки;
- метеоризм и другие диспепсические явления;
- кожные аллергические реакции, прогрессирующая аллопеция.
В ходе лабораторных исследований на фоне применения Октреотида отмечают:
- изменения в биохимических показателях крови;
- повышение или наоборот, снижение уровня инсулина;
- нарушение функции щитовидной железы;
- повышение концентрации общего билирубина.
На УЗИ органов брюшной полости иногда наблюдают признаки формирования кристаллов и более крупных конкрементов в полости желчного пузыря.
При возникновении побочных эффектов необходимо как можно быстрее обратиться к врачу. Он принимает решение о целесообразности дальнейшего применения Октреотида.
Несмотря на высокий риск побочных реакций и системное влияние синтетического аналога соматостатина, перечень противопоказаний к применению препарата достаточно короткий. От его использования отказываются только в случае индивидуальной непереносимости. С осторожностью и под медицинским контролем средство вводят пациентам с желчекаменной болезнью и сахарным диабетом.
Октреотид при панкреатите: особенности применения у детей, беременных и кормящих женщин, аналоги
Клинический и практический опыт использования Октреотида при беременности и у детей ограничен. В соответствии с имеющимися данными, у большинства женщин введение препарата не вызывало каких-либо осложнений. Беременность заканчивалась благополучно, пороков развития плода не отмечали. Но у некоторых женщин использование Октреотида в первом триместре заканчивалось самопроизвольным выкидышем, но достоверной взаимосвязи между этими факторами не установлено. Также неизвестно, выделяется ли препарат с грудным молоком.

При беременности Октреотид назначают по строгим жизнеугрожающим показаниям. Грудное вскармливание рекомендуют приостановить. Клинический опыт применения препарата у детей и подростков отсутствует. Пожилым пациентам средство, как правило, прописывают в стандартной дозировке.
При превышении рекомендуемой дозы возможно:
- резкое повышение уровня глюкозы в крови;
- аритмия вплоть до остановки сердца;
- гипотензия;
- поражение печени и поджелудочной железы;
- острая гипоксия органов центральной нервной системы;
- диарея.
Специфическое лечение отсутствует. При появлении симптомов передозировки пациент подлежит госпитализации, проводят симптоматическую терапию.
При выписке рецепта на Октреотид, применяемый при панкреатите, доктор может указать один из аналогов препарата. Это:
- Генфаст (Канада);
- Октретекс (Россия);
- Октрид (Индия);
- Сандостатин (Швейцария);
- Серакстал (Италия).
В целом, Октреотид при панкреатите — средство экстренной терапии. Препарат не подходит для постоянного применения, а вводится при острой боли и других мучительных для пациентов симптомах. Дополнительно назначают антиферментные средства, при риске бактериальных осложнений — антибиотики, спазмолитики, анальгетики и другие медикаменты для нормализации функций предстательной железы и органов пищеварения. Обязательно соблюдение диеты с ограничением потребления жирной, острой и жаренной пищи, петрушки и другой зелени, прочих продуктов.
Источник
