Криодеструкция при раке поджелудочной железы

Специализация – лечение больных с опухолями печени и поджелудочной железы
Наша цель – радикальное лечение, максимальное увеличение продолжительности и повышение качества жизни больных.
В отделении опухолей печени и поджелудочной железы совершенствуются методики хирургического, комбинированного и комплексного лечения при различных локализациях злокачественных опухолей гепатопанкреатодуоденальной зоны, разрабатываются новые варианты уточненной диагностики и лечения. Создана научная школа онкологов-хирургов с широким диапазоном возможностей дальнейшего совершенствования методик онкохирургии. Многие ученики выходцы из нашего отделения работают ведущими специалистами, руководителями клиник в городах России и странах СНГ.
Большой научно-практический опыт отделения обобщен в более 400 научных публикациях. Подготовлено 7 докторов и более 30 кандидатов медицинских наук.
В хирургическом отделении опухолей печени и поджелудочной железы осуществляется научно-исследовательская работа по двум основным темам:
«Разработка мультидисциплинарного подхода к лечению злокачественных опухолей билиопанкреатодуоденальной зоны»: опухоли поджелудочной железы, опухоли 12-перстной кишки, опухоли большого дуоденального сосочка (фатеров сосок), опухоли желчных протоков (дистальные и проксимальные отделы желчных протоков, в том числе и опухоль Клатскина), опухоли желчного пузыря, возможные вторичные метастатические поражения вышеперечисленных органов.
«Разработка мультидисциплинарного подхода к лечению злокачественных опухолей печени»: первичный рак печени, метастатическое поражение печени (причем как метастазы колоректального рака, так и метастазы неколоректальных опухолей в печени).
Основными операциями на печени являются анатомические резекции печени как в объеме больших и предельно больших резекций (гемигепатэктомии, расширенные гемигепатэктомии), так и в объеме удаления одного или нескольких сегментов печени (сегментэктомии, бисегментэктомии).
Кроме того, выполняется локальное воздействие на опухолевый узел в печени (радиочастотная термоабляция или криодеструкция опухоли). Основными операциями на органах билиопанкреатодуоденальной области являются гастропанкреатодуоденальная резекция – ГПДР (при локализации опухоли в головке поджелудочной железы, фатеровом сосочке, 12-перстной кишке, дистальном отделе холедоха), дистальная субтотальная резекция поджелудочной железы (при локализации опухоли в теле и хвосте поджелудочной железы).
Кроме того приоритетными направлениями являются:
- Выполнение операций при множественном поражении печени.
- Выполнение операций при билобарном поражении печени, в том числе split-резекции.
- Выполнение одномоментных операций (резекция печени и резекция толстой кишки).
- Применение чрескожной и интраоперационной радиочастотной термоабляции опухолевых образований в печени.
- Применение криодеструкции опухолей в печени и поджелудочной железе.
- Применение новых схем адъювантной химиотерапии с учетом молекулярно-биологических маркеров.
- Применение предоперационной химиоэмболизации опухолей печени и поджелудочной железы.
- Выполнение расширенных ГПДР в новой модификации (лимфо- и невродиссекция).
- Выполнение операций на поджелудочной железе с резекцией магистральных сосудов
Источник
1. Давыдов М.И., Аксель Е.М. Статистика злокачественных новообразований в России и странах СНГ в 2009 г. Вестник ГУ РОНЦ им. Н.Н. Блохина РАМН. 2011; 22 (3): (85) (прил. 1): 172 с.
2. Напалков Н.П. Заболеваемость и смертность от рака основных локализаций (по материалам сборника ВОЗ “World Health 1995. Bridging the Gaps”). Диагностика и интервенционная радиология опухолей малого таза. Доклад на 23-м Европейском семинаре по диагностической и интервенционной радиологии. Обнинск, 1995 г. 8–9 октября. 35 с.
3. Чиссов В.И., Дарьялова С.Л. Онкология (клинические рекомендации). М.: ГЭОТАР-Медиа, 2006. 720 с.
4. Кубышкин В.А., Вишневский В.А. Рак поджелудочной железы. М.: Медпрактика-М, 2003. 386 с.
5. Xu K.C., Korpan N.N., Niu L.Z. Modern cryosurgery for cancer. World Scientific. 2012. 903 p.
6. Warshaw A.L., Castilo C.F. Pancreatic carcinoma. N. Engl. J. Med. 1992; 326 (7): 455–465.
7. Korpan N.N. Basics of cryosurgery. Wien, New York: ShringerVerlag, 2001. 325 p.
8. Прохоров Г.Г. Основы криохирургии (Обзор истории и со временного состояния проблемы). Международный сборник научных трудов под ред. д.м.н. В.И. Коченова “Медицинская криология”. Н. Новгород, 2008. Вып. 5. 408 с.
9. Альперович Б.И., Мерзликин Н.В., Комкова Т.Б. Криохирургические операции при заболеваниях печени и поджелудочной железы. Под ред. Альперовича Б.И. М.: ГЭОТАР-Медиа, 2015. 240 с.
10. Xu K.C., Niu L.Z., Hu Y.Z. A pilot study on combination of cryosurgery and 125iodine seed implantation for treatment of locally advanced pancreatic cancer. World J. Gastroenterol. 2008; 14: 1603–1611.
11. Кубышкин В.А., Ионкин Д.А., Кунгурцев С.В., Чжао А.В. История криохирургии. Хирургия. 2015; 5: 62–74.
12. Альперович Б.И. Исторический очерк криохирургии в России. Криохирургия в гепатологии. Достижения криомедицины. СПб.: Наука, 2001: 4–21.
13. Ханевич М.Д., Манихас Г.М. Криохирургия рака поджелудочной железы. СПб.: Аграф+, 2011. 228 с.
14. Ханевич М.Д., Вашкуров С.М., Семенов А.В., Анисимова А.В. Новые возможности криохирургии в онкологии. Сборник научных трудов 1-й Международной научно- практической конференции “Криохирургия. Современные методы и инновационные технологии”. СПб., 2007: 21–28.
15. Цыганов Д.И. Процессы и аппараты. М.: Сайнс-Прейс, 2011. 303 с.
16. Kovach S.J., Hendrickson R.J., Cappadona C.R. Cryoablation of unresectable cancer. Surgery. 2002; 131 (4): 463–464.
17. Prokhorov G., Prokhorov D., Andreev A. et al. Total body hypothermia in cryosurgery. In: Korpan N., ed. Basics of Cryosurgery. Wien: Springer, 2001. 324 p.
18. Чжао А.В., Ионкин Д.А., Степанова Ю.А., Шуракова А.Б. Криодеструкция рака поджелудочной железы. Высокотехно логическая медицина. 2016; 2: 4–11.
19. Ducreux M., Cuhna A.S., Caramella C., Hollebecque A., Burtin P., Goere D., Seufferlein T., Haustermans K., Van Laethem J.L., Conroy T., Arnold D. Cancer of the pancreas: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann. Oncol. 2015; (Suppl. 5): v56–v68. DOI: 10.1093/annonc/mdv295.
20. Chu K.F., Dupuy D.E. Thermal ablation of tumors: biological mechanisms and advances in therapy. Nat. Rev. Cancer. 2014; 14 (3): 199–208. DOI: 10.18632/oncotarget.
21. Gage A.A., Bauhst J. Mechanisms of tissue injury in cryosurgery. Cryobiology. 1998; 37 (3): 171–186.
22. Гранов А.М., Давыдов М.И. Интервенционная радиология в онкологии (Пути развития). Научно-практическое издание. СПб.: ФОЛИАНТ, 2013. 545 с.
23. Альперович Б.И., Комкова Т.Б., Мерзликин Н.В. Основы криохирургии печени и поджелудочной железы. Томск: Печатная мануфактура, 2006. 232 с.
24. Keogan M.T., Edelman R.R. Technologic advances in abdominal MR imaging. Radiol. 2001; 220 (2): 310–320.
25. Matsumoto R., Selig A.M., Colucci V.M., Jolesz F.A. MR monitoring during cryoterapy in the liver: predictability of histologic outcome. J. Magn. Reson. Imaging. 1993; 3 (5): 770–776.
26. Morrin M.M., Rofsky N.M. Techniques for liver MR imaging. Magn. Reson. Imaging Clin. N. Am. 2001; 9 (4): 75–96.
27. Чжао А.В., Земсков В.М., Козлова М.Н., Ионкин Д.А. Мониторинг иммунного статуса при криодеструкции злокачественных опухолей поджелудочной железы. Высокотехнологическая медицина. 2017; 4: 5–11.
28. Waitz R., Solomon S.B., Petre E.N., Trumble A.E., Fassò M., Norton L., Allison J.P. Potent induction of tumor immunity by combination tumor cryoablation with anti-CTLA-4 therapy. Cancer Res. 2012; 72 (2): 430–439. DOI: 10.1158/0008-5472.CAN-11-1782.
29. Sabel M.S., Nehs M.A., Su G., Lowler K.P., Ferrara J.L., Chang A.E. Immunologic response to cryoablation of breast cancer. Breast Cancer. Res. Treat. 2005; 90 (1): 97–104.
30. Korpan N.N. Cryosurgery: ultrastructural changes in pancreas tissue after low temperature exposure. Technol. Cancer Res. Treat. 2007; 6 (2): 59–67. DOI: 10.1177/153303460700600202.
Источник
отметить
статью
Ионкин Д. А., Карельская Н. А., Степанова Ю. А., Земсков В. М., Козлова М. Н., Жаворонкова О. А., Чжао А. В.
Ионкин Дмитрий Анатольевич – канд. мед. наук, старший научный сотрудник отделения хирургии печени и поджелудочной железы ФГБУ “НМИЦ хирургии им. А.В. Вишневского”, ГБУ “НМИЦ хирургии имени А.В. Вишневского” Минздрава России, ionkin@ixv.ru, 117997, г. Москва, ул. Б. Серпуховская, д. 27, Российская Федерация
Карельская Наталья Александровна – канд. мед. наук, старший научный сотрудник отделения рентгенологии и магнитно-резонансных исследований с кабинетом ультразвуковой диагностики ФГБУ “НМИЦ хирургии им. А.В. Вишневского”, ГБУ “НМИЦ хирургии имени А.В. Вишневского” Минздрава России, 117997, г. Москва, ул. Б. Серпуховская, д. 27, Российская Федерация
Степанова Юлия Александровна – доктор мед. наук, старший научный сотрудник научно-организационного отдела ФГБУ “НМИЦ хирургии им. А.В. Вишневского”; профессор кафедры лучевой диагностики ИПО ФГАОУ ВО “Первый МГМУ им. И.М. Сеченова”, ГБУ “НМИЦ хирургии имени А.В. Вишневского” Минздрава России; ФГАОУ ВО Первый МГМУ имени И.М. Сеченова Минздрава России, 117997, г. Москва, ул. Б. Серпуховская, д. 27, Российская Федерация
Земсков Владимир Михайлович – доктор мед. наук, профессор, руководитель группы клинической иммунологии ФГБУ “НМИЦ хирургии им. А.В. Вишневского”, ГБУ “НМИЦ хирургии имени А.В. Вишневского” Минздрава России, 117997, г. Москва, ул. Б. Серпуховская, д. 27, Российская Федерация
Козлова Мария Николаевна – канд. мед. наук, старший научный сотрудник группы клинической иммунологии ФГБУ “НМИЦ хирургии им. А.В. Вишневского”, ГБУ “НМИЦ хирургии имени А.В. Вишневского” Минздрава России, 117997, г. Москва, ул. Б. Серпуховская, д. 27, Российская Федерация
Жаворонкова Ольга Александровна – канд. мед. наук, старший научный сотрудник отделения рентгенологии и магнитно-резонансных исследований с кабинетом ультразвуковой диагностики ФГБУ “НМИЦ хирургии им. А.В. Вишневского”, ГБУ “НМИЦ хирургии имени А.В. Вишневского” Минздрава России, 117997, г. Москва, ул. Б. Серпуховская, д. 27, Российская Федерация
Чжао Але
Цель. Улучшить качество и увеличить продолжительность жизни больных местнораспространенным раком поджелудочной железы. Материал и методы. С 2012 г. криодеструкция лапаротомным доступом была выполнена 36 больным местнораспространенным раком поджелудочной железы. Мужчин было 14 (38,9%), женщин – 22 (61,1%), средний возраст больных – 58 ± 6,8 года. Размер опухолей поджелудочной железы варьировал от 4 до 10 см. Применяли отечественные установки “Крио-МТ”, “КРИО-01” (ЕЛАМЕД), криоаппликаторы 2-5 см. Целевая температура составляла -186 °С, время экспозиции – 3-5 мин. Число сеансов зависело от размера опухоли и варьировало от 1 до 5 (в среднем 2,4). Локальная криодеструкция была дополнена формированием обходных анастомозов в 18 (50%) наблюдениях. Всем больным в дальнейшем проведена адъювантная химиотерапия, в 10 наблюдениях дополненная регионарной химиоэмболизацией. Результаты. Летальных исходов во время криодеструкции и в послеоперационном периоде не было. В ближайшем послеоперационном периоде осложнения отмечены у 14 (38,8%) больных, тяжелые осложнения – у 13,6%. После криодеструкции происходило полное исчезновение болевого синдрома (39,2%) либо значительное его уменьшение (41,6%). Выживаемость больных через 6, 12, 24, 36 мес составила соответственно 92, 84, 48 и 14%, медиана выживаемости – 18,2 мес. Заключение. Криодеструкция при местнораспространенном раке поджелудочной железы является вмешательством, в значительной степени улучшающим качество жизни онкологических пациентов, в первую очередь за счет уменьшения болевого синдрома. В сочетании с химиотерапевтическим лечением отмечено и некоторое увеличение выживаемости.
Ключевые слова:
поджелудочная железа, рак, криохирургия, криодеструкция, осложнения, отдаленные результаты, pancreas, cancer, cryosurgery, cryodestruction, complications, long-term results
Литература:
1.Давыдов М.И., Аксель Е.М. Статистика злокачественных новообразований в России и странах СНГ в 2009 г. Вестник ГУ РОНЦ им. Н.Н. Блохина РАМН. 2011; 22 (3): (85) (прил. 1): 172 с.
2.Напалков Н.П. Заболеваемость и смертность от рака основных локализаций (по материалам сборника ВОЗ “World Health 1995. Bridging the Gaps”). Диагностика и интервенционная радиология опухолей малого таза. Доклад на 23-м Европейском семинаре по диагностической и интервенционной радиологии. Обнинск, 1995 г. 8-9 октября. 35 с.
3.Чиссов В.И., Дарьялова С.Л. Онкология (клинические рекомендации). М.: ГЭОТАР-Медиа, 2006. 720 с.
4.Кубышкин В.А., Вишневский В.А. Рак поджелудочной железы. М.: Медпрактика-М, 2003. 386 с.
5.Xu K.C., Korpan N.N., Niu L.Z. Modern cryosurgery for cancer. World Scientific. 2012. 903 p.
6.Warshaw A.L., Castilo C.F. Pancreatic carcinoma. N. Engl. J. Med. 1992; 326 (7): 455-465.
7.Korpan N.N. Basics of cryosurgery. Wien, New York: Shringer-Verlag, 2001. 325 p.
8.Прохоров Г.Г. Основы криохирургии (Обзор истории и со временного состояния проблемы). Международный сборник научных трудов под ред. д.м.н. В.И. Коченова “Медицинская криология”. Н. Новгород, 2008. Вып. 5. 408 с.
9.Альперович Б.И., Мерзликин Н.В., Комкова Т.Б. Криохирургические операции при заболеваниях печени и поджелудочной железы. Под ред. Альперовича Б.И. М.: ГЭОТАР-Медиа, 2015. 240 с.
10.Xu K.C., Niu L.Z., Hu Y.Z. A pilot study on combination of cryosurgery and 125iodine seed implantation for treatment of locally advanced pancreatic cancer. World J. Gastroenterol. 2008; 14: 1603-1611.
11.Кубышкин В.А., Ионкин Д.А., Кунгурцев С.В., Чжао А.В. История криохирургии. Хирургия. 2015; 5: 62-74.
12.Альперович Б.И. Исторический очерк криохирургии в России. Криохирургия в гепатологии. Достижения криомедицины. СПб.: Наука, 2001: 4-21.
13.Ханевич М.Д., Манихас Г.М. Криохирургия рака поджелудочной железы. СПб.: Аграф+, 2011. 228 с.
14.Ханевич М.Д., Вашкуров С.М., Семенов А.В., Анисимова А.В. Новые возможности криохирургии в онкологии. Сборник научных трудов 1-й Международной научно-практической конференции “Криохирургия. Современные методы и инновационные технологии”. СПб., 2007: 21-28.
15.Цыганов Д.И. Процессы и аппараты. М.: Сайнс-Прейс, 2011. 303 с.
16.Kovach S.J., Hendrickson R.J., Cappadona C.R. Cryoablation of unresectable cancer. Surgery. 2002; 131 (4): 463-464.
17.Prokhorov G., Prokhorov D., Andreev A. et al. Total body hypothermia in cryosurgery. In: Korpan N., ed. Basics of Cryosurgery. Wien: Springer, 2001. 324 p.
18.Чжао А.В., Ионкин Д.А., Степанова Ю.А., Шуракова А.Б. Криодеструкция рака поджелудочной железы. Высокотехно логическая медицина. 2016; 2: 4-11.
19.Ducreux M., Cuhna A.S., Caramella C., Hollebecque A., Burtin P., Goere D., Seufferlein T., Haustermans K., Van Laethem J.L., Conroy T., Arnold D. Cancer of the pancreas: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann. Oncol. 2015; (Suppl. 5): v56-v68. DOI: 10.1093/annonc/mdv295.
20.Chu K.F., Dupuy D.E. Thermal ablation of tumors: biological mechanisms and advances in therapy. Nat. Rev. Cancer. 2014; 14 (3): 199-208. DOI: 10.18632/oncotarget.
21.Gage A.A., Bauhst J. Mechanisms of tissue injury in cryosurgery. Cryobiology. 1998; 37 (3): 171-186.
22.Гранов А.М., Давыдов М.И. Интервенционная радиология в онкологии (Пути развития). Научно-практическое издание. СПб.: ФОЛИАНТ, 2013. 545 с.
23.Альперович Б.И., Комкова Т.Б., Мерзликин Н.В. Основы криохирургии печени и поджелудочной железы. Томск: Печатная мануфактура, 2006. 232 с.
24.Keogan M.T., Edelman R.R. Technologic advances in abdominal MR imaging. Radiol. 2001; 220 (2): 310-320.
25.Matsumoto R., Selig A.M., Colucci V.M., Jolesz F.A. MR monitoring during cryoterapy in the liver: predictability of histologic outcome. J. Magn. Reson. Imaging. 1993; 3 (5): 770-776.
26.Morrin M.M., Rofsky N.M. Techniques for liver MR imaging. Magn. Reson. Imaging Clin. N. Am. 2001; 9 (4): 75-96.
27.Чжао А.В., Земсков В.М., Козлова М.Н., Ионкин Д.А. Мониторинг иммунного статуса при криодеструкции злокачественных опухолей поджелудочной железы. Высокотехнологическая медицина. 2017; 4: 5-11.
28.Waitz R., Solomon S.B., Petre E.N., Trumble A.E., Fassò M., Norton L., Allison J.P. Potent induction of tumor immunity by combination tumor cryoablation with anti-CTLA-4 therapy. Cancer Res. 2012; 72 (2): 430-439. DOI: 10.1158/0008-5472.CAN-11-1782.
29.Sabel M.S., Nehs M.A., Su G., Lowler K.P., Ferrara J.L., Chang A.E. Immunologic response to cryoablation of breast cancer. Breast Cancer. Res. Treat. 2005; 90 (1): 97-104.
30.Korpan N.N. Cryosurgery: ultrastructural changes in pancreas tissue after low temperature exposure. Technol. Cancer Res. Treat. 2007; 6 (2): 59-67. DOI: 10.1177/153303460700600202.
Cryoablation for locally advanced pancreatic cancer
Ionkin D. A., Karelskaya N. A., Stepanova Y. A., Zemskov V. M., Kozlova M. N., Zhavoronkova O. A., Chzhao A. V.
Aim. To improve quality and duration of life in patients with locally advanced pancreatic cancer. Material and methods. Cryosurgery through laparotomy has been performed in 36 patients with locally advanced pancreatic cancer since 2012. There were 14 (38.9%) men and 22 (61.1%) women (mean age 58 ± 6.8 years). Dimensions of pancreatic tumors were from 4 to 10 cm. Domestic devices “CRYO-MT”, “CRYO-01”, “ELAMED” and cryoapplicators with a diameter 2-5 cm were applied. Target temperature was about 186 °C, time of exposure – 3-5 min. There were 1-5 sessions of cryoablation (mean 2.4) and their number depended on tumor dimensions. Local cryodestruction was supplemented by bypass anastomoses in 18 patients (50%). All patients subsequently underwent adjuvant chemotherapy with additional regional chemoembolization in 10 of them. Results. There were no lethal outcomes during cryodestruction and in postoperative period. Early postoperative complications occurred in 14 (38.8%) patients, severe complications – in 13.6%. Cryodestruction was followed by complete regression (39.2%) or significant improvement (41.6%) of pain syndrome. 6-, 12-, 24- and 36-month survival was 92%, 84%, 48% and 14%, respectively. Median survival was 18.2 months. Conclusion. Cryodestruction is able to improve patients’ quality of life due to reduced pain syndrome in case of locally advanced pancreatic cancer. Certain increase of survival was observed in additional chemotherapy.
Keywords:
поджелудочная железа, рак, криохирургия, криодеструкция, осложнения, отдаленные результаты, pancreas, cancer, cryosurgery, cryodestruction, complications, long-term results
Источник
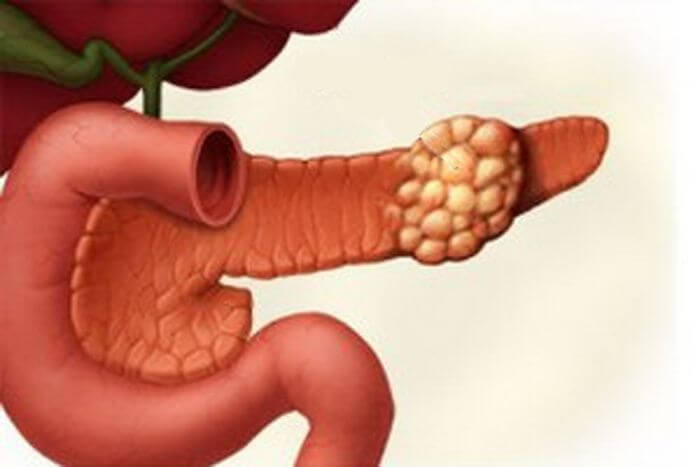
Опухоль поджелудочной железы симптомы и лечение. По своему происхождению новообразования в поджелудочной железе бывают доброкачественными или злокачественными.
Часто их выявляют после инструментального обследования других органов. На УЗИ однозначно вид опухоли не определить. При подозрении на новообразование в поджелудочной железе нужно обратиться к врачу, который назначит дополнительное всестороннее обследование.
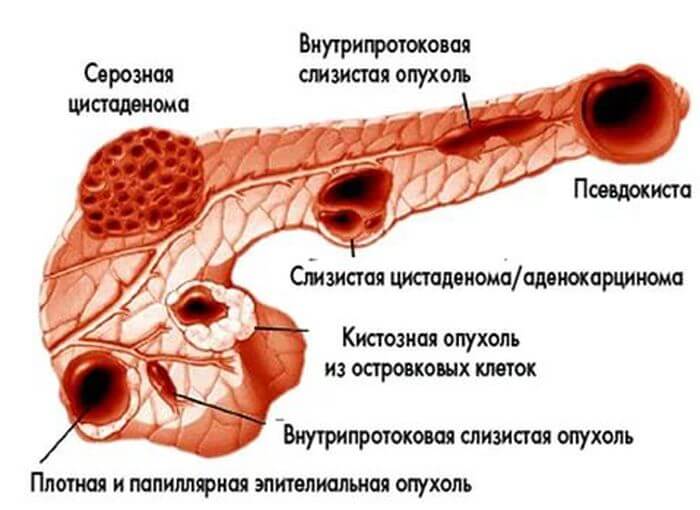
Классификация опухолей
Новообразование в поджелудочной железе разделяются:
По локализации — месту возникновения в структуре железы:
- головка;
- тело;
- хвост;
- островки Лангерганса;
- протоки.
Гистологическому строению определяется, из каких клеток образовалась опухоль:
- эпителиальное происхождение;
- железистой паренхимы;
- из островкового эпителия;
- неэпителиального генеза;
- дизонтогенетические.
Функциональным нарушениям – состояние, связанное с изменением регуляции в организме: гормональной или нервной. Орган остается неповрежденным, но деятельность поджелудочной железы нарушается.
Симптомы
Развитие опухоли до поры протекает без видимых симптомов. Когда она разрастается и возможно прорастает в близлежащие органы: желудок, тогда появляются типичные симптомы, с которыми доктор знаком. По симптомам он назначает всестороннее обследование.
Злокачественная опухоль поджелудочной железы проявляет свои симптомы при значительном разрастании:
Закупорка протоков
Закупорке протоков (обтюрация) – появляется при сдавливании образованием органов, которые нарушают свое функционирование, и проявляется болями, свидетельствующими о том, что новообразование просочилось сквозь нервные окончания. У каждого пациент симптомы проявляются индивидуально и зависят от места возникновения.
Опухоль головки поджелудочной железы провоцирует боль в правом подреберье. Опухоль хвоста поджелудочной железы вызывает дискомфорт и боль в левом подреберье. Если образованием охвачено тело поджелудочной железы, то боль проявляется вкруговую, опоясывающая.
Боль сильно увеличивается при несоблюдении диеты, а также лежа на спине. Сдавливание органов приводит к закупорке желчных протоков, проявляющееся в оттоке желчи из печени в кишечник. Результатом становится механическая желтуха. У нее свои симптомы:
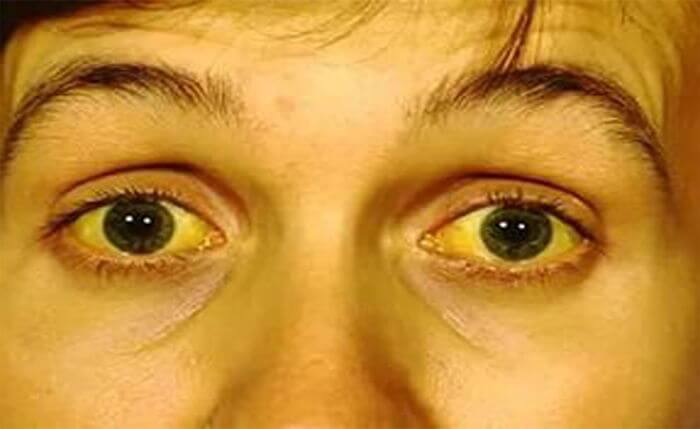
- желтушное окрашивание кожи, склер или слизистых оболочек;
- обесцвечивание стула;
- потемнение мочи;
- изменение размера печени и желчного пузыря в сторону увеличения;
- возникновение кожного зуда.
Рак поражает близлежащие органы, из которых может, в любой момент открыться кровотечение.
Интоксикация
Интоксикация организма. Ее признаки часто путают с признаками заболеваний и отклонений в ЖКТ. Симптомы похожи, но действие на организм интоксикации значительно тяжелее:
- резкое снижение веса;
- потеря аппетита;
- вялость, немощь, апатия;
- повышение температуры.
Доброкачественная опухоль поджелудочной железы позволяет классифицировать симптоматику 2 видов:
Ранняя стадия имеет бессимптомное течение, и приобретает их в процессе роста:
- боли вверху живота, подреберьях, правом или левом, отдающая в спину, усиливающаяся по ночам;
- дискомфорт и боль после приема пищи;
- постепенная потеря веса;
- тошнота, снижение аппетита, немощь и потеря трудоспособности.
Поздняя стадия – проявляется симптомами, как и при злокачественной опухоли. Помимо перечисленных выше, симптомов вызывает страх и нервные расстройства, повышает потоотделение. Симптомы могут возникать постепенно или внезапно. И они отличаются, завися от типа доброкачественного образования.
Риски возникновения
Точной причины появления раковых клеток нет. Но опухолевый процесс имеет свои факторы риска, о которых многие знают. Среди них:
- Вредные привычки: алкоголь, курение.
- Генная предрасположенность.
- Неправильное питание.
- Панкреатит.
- Неблагоприятная экологическая обстановка.
Диагностика
Всесторонне обследование пациента, используя различные методы исследования, позволит выяснить тяжесть опухоли: очаги, размеры, действие на соседние органы, метастазирование.
Обследование поможет определиться с методикой лечения:
- УЗИ. Позволяет увидеть новообразование, очаг его распространения.
- Компьютерная томография с введением контрастного вещества выявит не только очаги опухоли, но и метастазы, если они есть.
- Рентгенологические методы: А) Рентгенография определяет последствия прорастания опухоли на желудок и двенадцатиперстную кишку, сдавливание органов, диффузия слизистых оболочек, снижение моторики. В) Релаксационная дуоденография определяет локализацию опухоли и последствия ее разрастания. С) Ирригография выявляет дефекты в поперечно-ободочной кишке в результате прорастания опухоли.
- Эндоскопическая ретроградная холангиопанкреатография позволяет осмотреть желчную и панкреатическую системы с целью выявления их поражений. Взять материал для биопсии из неблагополучных очагов.
- Эндоскопический ультразвук. За счет технического оснащения: эндоскоп, видеокамера, ультразвуковой датчик, возможно, исследовать новообразование, введя инструменты через кишку. Такое исследование позволяет выявить новообразование на ранних стадиях.
- Рентгенохирургическая диагностика с контрастом позволяет выявить причины механической желтухи и смещение артерий.
- Радионуклидное исследование позволяет выявить закупорку общего с поджелудочной железой желчного протока.
- Нашумевший спорный тестер Джека Андраки, основан на анализе крови или мочи, используя специальную бумагу.
Главное в диагностике — установка медицинского диагноза на основании интерпретация полученных результатов исследования и анализов, формирование экспертного заключения.
Лечение
Необходимое лечение подбирается доктором на основании диагностики и анализов.
Хирургическая терапия всегда показана при обнаружении доброкачественного образования. Исследование гистологии со срезов образования позволит точно установить была ли она доброкачественной. Основные операции по удалению новообразований:
- Резекция состоит в удалении части поджелудочной железы, чаще в ее хвосте.
- Удаление непосредственно образования способом вылущивания. Выполняются для опухолей, которые продуцируют гормоны: доброкачественная инсулома.
- Панкреатодуоденальная резекция производится в случае размещения образования на головке железы. Оно удаляется вместе с 12-перстной кишкой.
- Селективная артериальная эмболизация закупоривает сосуд, на котором растет образование с целью отключить подпитку кровоснабжением. Используется при гемангиоме.
Химиотерапия
Химиотерапия призвана лечить злокачественное образование при помощи токсинов и ядов, которые называются химиопрепаратом. Она бывает: предоперационной, послеоперационной, профилактической, лечебной.
Поскольку раковые клетки бесконечно делятся, то химиотерапия циклично повторяется в расчете с клеточным циклом деления. Процедура состоит из капельного введения препарат или приёмом таблеток.
Наружная радиотерапия, являющаяся разновидностью терапии лучевой. Суть излечения — бомбардирование зоны новообразования излучением от медицинского ускорителя в виде пучка элементарных частиц. Проводится сеансами через фиксированный промежуток времени. Показания к применению:
- Сокращение размера опухоли на поджелудочной железе перед хирургическим вмешательством.
- Локально-возникшем раке поджелудочной железы.
- Уменьшение страданий при метастазах.
- Предотвращение рецидивов рака после хирургической операции.
Симптоматическая терапия направлена на снятие болей и облегчения страданий умирающего пациента: гормональная терапия – это лечение с помощью применения гормонов, способных тормозить рост рака. Продлевает продолжительность жизни.
Виротерапия применяет онкотропные или онколитические вирусы в терапевтических целях, мобилизуя против злокачественных клеток естественные защитные силы иммунной системы организма.
Нанонож как необратимая электропорация, разрушающая раковые клетки путем воздействия на них электрическим полем большой интенсивности локализовано. Для этого применяется специальный аппарат — нанонож.
В настоящее время слывет одним из самых результативных способов уничтожения опухоли в поджелудочной железе. Факт возможности повторения процедуры важное обстоятельство для повторного проведения при рецидивах или неоперабельном раке.
Шансы на выздоровление или жизнь после оперативного лечения
Сама операция на поджелудочной железе мало опасна. Прогноз оптимистичней при ранних сроках выполнения операции. Полностью выздоравливают пациенты с доброкачественными опухолями: глюкагономы, инсуломы, гастриномы и их разновидности
Рак поджелудочной железы имеет печальную статистику:
- На операцию поступают пациенты, у которых отсутствуют множественные метастазы, А это, как правило, лишь 15% больных. Для 85 % предоставляются виды лечения, направленные на продление жизни.
- Смертность на операционном столе у одного пациента из 6.
- Продолжительность жизни до 5 лет у каждого десятого больного после хирургического вмешательства, у остальных меньше.
После оперативного лечения возможны осложнения в функционировании организма. Любая операция влечет приспособление организма к потере органа или его части. Если орган жизненно важен, то адаптация проходит тяжелее. У пациентов после удаления опухоли поджелудочной железы, симптомы и лечение влекут 2 проблемы: сбои при пищеварении, снижение инсулина в организме.
Решаются проблемы дефицита путем назначения медикаментозных препаратов. При сопутствующих удалениях частей близлежащих органов: желудка, селезенки, двенадцатиперстной кишки врач посоветует надлежащую терапию и диету.
Профилактика
Поскольку ученые неутомимо работают над вопросом изучения причин, дающих толчок развитию рака, а ответа на них нет со 100 % достоверностью, поэтому руководства во избежание заболевания нет.
Лучший способ профилактики исключить знакомые всем факторы риска. Быть внимательным к себе при проявлениях болей в месте расположения железы. Не откладывать визит к доктору и хотя бы поверхностное обследование УЗИ.
Опухоль поджелудочной железы симптомы и лечение животрепещущая тема для многих страдающих заболеванием.
Источник
