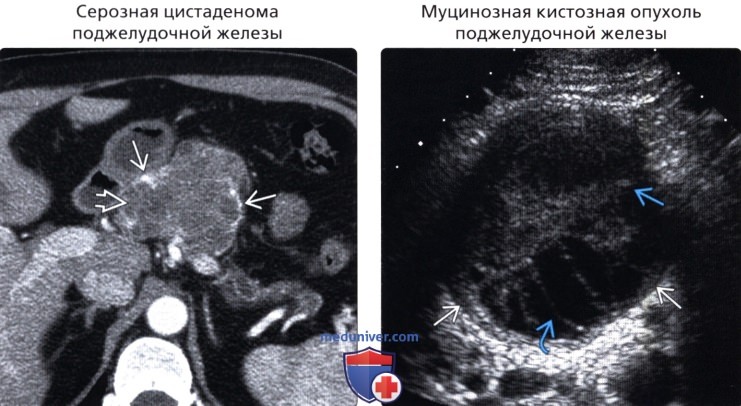
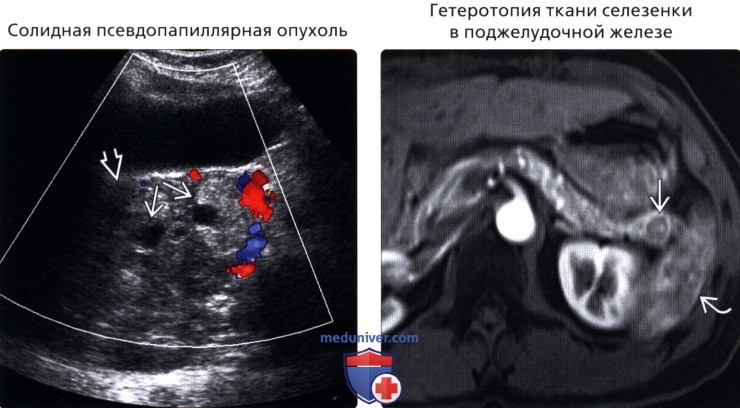
Дифференциальная диагностика образований поджелудочной железы
Что такое протоковая аденокарцинома поджелудочной железы? Это один из самых грозных и распространенных видов рака поджелудочной железы. Дифференициальная диагностика в деле установления этого диагноза крайне важна, так как она позволяет прогнозировать течение заболевания и его прогноз, «перспективность» выполнения тяжелых оперативных вмешательств, и течение послеоперационного периода.
Чем более дифференцированный рак – тем легче дифференциальная диагностика. Злокачественные опухоли низкой и средней степени дифференцировки имеют низкий градиент плотности с окружающей паренхимой при оценке изображений в артериальную и венозную фазы контрастного усиления, и могут стать причиной ошибок.
Что делать, если диагностика выявила солидное образование в поджелудочной железе? Если поразмыслить и рассуждать объективно, то любое солидное образование в этом органе – это показание к хирургическому вмешательству. Воздержаться от операции (на время) можно лишь при ряде кистозных опухолей. Любая солидная опухоль – будь она даже доброкачественной – имеет тенденцию к малигнизации, и чем скорее она будет удалена, тем большая вероятность высокого уровня выживаемости пациента.
Возможны ли ошибки при диагностике протоковой аденокарциномы? Опухоль Франца (в отечественной литературе мы знаем её как солидно-псевдопапиллярную опухоль), пока она небольших размеров, имеет нечеткие контуры и гиподенсную структуру, а это значит, что может быть расценена как протоковая аденокарцинома.
Будет ли от этого хуже больному? Вероятнее всего нет, если только не сравнивать качество жизни в послеоперационном периоде с периодом, когда ведется мониторинг за ростом солидно-псевдопапиллярной опухоли. Чем СППО больше, тем более выражен в ней распад и ее легче дифференцировать.
Нейроэндокринная опухоль – если она гормонально активная – может быть гиперконтрастной. Но если она не гормональноактивная – то тогда она может быть умеренно гиподенсной и требует дифференциальной диагностики. Ошибки интерпретации данных приводят к тому же результату, что и при СППО. Нейроэндокринные опухоли, увы, озлокачествляются, а значит, и объем резекции потребуется соответствующий.
Метастазы в поджелудочной железе, как правило, гиперваскулярны, и их чаще дифференцируют с нейроэндокринными опухолями, а не с аденокарциномой.
«Головная боль» врачей-рентгенологов – это хронический индуративный панкреатит. Он может иметь «пятнистую» картину при контрастном усилении и подчас очень трудно отличим от рака. Однако тяжелые формы хронического панкреатита лечат, по сути, так же, как и протоковую аденокарциному. И если быть совсем уж объективным, самое страшное – не заметить опухоль на фоне хронического воспаления. Потому что если воспаление можно «мониторировать», то опухоль необходимо удалять.
О других солидных опухолях поджелудочной железы можно прочитать здесь.
Автор: Кармазановский Григорий, руководитель отделения лучевой диагностики ФГУ «Институт хирургии им. А.В. Вишневского» Минздравсоцразвития, член европейского общества радиологии (ECR), член-корреспондент Североамериканского радиологического общества (RSNA), член президиума Российской Ассоциации Радиологов (РАР).
Источник
УЗИ при солидном образовании поджелудочной железыа) Дифференциальная диагностика солидного образования поджелудочной железы: 1. Распространенные заболевания: 2. Менее распространенные заболевания:
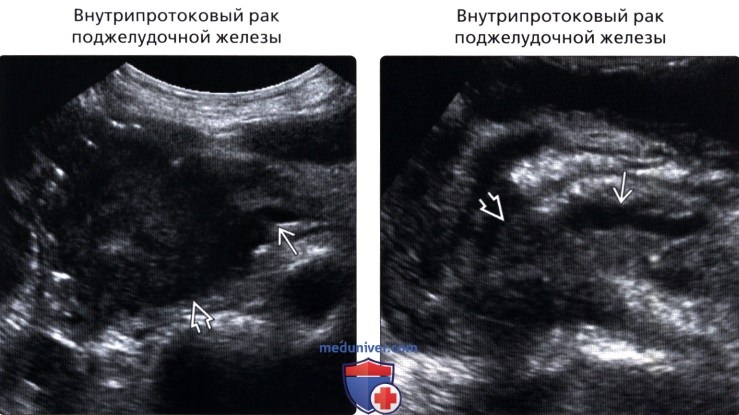
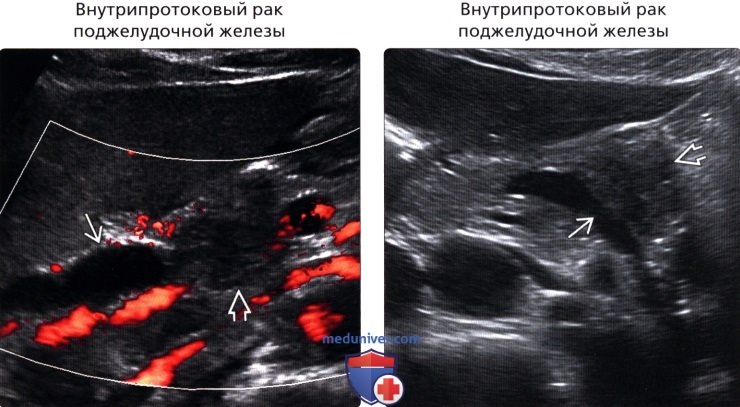
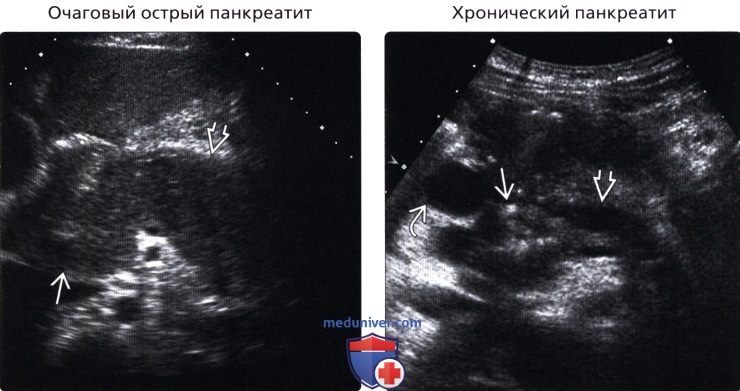
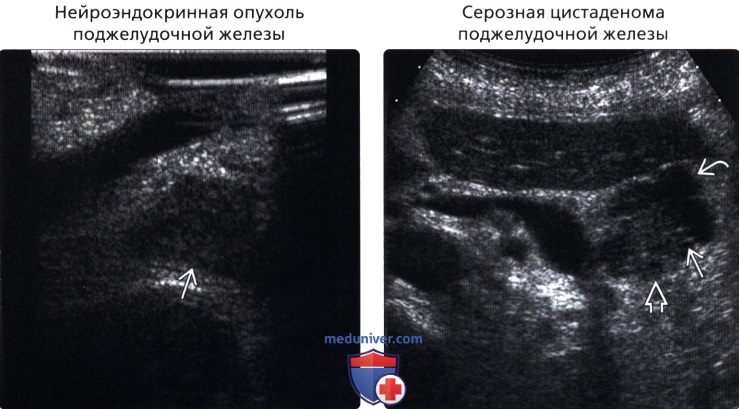
б) Важная информация: 1. Дифференциальная диагностика: 2. Распространенные заболевания: • Внутрипротоковая карцинома поджелудочной железы: • Очаговый острый панкреатит: • Хронический панкреатит: • Нейроэндокринная опухоль поджелудочной железы: • Серозная цистаденома поджелудочной железы: • Муцинозная кистозная опухоль поджелудочной железы:
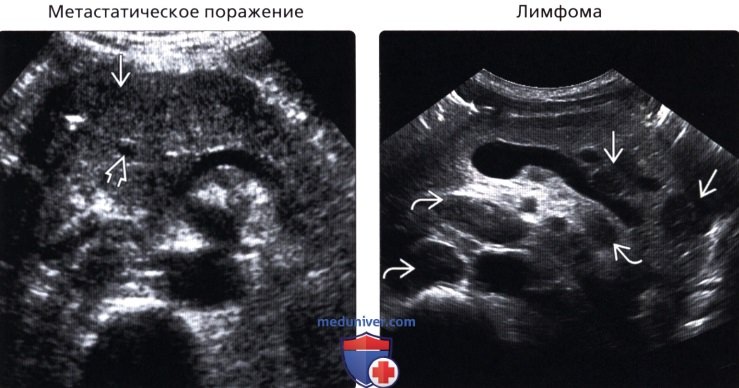
3. Менее распространенные заболевания: • Метастатические поражения: • Лимфома: • Солидная псевдопапиллярная опухоль: • Гетеротопия ткани селезенки в поджелудочную железу: в) Список использованной литературы: – Также рекомендуем “УЗИ при расширении протока поджелудочной железы” Редактор: Искандер Милевски. Дата публикации: 10.12.2019 |
Источник
Е.А. Дубцова, Л.В. Винокурова, К.А. Никольская, М.А. Агафонов
Центральный НИИ гастроэнтерологии Московского клинического научного центра, Москва
В статье обсуждаются трудности дифференциальной диагностики хронических заболеваний поджелудочной железы (ПЖ) с раком ПЖ, приводятся характерные клинические наблюдения. Указывается роль применения препаратов ферментов ПЖ у пациентов с хроническим заболеванием ПЖ.
Ключевые слова: поджелудочная железа, хроническое заболевание, рак, дифференциальная диагностика.
Сведения об авторах:
Дубцова Елена Анатольевна – д.м.н., ЦНИИ гастроэнтерологии, Москва
Винокурова Людмила Васильевна – д.м.н., ЦНИИ гастроэнтерологии, Москва
Diseases of the Pancreas – Difficulty of Differential Diagnosis
E.A. Dubtsova, L.V. Vinokurova, K.A. Nikolskaya, M.A. Agafonov
Central Science and Research Institute for Gastroenterology of Moscow State Clinical Science Center, Moscow
The paper discusses difficulties in differential diagnostics of chronic pancreatic disease and pancreatic cancer; it presents relevant clinical cases. The role of pancreatic enzymes preparations in patients with chronic pancreatic disease is highlighted.
Keywords: pancreas, chronic disease, cancer, differential diagnosis.
===
Одним из основных вопросов диагностики заболеваний поджелудочной железы (ПЖ) остается определение их принадлежности к злокачественному или доброкачественному процессу и решение вопроса о необходимости радикального лечения при раке ПЖ и адекватности проведения оперативного вмешательства при хроническом панкреатите (ХП). Дифференциальная диагностика ХП и рака ПЖ является одной из наиболее сложных клинических проблем. Рак ПЖ занимает одно из ведущих мест в заболеваемости и смертности среди онкологических заболеваний органов пищеварения в большинстве развитых стран. К факторам риска рака ПЖ относят употребление в пищу большого количества жиров, курение, ХП, сахарный диабет. По литературным данным, риск возникновения рака ПЖ при ХП в 20 раз, а при наследственном – в 60 раз выше, чем в популяции [1–6]. По сводным данным зарубежных и отечественных авторов, рак ПЖ чаще выявляется на терминальной стадии, при этом в момент диагностирования заболевания резектабельность опухоли не превышает 10–15%, а у остальных 85–90% пациентов выявляется нерезектабельная опухоль или отдаленные метастазы [7, 8].
Наиболее важными диагностическими методами визуализации является мультиспиральная компьютерная томография (МСКТ), магнитно-резонансная томография (МРТ), ультразвуковое исследование (УЗИ) брюшной полости и эндоскопическая ультрасонография (ЭУС) [2, 9, 10].
В последнее десятилетие достаточно много публикаций посвящено диагностике аутоиммунного панкреатита (АИП). Особенности клинической картины этого заболевания схожи с таковой при раке ПЖ, что требует проведения дифференциальной диагностики между этими заболеваниями. Установление правильного диагноза принципиально важно, так как АИП, в отличие от рака ПЖ – процесс обратимый, а лечение может быть эффективным при применении стероидных препаратов. Имеются публикации ретроспективных исследований, где у больных АИП были выполнены панкреатодуоденальные резекции в связи с подозрением на новообразование ПЖ. В США, например, ретроспективно, по результатам гистологических исследований после резекции ПЖ, АИП выявлен в 10–11% случаев [11, 12].
Приведем два клинических примера.
Клинический пример 1.
Больной С., 62 лет, заболел за 3 месяца до госпитализации. Появилась резкая слабость, желтуха, снижение массы тела на 10 кг за 3 мес.
УЗИ брюшной полости от 14.05.14 – увеличение и диффузные изменения печени. Билиарная гипертензия. Выявлено утолщение стенок долевых протоков, общего, пузырного протоков, билиарный сладж в ОЖП. признаки хронического холецистита и полип желчного пузыря. Отмечено увеличение лимфатических узлов по ходу гепато-дуоденальной связки. Необходимо провести дифференциальную диагностику между аутоиммунным панкреатитом и отеком поджелудочной железы на фоне новообразования головки ПЖ.
В биохимическом анализе крови от 14.05.14 г – повышение уровня АСТ – 212,4 Ед/л, ГГТП – 1800 Ед/л, ЩФ – 602,2 Ед/л, СРБ – 12.9; Ig G4 – 14.5 (норма: 0.08 – 1.4) г/л, СА 19-9 – 265 Ед/мл.
По результатам ЭУС выявлено диффузное поражение поджелудочной железы (аутоиммуного? опухолевого? генеза). Образование головки поджелудочной железы необходимо верифицировать по результатам морфологического исследования. Билиарная гипертензия (до 15 мм). Утолщение стенок гепатикохоледоха (до 3,5 мм), пузырного протока, желчного пузыря. Билиарный сладж. Увеличение парапанкреатических лимфатических узлов и лимфатических узлов по ходу гепатодуоденальной связки до 26×18мм, 20×11 мм (рис. 1). МСКТ – опухоль панкреатической части холедоха. Билиарная гипертензия (рис. 2).
Цитологическое исследование: мелкие кусочки ткани поджелудочной железы с картиной хронического индуративного панкреатита. Элементов опухоли не найдено.
Проводился дифференциальный диагноз между аутоиммунным панкреатитом и опухолью панкреатической части холедоха. В пользу аутоиммунного панкреатита: повышение IgG4 в 10 раз, отсутствие морфологических признаков опухоли по результатам пункционной биопсии поджелудочной железы. В пользу опухоли повышение онкомаркеров СА 19-9 до 265, заключение МСКТ.
Учитывая значительное повышение IgG4, решено провести курс консервативной терапии. Больному были назначены: омепразол 40 мг/сут., панкреатин в мини-таблетках (Пангрол) 50000 Ед/сут (по 10000 Ед с каждым приемом пищи), а также курс преднизолона в дозе 0,6 мг/кг/сут в течение 3 недель под контролем глюкозы крови с последующим снижением дозы до 5–10 мг в сутки. С целью уменьшения явлений холестаза была назначена урсодезоксихолевая кислота 1000 мг/сут.
Спустя 6 недель планировалось оценить состояние поджелудочной железы по данным визуализации. При отсутствии положительной динамики в виде уменьшения объема образования головки поджелудочной железы решить вопрос об оперативном лечении.
На фоне лечения отмечается положительная динамика в виде снижения АСТ с 212,4 Ед/л до нормы, нормализация уровня билирубина, снижение ГГТП с 1800 Ед/л до 175,2 Ед/л, щелочной фосфатазы с 602,2 Ед/л до 125,7 Ед/л, уменьшение СОЭ с 90 до 25 мм/ч. Отмечается снижение IgG4с 14,5 до 1,7 г/л и онкомаркеров СА 19-9 с 265 до 137 Ед/мл.
В течение дальнейших трех месяцев больной продолжал принимать преднизолон в поддерживающей дозе (10 мг/сут), препарат урсодезоксихолевой кислоты 1000 мг/сут и полиферментную терапию (Пангрол – 50000 Ед/сут). Результатом проводимой терапии была нормализация уровня всех онкомаркеров и биохимических показателей. Сохранялось повышение ГГТП (227 Ед/л), щелочной фосфатазы (174,2 Ед/л) и умеренное повышение IgG4 до 2,5 г/л. Слабость прошла, боли не беспокоят, больной прибавил в массе тела, он остается под наблюдением в МКНЦ.
Подбор доз панкреатических ферментов больным ХП проводится индивидуально. В данном случае у больного не было тяжелого нарушения внешнесекреторной функции поджелудочной железы, поэтому была назначена стандартная доза препарата Пангрол 50000 Ед в сутки.
Описанным клиническим случаем хотелось бы продемонстрировать сложности дифференциальной диагностики аутоиммунного панкреатита и рака поджелудочной железы.
Недооценка тяжести патологии, как и гипердиагностика могут привести к выбору неправильной тактики ведения больных – динамическое наблюдение за больными, которым показано оперативное лечение либо их медикаментозное лечение при недиагностированном опухолевом процессе.
Клинический пример 2.
Больной Ж., 55 лет, жалобы на постоянные боли в верхней половине живота с иррадиацией в спину, интенсивность которых усиливается после приема пищи.
Из анамнеза: начало болей в верхней половине живота после алкогольного эксцесса; боли продолжаются несколько месяцев; снижение массы тела на 15 кг в течение нескольких месяцев.
Уровень ферментов ПЖ в крови в пределах нормы, билирубин – 39,6 (прямой – 19,8) мкмоль/л, ГГТП – 1101,3 Ед/л, ЩФ – 615,8 Ед/л, АСТ – 188,3 Ед/л, АЛТ – 518,1 Ед/л; С-реактивный протеин – 3,53, глюкоза – 5,6 ммоль/л.
Выявлено повышение онкомаркеров: СА 19-9 – 152,0, СА 242 – 78,2, РЭА – 74,3 Ед/мл.
По данным УЗИ брюшной полости, увеличение головки поджелудочной железы за счет объемного образования в ней. Вирсунгов проток 3,2 мм в диаметре.
Эндоскопическая ультрасонография – расширение общего желчного протока (ОЖП) и главного панкреатического протока (ГПП). Хронический панкреатит. Необходимо дифференцировать очаговое образование головки поджелудочной железы и псевдотуморозную форму панкреатита (рис. 3).
Дважды проводилась тонкоигольная пункция ПЖ, по результатам которой атипичные клетки не выявлены (рис.4).
Дифференциальный диагноз проводился между двумя нозологиями: хронический панкреатит с преимущественным поражением головки поджелудочной железы и опухолью головки поджелудочной железы.
В пользу последнего свидетельствует:
– отрицательная динамика СА 19-9 в течение месяца: с 152 до 220 Ед/мл;
– отсутствие воспалительных изменений в крови (СРБ и лейкоциты в пределах нормы);
– отсутствует положительная динамика размеров образования головки ПЖ на фоне длительной консервативной терапии.
У больного имелся стойкий болевой синдром и подозрение на опухоль ПЖ по результатам визуализации, без морфологического подтверждения диагноза, что явилось показанием к хирургическому лечению. Больному была проведена панкреатодуоденальная резекция. Результаты гистологического и цитологического исследования операционного материала показали наличие аденокарциномы (рис. 5).
После проведенной резекции поджелудочной железы больные нуждаются в ферментозаместительной терапии, в зависимости от объема операции и степени внешнесекреторной недостаточности поджелудочной железы.
Степень внешнесекреторной недостаточности ПЖ можно определить по уровню эластазы кала. В норме уровень эластазы-1 в кале составляет 200–500 мкг/г кала и более. Экзокринная недостаточность средней и легкой степени 100–200 мкг/г, тяжелой степени – менее 100 мкг/г.
К экзокринной недостаточности, помимо резекции ПЖ, может приводить длительно протекающий и осложненный кистами и кальцинатами хронический панкреатит. Больным, перенесшим резекцию ПЖ, и больным, страдающим хроническим панкреатитом с экзокринной недостаточностью ПЖ, показан постоянный прием средних и высоких доз высокоэффективных капсулированных ферментных препаратов.
Одним из таких препаратов является Пангрол – современный капсулированный препарат панкреатина, произведенный по инновационной запатентованной технологии. Капсулы содержат мини-таблетки одного размера, покрытые кишечнорастворимой и функциональной мембраной для контролируемого высвобождения липазы. Одинаковый размер мини таблеток способствует их равномерному перемешиванию с пищей и оптимальному распространению ферментов. Кислотоустойчивая оболочка мини-таблеток способствует защите от агрессивных факторов в желудке и началу активации ферментов только в кишечнике. Пангрол назначается по 20000–50000 Ед 3 раза в день, во время каждого приема пищи. При необходимости, а именно – при тяжелой экзокринной недостаточности, доза препарата может быть увеличена до 150000–200000 Ед/сут. Критерием адекватно подобранной дозы служит уменьшение таких клинических проявлений внешнесекреторной недостаточности поджелудочной железы как диарея, стеаторея, метеоризм, снижение массы тела. Препарат Пангрол может быть рекомендован пациентам с различной степенью выраженности внешнесекреторной недостаточности как врачом гастроэнтерологом, так и врачом- терапевтом поликлинического звена, потому что чаще всего такие пациенты находятся под наблюдением участкового-терапевта. И очень важно, что бы врачи этого звена могли своевременно назначить эффективную терапию таким пациентам.
Итак, в описанных выше клинических примерах мы встретились с трудностями дифференциальной диагностики хронического панкреатита и рака ПЖ. При наличии механической желтухи у больных хроническим панкреатитом, стойкого повышения активности липазы в крови, повышения уровня онкомаркеров следует заподозрить новообразование ПЖ. В качестве наиболее достоверных методов обследования рекомендуется использовать эндоскопическую ультрасонографию с тонкоигольной пункцией поджелудочной железы и компьютерную томографию органов брюшной полости.
Литература
1. Krejs G.J. Pancreatic cancer: epidemiology and risk factors. Digestive Diseases. 2010; 28: 2: 355–358.
2. Hǜser N., Assfalg V., Hartman D. et. al. Диагностика и хирургическое лечение рака поджелудочной железы. Экспериментальная и клиническая гастроэнтерология. 2011; 7: 102–111.
3. Bartosch- Härlid A., Andesson R, Diabetes Mellitus in Pancreatic Cancer and the Need for Diagnosis of Asymptomatic Disease. Pancreatology. 2010; 10: 4: 423–428.
4. Lilley M, Gilchrist D. The hereditary spectrum of pancreatic cancer: the Edmonton experience. Can J Gastroenterol. 2004; 18 (1): 17–21.
5. McKay C. J., Glen P., McMillan D.C. Chronic inflammation and pancreatic cancer. Clinical Gastroenterology. 2008; 22: 1: 65–73.
6. Raimondi S., Lowenfels A.B., Morselli-Labate A.M., Maisonneuve, Pezzilli R. Pancreatic cancer in chronic pancreatitis; aetiology, incidence, and early detection. Clinical Gastroenterology. 2010; 24: 3: 349–358.
7. Кармазановский Г.Г.,Кубышкин В.А., Вишневский В.А., Яшина Н.И. и др. Хронический псевдотуморозный панкреатит. Возможности дифференциальной лучевой диагностики. Материалы I Конгресса Московских хирургов. Неотложная и специализированная помощь. М.: 2005; 300.
8. Путов Н.В., Артемьев Н.Н., Коханенко Н.Ю. Рак поджелудочной железы. – М.: Питер, 2005; 396.
9. Bronstein Y.L., Loyer E.M., Kaur H. et al. Detection of small pancreatic tumors with multiphasic helical CT. AJR Am J Roentgenol. 2004; 182 (3): 619–623.
10. Bipat S., Phoa S.S., van Delden O.M. et al. Ultrasonography, computed tomography and magnetic resonance imaging for diagnosis and determining resectability of pancreatic adenocarcinoma: a meta-analysis. J Comput Assist Tomogr. 2005; 29 (4): 438–445.
11. Шапошникова Ю.Н. Аутоиммуный панкреатит: особенности диагностики и лечения. Сучасна Гастроэнтерологiя. 2011; 51: 1: 102–108.
12. Gardner T.B., Levy M.J. et al. Misdiagnosis of Autoimmune pancreatitis a caution to clinicians. Am. J. Gastroenterol. 2009; 104, iss.7advance online publicftion, 104. 1620–1623. – dol: 10.1038/fug.2008.
Источник