Что такое малигнизация поджелудочной железы
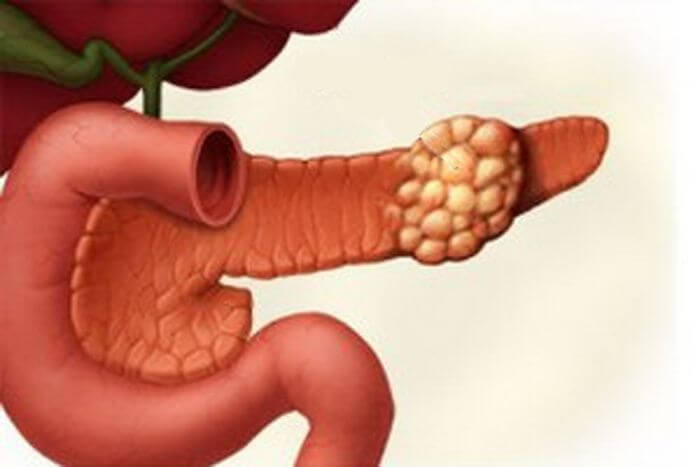
Опухоль поджелудочной железы симптомы и лечение. По своему происхождению новообразования в поджелудочной железе бывают доброкачественными или злокачественными.
Часто их выявляют после инструментального обследования других органов. На УЗИ однозначно вид опухоли не определить. При подозрении на новообразование в поджелудочной железе нужно обратиться к врачу, который назначит дополнительное всестороннее обследование.

Классификация опухолей
Новообразование в поджелудочной железе разделяются:
По локализации — месту возникновения в структуре железы:
- головка;
- тело;
- хвост;
- островки Лангерганса;
- протоки.
Гистологическому строению определяется, из каких клеток образовалась опухоль:
- эпителиальное происхождение;
- железистой паренхимы;
- из островкового эпителия;
- неэпителиального генеза;
- дизонтогенетические.
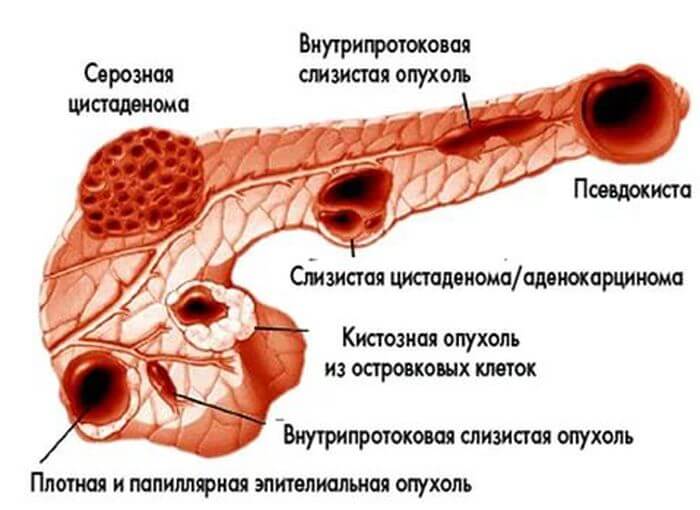
Функциональным нарушениям – состояние, связанное с изменением регуляции в организме: гормональной или нервной. Орган остается неповрежденным, но деятельность поджелудочной железы нарушается.
Симптомы
Развитие опухоли до поры протекает без видимых симптомов. Когда она разрастается и возможно прорастает в близлежащие органы: желудок, тогда появляются типичные симптомы, с которыми доктор знаком. По симптомам он назначает всестороннее обследование.
Злокачественная опухоль поджелудочной железы проявляет свои симптомы при значительном разрастании:
Закупорка протоков
Закупорке протоков (обтюрация) – появляется при сдавливании образованием органов, которые нарушают свое функционирование, и проявляется болями, свидетельствующими о том, что новообразование просочилось сквозь нервные окончания. У каждого пациент симптомы проявляются индивидуально и зависят от места возникновения.
Опухоль головки поджелудочной железы провоцирует боль в правом подреберье. Опухоль хвоста поджелудочной железы вызывает дискомфорт и боль в левом подреберье. Если образованием охвачено тело поджелудочной железы, то боль проявляется вкруговую, опоясывающая.
Боль сильно увеличивается при несоблюдении диеты, а также лежа на спине. Сдавливание органов приводит к закупорке желчных протоков, проявляющееся в оттоке желчи из печени в кишечник. Результатом становится механическая желтуха. У нее свои симптомы:
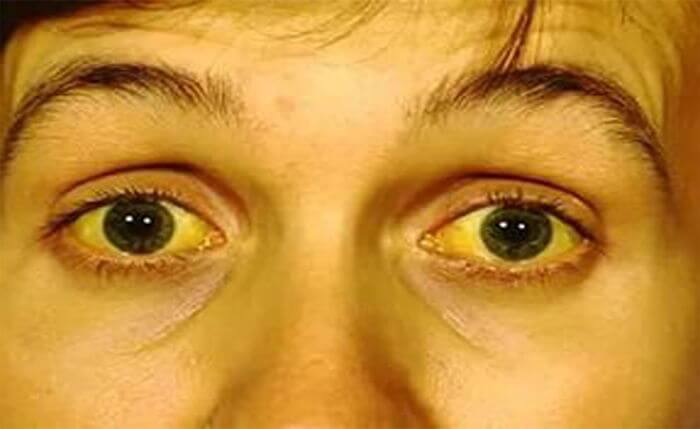
- желтушное окрашивание кожи, склер или слизистых оболочек;
- обесцвечивание стула;
- потемнение мочи;
- изменение размера печени и желчного пузыря в сторону увеличения;
- возникновение кожного зуда.
Рак поражает близлежащие органы, из которых может, в любой момент открыться кровотечение.
Интоксикация
Интоксикация организма. Ее признаки часто путают с признаками заболеваний и отклонений в ЖКТ. Симптомы похожи, но действие на организм интоксикации значительно тяжелее:
- резкое снижение веса;
- потеря аппетита;
- вялость, немощь, апатия;
- повышение температуры.
Доброкачественная опухоль поджелудочной железы позволяет классифицировать симптоматику 2 видов:
Ранняя стадия имеет бессимптомное течение, и приобретает их в процессе роста:
- боли вверху живота, подреберьях, правом или левом, отдающая в спину, усиливающаяся по ночам;
- дискомфорт и боль после приема пищи;
- постепенная потеря веса;
- тошнота, снижение аппетита, немощь и потеря трудоспособности.
Поздняя стадия – проявляется симптомами, как и при злокачественной опухоли. Помимо перечисленных выше, симптомов вызывает страх и нервные расстройства, повышает потоотделение. Симптомы могут возникать постепенно или внезапно. И они отличаются, завися от типа доброкачественного образования.
Риски возникновения
Точной причины появления раковых клеток нет. Но опухолевый процесс имеет свои факторы риска, о которых многие знают. Среди них:
- Вредные привычки: алкоголь, курение.
- Генная предрасположенность.
- Неправильное питание.
- Панкреатит.
- Неблагоприятная экологическая обстановка.
Диагностика
Всесторонне обследование пациента, используя различные методы исследования, позволит выяснить тяжесть опухоли: очаги, размеры, действие на соседние органы, метастазирование.
Обследование поможет определиться с методикой лечения:
- УЗИ. Позволяет увидеть новообразование, очаг его распространения.
- Компьютерная томография с введением контрастного вещества выявит не только очаги опухоли, но и метастазы, если они есть.
- Рентгенологические методы: А) Рентгенография определяет последствия прорастания опухоли на желудок и двенадцатиперстную кишку, сдавливание органов, диффузия слизистых оболочек, снижение моторики. В) Релаксационная дуоденография определяет локализацию опухоли и последствия ее разрастания. С) Ирригография выявляет дефекты в поперечно-ободочной кишке в результате прорастания опухоли.
- Эндоскопическая ретроградная холангиопанкреатография позволяет осмотреть желчную и панкреатическую системы с целью выявления их поражений. Взять материал для биопсии из неблагополучных очагов.
- Эндоскопический ультразвук. За счет технического оснащения: эндоскоп, видеокамера, ультразвуковой датчик, возможно, исследовать новообразование, введя инструменты через кишку. Такое исследование позволяет выявить новообразование на ранних стадиях.
- Рентгенохирургическая диагностика с контрастом позволяет выявить причины механической желтухи и смещение артерий.
- Радионуклидное исследование позволяет выявить закупорку общего с поджелудочной железой желчного протока.
- Нашумевший спорный тестер Джека Андраки, основан на анализе крови или мочи, используя специальную бумагу.
Главное в диагностике — установка медицинского диагноза на основании интерпретация полученных результатов исследования и анализов, формирование экспертного заключения.
Лечение
Необходимое лечение подбирается доктором на основании диагностики и анализов.
Хирургическая терапия всегда показана при обнаружении доброкачественного образования. Исследование гистологии со срезов образования позволит точно установить была ли она доброкачественной. Основные операции по удалению новообразований:
- Резекция состоит в удалении части поджелудочной железы, чаще в ее хвосте.
- Удаление непосредственно образования способом вылущивания. Выполняются для опухолей, которые продуцируют гормоны: доброкачественная инсулома.
- Панкреатодуоденальная резекция производится в случае размещения образования на головке железы. Оно удаляется вместе с 12-перстной кишкой.
- Селективная артериальная эмболизация закупоривает сосуд, на котором растет образование с целью отключить подпитку кровоснабжением. Используется при гемангиоме.
Химиотерапия
Химиотерапия призвана лечить злокачественное образование при помощи токсинов и ядов, которые называются химиопрепаратом. Она бывает: предоперационной, послеоперационной, профилактической, лечебной.
Поскольку раковые клетки бесконечно делятся, то химиотерапия циклично повторяется в расчете с клеточным циклом деления. Процедура состоит из капельного введения препарат или приёмом таблеток.
Наружная радиотерапия, являющаяся разновидностью терапии лучевой. Суть излечения — бомбардирование зоны новообразования излучением от медицинского ускорителя в виде пучка элементарных частиц. Проводится сеансами через фиксированный промежуток времени. Показания к применению:
- Сокращение размера опухоли на поджелудочной железе перед хирургическим вмешательством.
- Локально-возникшем раке поджелудочной железы.
- Уменьшение страданий при метастазах.
- Предотвращение рецидивов рака после хирургической операции.
Симптоматическая терапия направлена на снятие болей и облегчения страданий умирающего пациента: гормональная терапия – это лечение с помощью применения гормонов, способных тормозить рост рака. Продлевает продолжительность жизни.
Виротерапия применяет онкотропные или онколитические вирусы в терапевтических целях, мобилизуя против злокачественных клеток естественные защитные силы иммунной системы организма.
Нанонож как необратимая электропорация, разрушающая раковые клетки путем воздействия на них электрическим полем большой интенсивности локализовано. Для этого применяется специальный аппарат — нанонож.
В настоящее время слывет одним из самых результативных способов уничтожения опухоли в поджелудочной железе. Факт возможности повторения процедуры важное обстоятельство для повторного проведения при рецидивах или неоперабельном раке.
Шансы на выздоровление или жизнь после оперативного лечения
Сама операция на поджелудочной железе мало опасна. Прогноз оптимистичней при ранних сроках выполнения операции. Полностью выздоравливают пациенты с доброкачественными опухолями: глюкагономы, инсуломы, гастриномы и их разновидности
Рак поджелудочной железы имеет печальную статистику:
- На операцию поступают пациенты, у которых отсутствуют множественные метастазы, А это, как правило, лишь 15% больных. Для 85 % предоставляются виды лечения, направленные на продление жизни.
- Смертность на операционном столе у одного пациента из 6.
- Продолжительность жизни до 5 лет у каждого десятого больного после хирургического вмешательства, у остальных меньше.
После оперативного лечения возможны осложнения в функционировании организма. Любая операция влечет приспособление организма к потере органа или его части. Если орган жизненно важен, то адаптация проходит тяжелее. У пациентов после удаления опухоли поджелудочной железы, симптомы и лечение влекут 2 проблемы: сбои при пищеварении, снижение инсулина в организме.
Решаются проблемы дефицита путем назначения медикаментозных препаратов. При сопутствующих удалениях частей близлежащих органов: желудка, селезенки, двенадцатиперстной кишки врач посоветует надлежащую терапию и диету.
Профилактика
Поскольку ученые неутомимо работают над вопросом изучения причин, дающих толчок развитию рака, а ответа на них нет со 100 % достоверностью, поэтому руководства во избежание заболевания нет.
Лучший способ профилактики исключить знакомые всем факторы риска. Быть внимательным к себе при проявлениях болей в месте расположения железы. Не откладывать визит к доктору и хотя бы поверхностное обследование УЗИ.
Опухоль поджелудочной железы симптомы и лечение животрепещущая тема для многих страдающих заболеванием.
Источник
Малигнизация – процесс трансформации доброкачественных клеток в злокачественные. Может происходить в любых нормальных тканях или тканях доброкачественных опухолей. Сопровождается снижением уровня дифференцировки, изменением морфологических свойств, нарушением функции и бурным размножением клеток, прогрессирующим ростом новообразования и развитием отдаленных метастазов. Малигнизацию подтверждают на основании клинических данных, результатов лабораторных и инструментальных исследований. В процессе лечения опухоли обычно применяют хирургические вмешательства, химиотерапию и радиотерапию. Возможно использование гормонов, иммуностимуляторов и других препаратов.
Общие сведения
Малигнизация (озлокачествление, злокачественное перерождение) – сложный патоморфологический процесс, в ходе которого доброкачественные клетки приобретают свойства злокачественных. Малигнизации могут подвергаться как нормальные клетки, так и уже измененные, но не проявляющие признаков злокачественности. Чаще всего очаги озлокачествления возникают в области язв, полипов и различных доброкачественных опухолей. Причиной малигнизации могут стать генетическая предрасположенность и вредные факторы окружающей среды.
На начальных стадиях малигнизация протекает бессимптомно, поэтому ранняя диагностика злокачественных новообразований сопряжена со значительными затруднениями, однако регулярные профилактические осмотры, использование современных лабораторных и инструментальных методов исследования позволяют частично решить проблему раннего выявления малигнизации. Диагностику и лечение осуществляют специалисты в области онкологии, гастроэнтерологии, пульмонологии, неврологии, дерматологии, отоларингологии, гинекологии, ортопедии и врачи других специальностей (в зависимости от локализации опухоли).
В настоящее время злокачественные опухоли являются второй по распространенности причиной смертности после сердечно-сосудистых заболеваний. В 2012 году от рака умерло более 8 миллионов человек. Вероятность малигнизации увеличивается с возрастом, однако, наряду с людьми преклонных лет, злокачественные опухоли нередко поражают детей и пациентов трудоспособного возраста. Самыми распространенными видами рака являются рак легких, рак желудка, рак молочной железы, рак печени и рак толстого кишечника.
В результате малигнизации в человеческом организме может образовываться примерно 150 видов злокачественных клеток. Около 80% таких клеток имеют эпителиальное происхождение, 15% – соединительнотканное, 5% – гематогенное. По прогнозам специалистов, распространенность малигнизации в ближайшие десятилетия будет расти, что связано с целым рядом факторов, в том числе – с увеличением продолжительности жизни, неблагоприятной экологической обстановкой, вредными привычками, использованием большого количества химикатов, повышением уровня ионизирующего излучения и т. д. Все это обуславливает чрезвычайную важность изучения процессов малигнизации, а также разработки оптимальных алгоритмов выявления таких процессов при проведении массовых осмотров, диагностики и лечения неонкологических заболеваний.
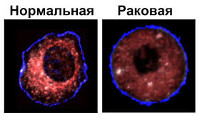
Малигнизация
Причины малигнизации
Причиной малигнизации клеток является сочетание нескольких факторов, в числе которых специалисты указывают химические канцерогены, особенности окружающей среды, некоторые вирусы, состояния гормонального дисбаланса, возраст, вредные привычки и неблагоприятную наследственность. При проведении исследований было установлено, что малигнизацию могут провоцировать более 2000 различных химических веществ, однако степень их влияния на процессы злокачественного перерождения клеток может сильно различаться.
В перечень химических соединений, безусловно, вызывающих малигнизацию клеток, входят полициклические ароматические углеводороды (источниками являются транспорт, промышленные предприятия и отопительные системы), нитрозамины (содержатся в сигаретах, некоторых сортах пива и амидопирине), производные гидразина (входят в состав гербицидов и некоторых лекарственных средств), асбест и другие минеральные волокна (источником являются промышленные производства), а также некоторые соединения металлов.
Самым значимым физическим фактором малигнизации является солнечное излучение, от уровня которого напрямую зависит вероятность развития рака кожи. Чем светлее кожа и волосы и чем дольше человек подвергается воздействию солнечных лучей – тем выше риск развития меланомы, базалиомы и плоскоклеточного рака кожи. Кроме того, малигнизацию может стимулировать ионизирующее излучение, провоцирующее возникновение лейкозов, костных опухолей (радиоактивный стронций) и рака щитовидной железы (радиоактивный цезий и йод).
Доказано, что вероятность малигнизации повышается при воздействии на клетки определенных вирусов, в частности – вируса ATLV (вызывает лейкоз), вируса Эпштейна-Барр (провоцирует развитие лимфомы Беркитта), вируса папилломы человека (играет определенную роль в возникновении рака шейки матки) и вируса герпеса II типа. Малигнизации также способствуют нарушения гормонального баланса. Гормоны могут напрямую провоцировать озлокачествление, действовать на клетки опосредованно, стимулируя их пролиферацию, оказывать негативное влияние на иммунитет и изменять метаболизм некоторых канцерогенов.
Существенную роль в процессе малигнизации играет генетическая предрасположенность. Описано множество наследственных заболеваний с высокой вероятностью малигнизации, например, системный полипоз кишечника, при котором у большинства пациентов к 40-50 годам развивается рак толстой кишки, или болезнь Дауна, при которой риск развития лейкоза в 11 раз выше, чем в среднем по популяции. Прослеживается связь между малигнизацией и врожденными пороками развития.
Выявляется зависимость между вероятностью малигнизации тканей определенных органов и полом пациента. Мужчины в 2,4 раза чаще страдают опухолями глаз, в 2,1 раза чаще – новообразованиями желудка, в 2 раза чаще – злокачественными поражениями носоглотки, в 1,7 раза – опухолями костей. У женщин вдвое чаще выявляется малигнизация тканей щитовидной железы. Первое место по распространенности у мужчин занимают опухоли дыхательных путей, у женщин – опухоли половых органов и молочной железы. В большинстве случаев вероятность малигнизации у пациентов обоих полов увеличивается с возрастом, однако некоторые виды новообразований чаще выявляются у детей или молодых людей.
В число привычек, оказывающих наиболее сильное влияние на малигнизацию клеток, входят курение, неправильное питание и прием алкоголя. У курящих рак легких развивается в 11 раз чаще; опухоли полости рта, гортани и глотки – в 7 раз чаще; новообразования мочевого пузыря – в 2,2 раза чаще; опухоли поджелудочной железы – 1,7 раз чаще, чем у некурящих. Основными пищевыми привычками, увеличивающими вероятность малигнизации, являются прием большого количества мясной, жирной, острой и пряной пищи, склонность к пересаливанию и употребление недостаточного количества растительной клетчатки. Алкоголь сам по себе не вызывает малигнизацию, но выступает в роли активатора, усиливая воздействие других факторов.
Стадии и этапы малигнизации
Начальной стадией малигнизации является инициация – мутация клеток под воздействием внутренних или внешних вредных факторов. В геноме клетки появляются клеточные или вирусные онкогены – измененные гены, вызывающие рост и размножение дефектных клеток. В организме человека постоянно образуются дефектные клетки, но в норме процесс малигнизации прерывается на этапе инициации, поскольку такие клетки подвергаются апоптозу – регулируемому процессу клеточной гибели. При одновременном выключении генов, вызывающих апоптоз, и активации генов, препятствующих апоптозу, дефектные клетки не погибают, а продолжают развиваться.
При повторном воздействии на клетки того же или другого вредного фактора наступает вторая стадия малигнизации – промоция. Онкогены активизируются, стимулируя пролиферацию дефектных клеток. Однако, даже этого недостаточно для развития злокачественной опухоли. Рост новообразования становится возможным только после прохождения третьей стадии малигнизации – уклонения дефектных клеток от процесса дифференцировки. Уклонение обычно происходит под влиянием определенных микроРНК.
Кроме того, переход на третью стадию малигнизации может быть обусловлен недостатком цитокининов, способствующих переходу клетки на более высокий уровень дифференцировки. Со временем количество низкодифференцированных клеток увеличивается, возникает микроскопический участок измененной ткани. Клетки с преобладающим набором хромосом формируют так называемую стволовую линию – основу опухоли. Одной из особенностей малигнизации является генетическая нестабильность клеток, из-за которой клеточный состав новообразования постоянно меняется, вместо одной стволовой линии появляются другие.
Измененные клетки, утратившие способность реагировать на внешние воздействия (влияние микросреды, иммунный надзор), продолжают активно делиться. Наступает четвертая стадия развития злокачественного новообразования – опухолевая прогрессия. Ткань, изменившаяся в процессе малигнизации, прорастает соседние органы, разрушает стенки кровеносных и лимфатических сосудов. Клетки новообразования попадают в кровь и лимфу, а затем разносятся по организму, «оседая» в лимфатических узлах и отдаленных органах. Из «осевших» клеток формируются новые очаги опухолевого роста – вторичные новообразования (метастазы).
С точки зрения свойств ткани можно выделить следующие этапы малигнизации: гиперплазия ткани, появление участков очаговой пролиферации, возникновение доброкачественной опухоли, образование участков дисплазии, рак in situ (злокачественная опухоль, не прорастающая окружающие ткани), инвазивное злокачественное новообразование. В ряде случаев этап доброкачественной опухоли может отсутствовать. Этапы очаговой пролиферации, доброкачественной опухоли и дисплазии рассматриваются, как предраковые состояния.
Свойства опухоли после малигнизации
Злокачественные новообразования обладают рядом свойств, отсутствующих у любых нормальных клеток и тканей организма:
- В результате малигнизации опухоль становится способной к быстрому росту, сопровождающемуся сдавлением или разрушением окружающих тканей.
- При озлокачествлении у новообразования возникает способность к инфильтрации (внедрению) в окружающие ткани.
- После малигнизации у опухоли появляется способность к распространению путем метастазирования. Клетки злокачественного новообразования мигрируют с током крови и лимфы, а затем «оседают» в различных органах и тканях, давая начало вторичным опухолям (метастазам). Установлено, что существует определенная «тропность» – склонность к метастазированию в те или иные органы и ткани в зависимости от вида первичного новообразования.
- При малигнизации у опухоли возникает способность вырабатывать токсины, оказывающие выраженное негативное влияние на организм пациента. Развитие злокачественного новообразования сопровождается общей интоксикацией, утомляемостью, снижением аппетита и потерей веса вплоть до кахексии.
- После озлокачествления измененные клетки оказываются за пределами контроля иммунной системы организма.
- Малигнизация сопряжена с высокой склонностью к мутациям, в результате которых клетки обретают необычные способности (способность к неконтролируемому росту, к отсутствию реакции на иммунные воздействия, к метастазированию и т. д.).
- Для малигнизации характерен низкий уровень дифференцировки клеток. Чем ниже уровень зрелости клеток, тем злокачественнее опухоль, тем быстрее она прогрессирует и дает метастазы, тем выше ее устойчивость к химиотерапии и радиотерапии.
- Злокачественное новообразование обладает выраженным клеточным и тканевым атипизмом.
- В процессе малигнизации у измененных клеток и тканей появляется способность стимулировать рост кровеносных сосудов. Ткань злокачественной опухоли хорошо васкуляризована, в ней часто возникают кровоизлияния.
Источник
